Clear Sky Science · es
Una subpoblación proinflamatoria de neutrófilos impulsa la lesión por isquemia‑reperfusión intestinal vía la vía de estrés del retículo endoplásmico mediada por ATF4
Cuando el flujo sanguíneo daña el intestino
Cirujanos y médicos de cuidados intensivos llevan tiempo perplejos ante una paradoja peligrosa: cuando se interrumpe el suministro de sangre al intestino y luego se restaura, el propio acto de restablecer el flujo puede dañar gravemente el revestimiento intestinal. Este proceso, denominado lesión por isquemia‑reperfusión intestinal, puede provocar complicaciones potencialmente mortales como sepsis y fallo multiorgánico. El estudio resumido aquí revela que no todas las células inmunitarias que acuden al lugar actúan igual: una subpoblación de glóbulos blancos especialmente agresiva desempeña un papel central en convertir una respuesta salvavidas en una respuesta dañina.
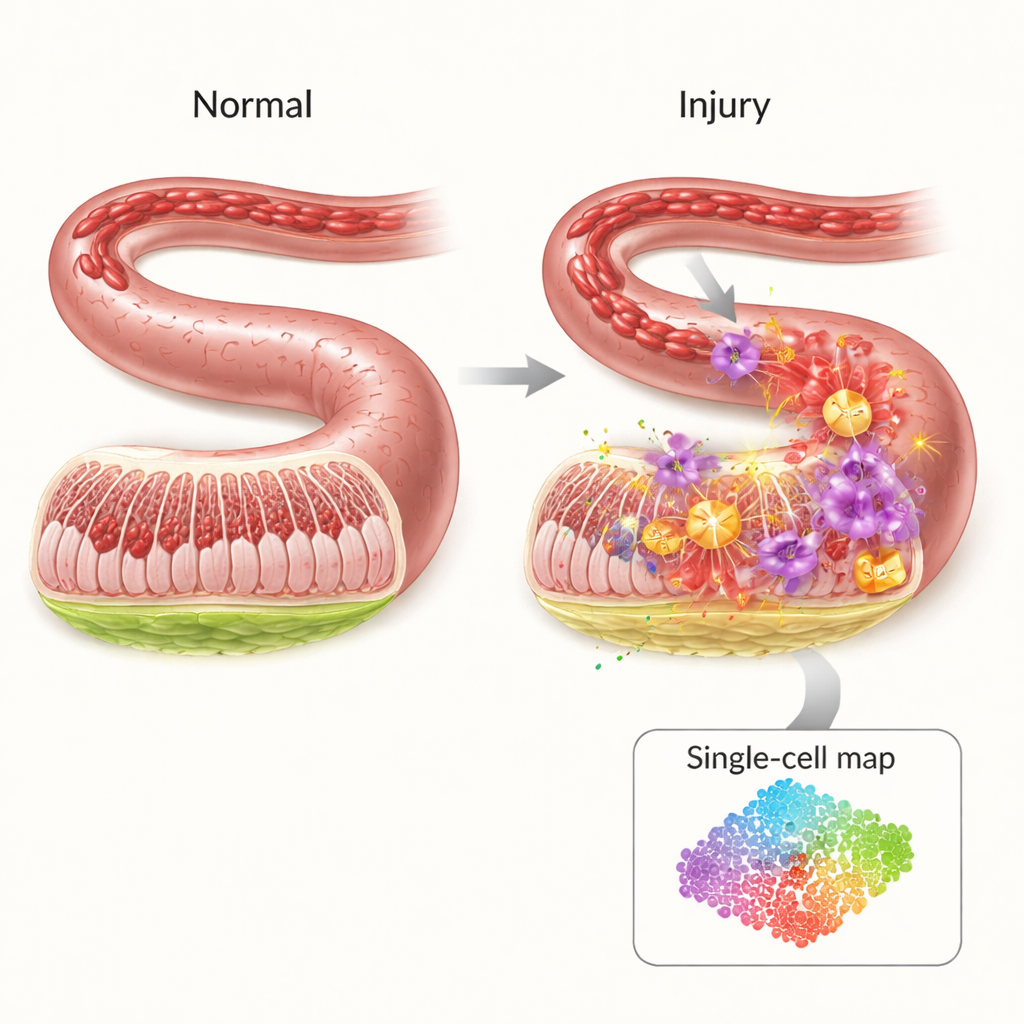
El frágil muro protector del intestino
El interior del intestino está recubierto por una barrera delgada pero altamente organizada que mantiene bacterias y toxinas confinadas en el tracto intestinal mientras permite el paso de nutrientes. Cuando se interrumpe el flujo sanguíneo —por ejemplo durante un shock, una cirugía mayor o un trauma severo— esta barrera se queda sin oxígeno. Sorprendentemente, la mayor parte del daño no ocurre durante la falta de riego sino cuando la circulación vuelve. La llegada súbita de oxígeno y de células inmunitarias desencadena una tormenta de señales inflamatorias y moléculas reactivas que pueden perforar la pared intestinal, permitiendo que gérmenes se filtren al torrente sanguíneo. A pesar de su importancia clínica, hoy los médicos disponen de pocos tratamientos dirigidos para prevenir esta cascada.
Acercándose a las células individuales
Para descubrir quién hace qué durante esta crisis, los investigadores emplearon secuenciación de ARN unicelular, una técnica que lee qué genes están activos en miles de células individuales a la vez. En un modelo murino de isquemia‑reperfusión intestinal, compararon intestinos lesionados con sanos y cartografiaron 19 tipos celulares principales. Encontraron que ciertas células inmunitarias —especialmente neutrófilos y monocitos inflamatorios— se expandieron de forma dramática tras la lesión, mientras que células protectoras como linfocitos T, linfocitos B y células asesinas naturales disminuyeron. Las redes de comunicación entre tipos celulares también cambiaron, emergiendo los neutrófilos como centros clave que envían y reciben numerosas señales inflamatorias, lo que los señala como impulsores fundamentales del daño.
Una subpoblación dañina de células de primera respuesta
Los neutrófilos son de los primeros respondedores más rápidos del organismo, desplazándose por la sangre para combatir infecciones y limpiar restos. Pero este estudio muestra que dentro de la población de neutrófilos existe un subgrupo particularmente agresivo responsable de gran parte del daño colateral en el intestino. Cuando los científicos eliminaron neutrófilos en ratones antes de inducir la isquemia‑reperfusión, los animales presentaron menos acortamiento intestinal, niveles más bajos de marcadores de lesión en sangre, mejor aspecto tisular al microscopio y proteínas de sellado más intactas en el revestimiento intestinal. En experimentos de cocultivo, los neutrófilos tomados de ratones lesionados dañaron directamente las células intestinales, reduciendo su supervivencia, aumentando la muerte celular y alterando las proteínas en forma de «cierre» que mantienen la integridad de la barrera intestinal.
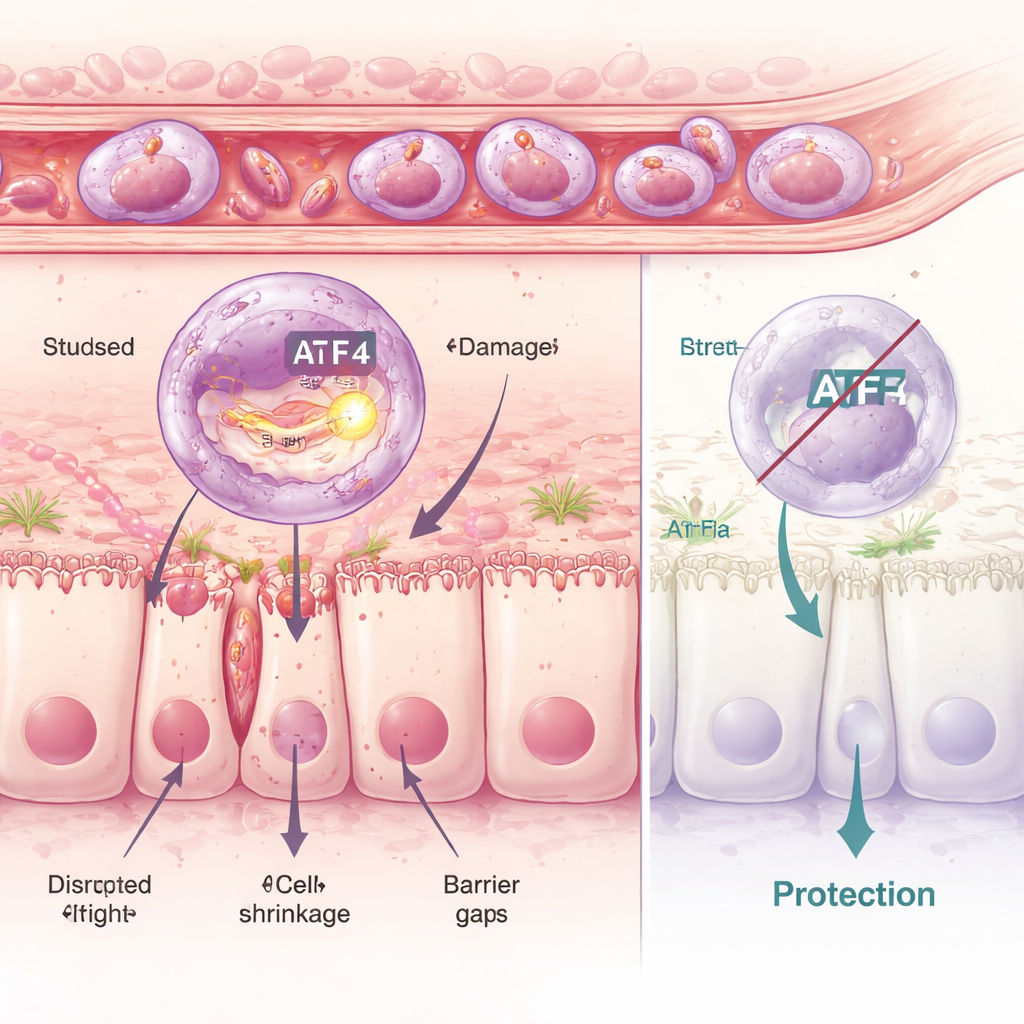
Estrés dentro de las células: cuando falla el control de calidad
Profundizando, los investigadores examinaron neutrófilos uno por uno e identificaron seis subgrupos distintos. Uno, denominado cúmulo C5, destacó por su fuerte perfil inflamatorio y por activar un programa molecular de estrés dentro de una estructura llamada retículo endoplásmico, la «taller» celular donde se pliegan las proteínas. Un regulador clave de este programa es una proteína llamada ATF4. En las células C5 dañinas, ATF4 y sus genes diana estaban muy activos. Usando fármacos que o bien aumentan o bien disminuyen esta respuesta de estrés interna, el equipo mostró que más estrés significaba más daño intestinal, mientras que bloquearlo preservaba la barrera intestinal. Ratones modificados genéticamente para carecer de ATF4 estuvieron en gran medida protegidos: incluso cuando se administraron fármacos que inducen estrés, sus neutrófilos ya no podían ejecutar por completo su programa dañino y el revestimiento intestinal permaneció mucho más intacto.
Qué significa esto para tratamientos futuros
En conjunto, estos hallazgos dibujan una imagen clara para el público general: entre el enjambre de células inmunitarias que inundan el intestino cuando vuelve el flujo sanguíneo, una subpoblación específica de neutrófilos primada por el estrés actúa como un equipo de limpieza demasiado entusiasta que derriba el edificio junto con los escombros. Su poder destructivo depende de una vía de estrés interna controlada por ATF4. Atenuar esta vía —sin eliminar todos los neutrófilos— podría ofrecer una manera de proteger el intestino durante situaciones de alto riesgo como cirugías mayores, infecciones graves o traumatismos. Aunque se necesita más trabajo para confirmar estos resultados en humanos y encontrar fármacos seguros y precisos, el estudio abre una ruta prometedora hacia terapias que mantengan la barrera intestinal intacta cuando los pacientes más lo necesitan.
Cita: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
Palabras clave: barrera intestinal, isquemia reperfusión, neutrófilos, estrés del retículo endoplásmico, ATF4