Clear Sky Science · es
La metadinámica revela la estabilización conformacional mediada por luteolina frente a PDGFRα D842V/G680R resistente a avapritinib en GIST
Por qué esto importa para el tratamiento del cáncer
Los fármacos dirigidos contra el cáncer pueden funcionar de forma notable, hasta que los tumores evolucionan y encuentran maneras de esquivarlos. Este artículo explora cómo un compuesto vegetal común, la luteolina, podría ayudar a restaurar la eficacia de un fármaco importante usado contra ciertos tumores del estroma gastrointestinal (GIST), un tipo de cáncer del tracto digestivo. Mediante simulaciones computacionales avanzadas, los investigadores muestran cómo la luteolina podría estabilizar una proteína deformada en las células cancerosas para que el fármaco existente pueda acoplarse de nuevo, sugiriendo una nueva forma de combatir la resistencia a fármacos sin reinventar el tratamiento desde cero. 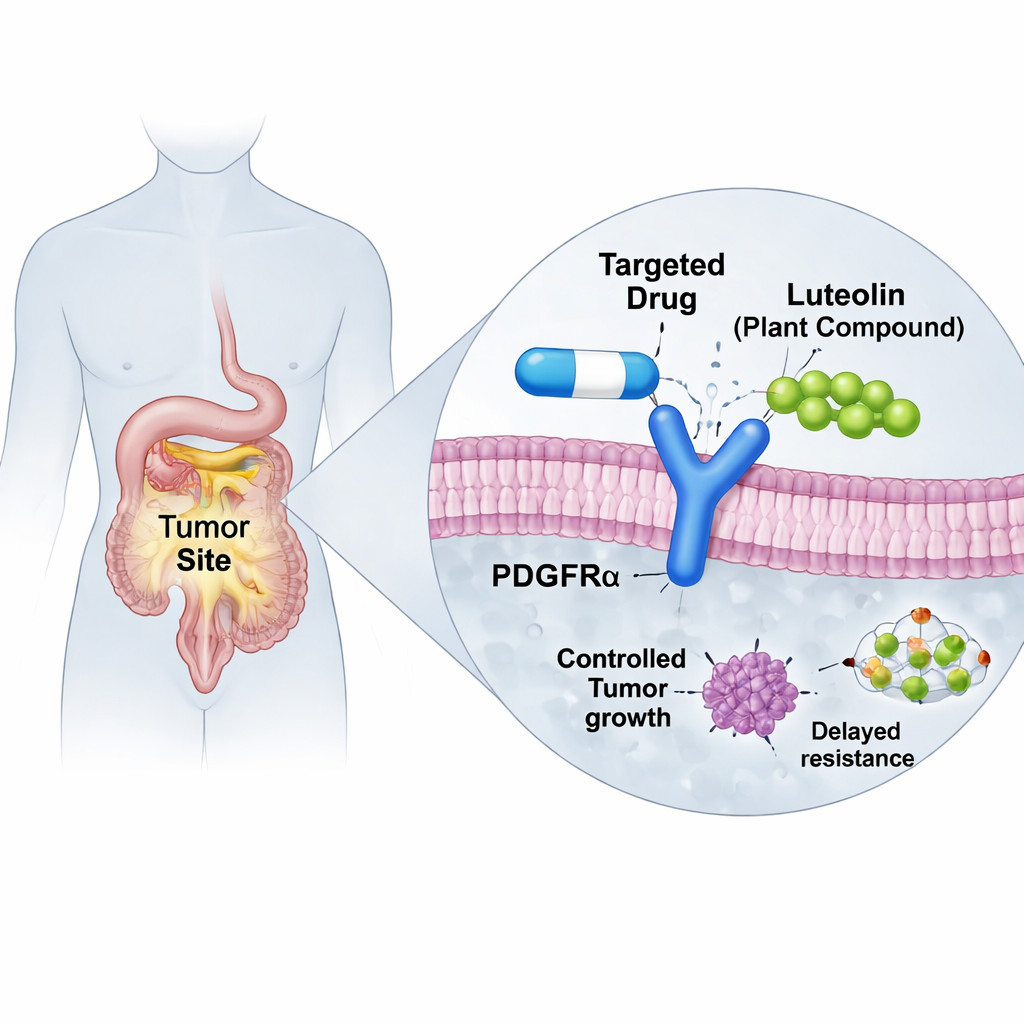
El problema de los tumores que aprenden a esquivar los fármacos
Los GISTs a menudo crecen debido a interruptores "de encendido" defectuosos en proteínas de la superficie celular conocidas como KIT o PDGFRα, que impulsan señales de crecimiento constantes. Las píldoras modernas llamadas inhibidores de tirosina quinasa fueron diseñadas para apagar esos interruptores y han transformado los resultados de muchos pacientes. Pero una mutación frecuente en PDGFRα, llamada D842V, hace que el fármaco más antiguo imatinib sea en gran medida inútil. Un fármaco más reciente, avapritinib, fue desarrollado específicamente para dominar a este mutante obstinado y ha mostrado un éxito notable en ensayos clínicos. Desafortunadamente, los tumores aún pueden adaptarse. Algunos pacientes desarrollan cambios adicionales en PDGFRα, como una mutación secundaria G680R, que bloquea físicamente que el avapritinib encaje cómodamente en su bolsillo de unión, provocando que el fármaco se desplace y aumente la resistencia.
Una molécula vegetal con una forma intrigante
Los productos naturales son una fuente rica de ideas para fármacos, y los flavonoides —compuestos coloridos presentes en muchas frutas, verduras y plantas medicinales— son conocidos por interactuar con proteínas que controlan el crecimiento dentro de las células. La luteolina, uno de esos flavonoides presente en un arbusto mediterráneo llamado Retama monosperma, ya se ha estudiado por sus propiedades anticancerígenas y antiinflamatorias y parece segura en niveles alcanzables mediante suplementos orales. Basándose en trabajos de cribado previos, los autores sospecharon que la luteolina podría adherirse a PDGFRα en un sitio cercano, pero no superpuesto, al sitio habitual de unión del fármaco. Si fuera cierto, esto podría permitir que la luteolina actúe como una especie de refuerzo sutil, empujando la proteína hacia una conformación que vuelva a recibir al avapritinib.
Simulando una asociación molecular
Para probar esta idea in silico, el equipo construyó modelos computacionales tridimensionales detallados de la proteína PDGFRα resistente que portaba tanto las mutaciones D842V como G680R. Simularon cómo se comportaba el avapritinib por sí solo y cómo se comportaba cuando la luteolina estaba presente en las cercanías, rastreando los movimientos atómicos durante cientos de nanosegundos —miles de millones de segundos en tiempo real. Cuando solo estaba unido el avapritinib, el fármaco gradualmente se desplazó fuera de su bolsillo a medida que el voluminoso cambio G680R lo empujaba, terminando completamente separado de la proteína. En contraste, cuando la luteolina también estaba unida en un sitio "alostérico" separado junto a una hélice clave, el avapritinib se mantuvo en gran medida en su lugar. La proteína en su conjunto se flexionó menos, segmentos estructurales clave conservaron su forma y los contactos importantes entre el fármaco y la proteína persistieron durante mucho más tiempo. 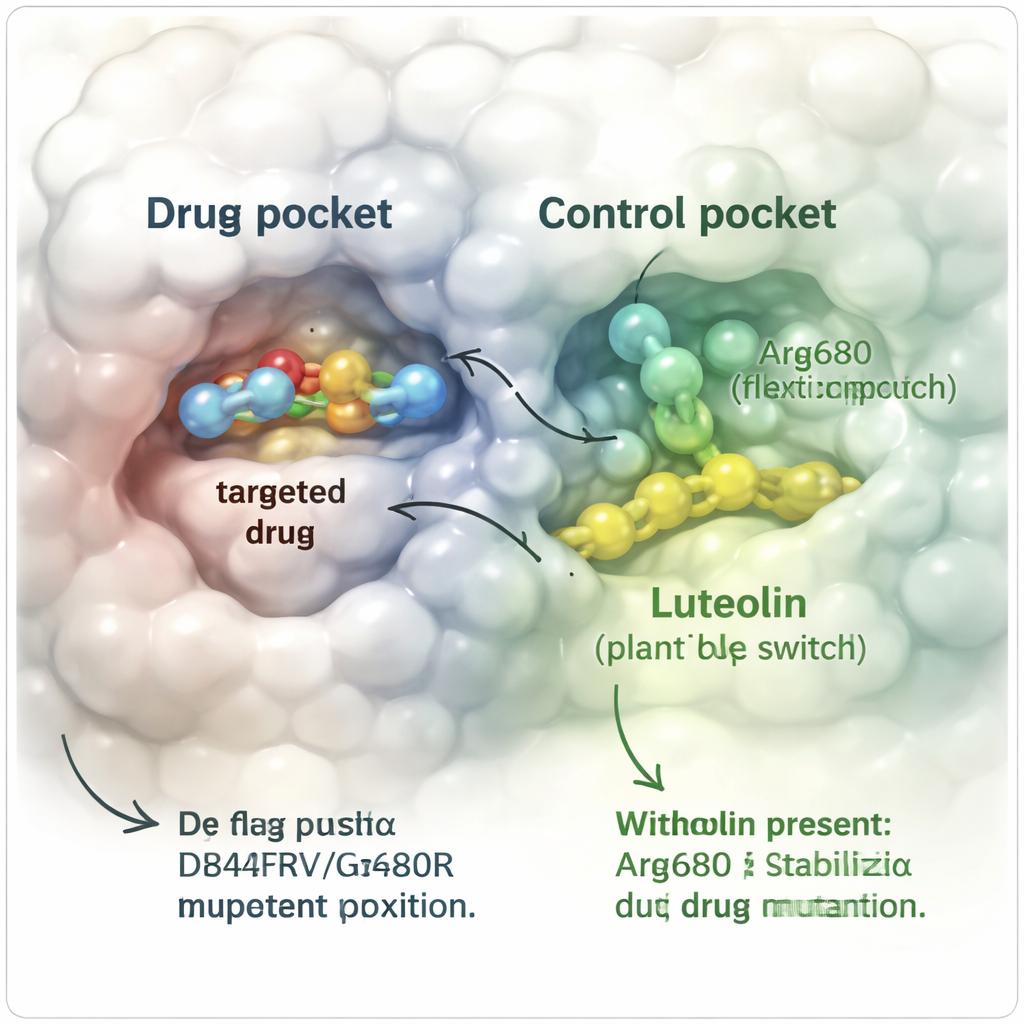
Asegurando un interruptor molecular descarriado
Las simulaciones estándar aún omiten cambios conformacionales raros pero importantes, por lo que los investigadores recurrieron a un enfoque mejorado llamado metadinámica para explorar más a fondo cómo la proteína podría torcerse y doblarse. Se centraron en el comportamiento del aminoácido alterado Arg680, que actúa como un pequeño brazo flexible cerca del bolsillo del fármaco. Sin luteolina, este brazo muestreaba muchas posiciones y el fármaco se deslizaba con facilidad, con barreras energéticas relativamente bajas para escapar. Con la luteolina en su sitio, Arg680 quedó retenido en una orientación específica que ya no chocaba con el fármaco. El paisaje energético cambió: el sistema pasó a preferir conformaciones en las que el avapritinib permanecía unido, y la "colina" energética que el fármaco tendría que escalar para escapar aumentó varios kilocalorías, haciendo que la disociación fuera mucho menos probable.
Qué podría significar esto para los pacientes
En términos sencillos, el estudio sugiere que la luteolina puede actuar como una férula molecular, estabilizando una proteína cancerosa deformada para que una píldora dirigida existente pueda agarrarla de nuevo. En lugar de diseñar un fármaco totalmente nuevo para cada mutación de resistencia, combinar la medicina actual con un compuesto ayudante cuidadosamente elegido podría restaurar su eficacia. El trabajo se basa en métodos computacionales potentes pero puramente teóricos, por lo que se necesitan todavía estudios en laboratorio y en animales para confirmar si la luteolina, o una molécula relacionada diseñada para mejores propiedades farmacológicas, realmente potencia al avapritinib en sistemas vivos. Aun así, el concepto de usar pequeños ayudantes alostéricos para reestabilizar dianas cancerosas resistentes podría abrir un nuevo camino para extender la vida útil de las terapias de precisión actuales.
Cita: El Khattabi, K., Akachar, J., Lemriss, S. et al. Metadynamics reveals luteolin-mediated conformational stabilization against avapritinib-resistant PDGFRα D842V/G680R GIST. Sci Rep 16, 6534 (2026). https://doi.org/10.1038/s41598-026-36898-0
Palabras clave: resistencia a fármacos, tumor del estroma gastrointestinal, inhibidores de tirosina quinasa, luteolina, modulación alostérica