Clear Sky Science · es
Síntesis y evaluación anticancerígena de nuevos derivados de tioimidazol con una fracción trimetoxifenil
Nuevas herramientas químicas en la lucha contra el cáncer
Los fármacos de quimioterapia suelen dañar tanto las células sanas como los tumores, provocando efectos secundarios severos. Este estudio explora una nueva familia de moléculas sintéticas que buscan atacar las células cancerosas con mucha más contundencia que el tejido normal. Al combinar de forma inteligente dos bloques químicos ya conocidos por su eficacia en medicamentos, los investigadores crearon compuestos que muestran una potente y dirigida capacidad de matar células cancerosas en modelos in vitro y en modelos tumorales 3D, mientras dejan en gran medida indemnes a las células sanas.
Diseñar moléculas asesinas de cáncer más inteligentes
El equipo se centró en dos estructuras químicas “privilegiadas” que aparecen repetidamente en fármacos exitosos. Una es el imidazol, un anillo pequeño que encaja bien en muchos objetivos biológicos. La otra es el grupo trimetoxifenil (TMP), un patrón de tres cadenas portadoras de oxígeno en un anillo aromático que es central en varios fármacos anticancerígenos que alteran la división celular. Al introducir un átomo de azufre en el núcleo del imidazol (creando un tioimidazol) y unirlo a un grupo TMP, los químicos esperaban afinar cómo se desplazan las moléculas por el organismo y con qué afinidad se unen a proteínas relacionadas con el cáncer. Mediante una ruta sintética escalonada, construyeron una biblioteca de compuestos relacionados, cada uno modificado de forma sutil para sondear qué características son más importantes para la actividad anticancerígena. 
Probar células cancerosas mientras se preserva el tejido sano
Las nuevas moléculas se probaron en cuatro líneas celulares humanas de cáncer: osteosarcoma (hueso), cervical, colon y pulmón, así como en fibroblastos pulmonares no cancerosos. Muchos de los compuestos ralentizaron o detuvieron el crecimiento de las células cancerosas, pero uno en particular, denominado 13b, destacó. Mató células de cáncer de hueso y cervical a concentraciones muy bajas, sin mostrar toxicidad detectable hacia los fibroblastos normales incluso a dosis más de 60 veces superiores. Varios otros compuestos fueron moderadamente potentes pero menos selectivos, lo que subraya cómo cambios estructurales pequeños —como añadir un átomo de cloro o un grupo nitro en posiciones específicas— pueden inclinar la balanza entre toxicidad amplia y acción dirigida al cáncer.
Cómo el compuesto líder induce la autodestrucción de las células cancerosas
Para entender qué hace realmente 13b dentro de las células, los investigadores buscaron signos de muerte celular programada, o apoptosis. Las células cancerosas tratadas con 13b dieron positivo para Annexina V y activaron las enzimas caspasa-3 y -7, marcadores clásicos de que la célula ha sido empujada a un programa ordenado de suicidio en lugar de reventar de forma desordenada. La microscopía reveló puntos brillantes de γH2AX, una señal de roturas en las hebras de ADN, en los núcleos de las células tratadas. Con el tiempo, el armazón interno de las células empezó a reorganizarse y desintegrarse, especialmente en células de cáncer cervical, que se redondearon y se desprendieron —señales visuales de que la apoptosis estaba en marcha. En conjunto, estos hallazgos muestran que 13b daña el ADN de las células cancerosas y luego las empuja por una vía controlada de muerte celular.
De monocapas a mini-tumores 3D
La mayoría de las pruebas de laboratorio cultivan células cancerosas en capas finas, que no imitan completamente la estructura densa y estratificada de los tumores reales. Para abordar esto, el equipo cultivó las células cancerosas en esferoides tridimensionales —pequeños agregados esféricos que se asemejan mejor a la arquitectura tumoral y a los desafíos de penetración de fármaco. Cuando estos esferoides se trataron con 13b, se redujeron en tamaño de forma dependiente de la dosis. Los esferoides de cáncer óseo fueron especialmente sensibles, volviéndose pequeños, sueltos y fragmentados a niveles más altos del fármaco. El teñido fluorescente mostró oleadas de apoptosis que se desplazaban desde el exterior del esferoide hacia el interior a medida que aumentaba la concentración, demostrando que 13b puede penetrar y matar células a lo largo de estas estructuras compactas. 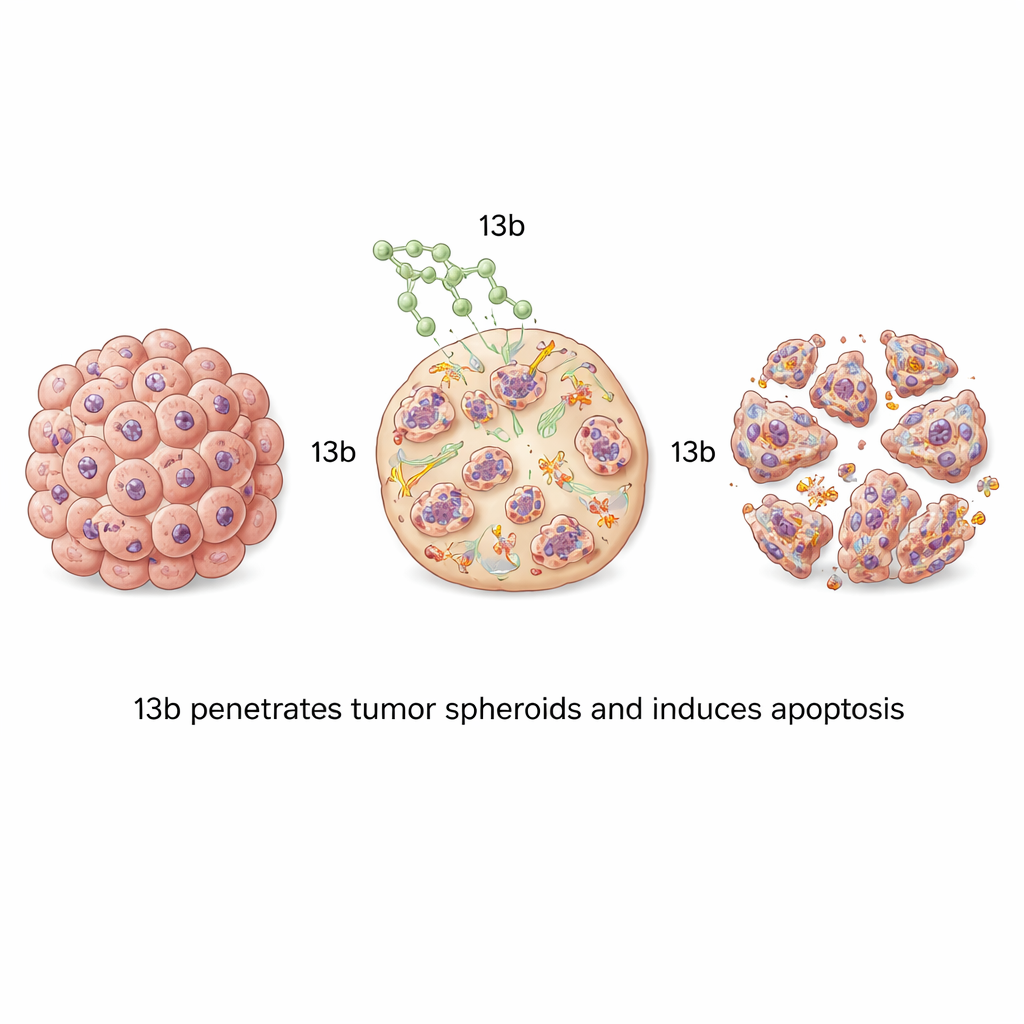
Por qué este trabajo importa para futuros tratamientos contra el cáncer
Para un público no especializado, el mensaje clave es que los investigadores han creado una nueva clase de pequeñas moléculas que combinan lo mejor de dos componentes farmacológicos probados en un único diseño híbrido. Su compuesto principal, 13b, es capaz de reconocer y destruir células cancerosas con eficiencia mientras preserva en gran medida a las células sanas en pruebas de laboratorio, y además sigue siendo eficaz en modelos tumorales 3D más realistas. Aunque queda mucho trabajo por delante —como identificar sus dianas moleculares exactas, mejorar su solubilidad y evaluarlo en animales—, este estudio muestra que fusionar las arquitecturas de tioimidazol y TMP es una estrategia prometedora para diseñar agentes anticancerígenos más selectivos y potentes.
Cita: Maciejewska, N., Grybaitė, B., Anusevičius, K. et al. Synthesis and anticancer evaluation of novel thioimidazole derivatives bearing a trimethoxyphenyl moiety. Sci Rep 16, 6271 (2026). https://doi.org/10.1038/s41598-026-36890-8
Palabras clave: agentes anticancerígenos, derivados de imidazol, trimetoxifenil, apoptosis, esferoides tumorales 3D