Clear Sky Science · es
Beneficio y riesgo asociados a la administración de inhibidores del receptor de interleucina‑6 durante COVID‑19 grave: estudio retrospectivo multicéntrico
Por qué esto importa para pacientes y familias
Durante la pandemia de COVID‑19, los médicos necesitaban con urgencia tratamientos para ayudar a los pacientes más graves a sobrevivir, especialmente a quienes tenían dificultades respiratorias. Una opción prometedora fue una clase de fármacos que bloquean la interleucina‑6 (IL‑6), un potente mensajero de la inflamación en el organismo. Estos medicamentos, como el tocilizumab y el sarilumab, pueden aplacar una respuesta inmune desbocada, pero también pueden debilitar las defensas del cuerpo frente a los gérmenes. Este estudio plantea una pregunta sencilla pero crucial: cuando se usan en hospitales reales durante casos graves de COVID‑19, ¿estos fármacos ayudan más de lo que dañan?
Cómo se diseñó el estudio
Investigadores en París revisaron retrospectivamente las historias clínicas de 2.587 adultos hospitalizados con COVID‑19 grave o crítico entre marzo de 2020 y diciembre de 2021. Algunos pacientes permanecieron solo en plantas de hospitalización, mientras que otros necesitaron unidades de cuidados intensivos (UCI) por fallo orgánico o por requerir ventilación mecánica. Dentro de estos grupos, una minoría —224 personas, alrededor del 9%— recibió al menos una dosis de un inhibidor del receptor de IL‑6 (IL‑6Ri), principalmente tocilizumab y, en menor medida, sarilumab. El equipo comparó a los pacientes que recibieron y no recibieron estos fármacos, centrando la atención en efectos adversos graves como las infecciones nosocomiales, hemorragias digestivas y alteraciones sanguíneas como trombocitopenia o leucopenia.
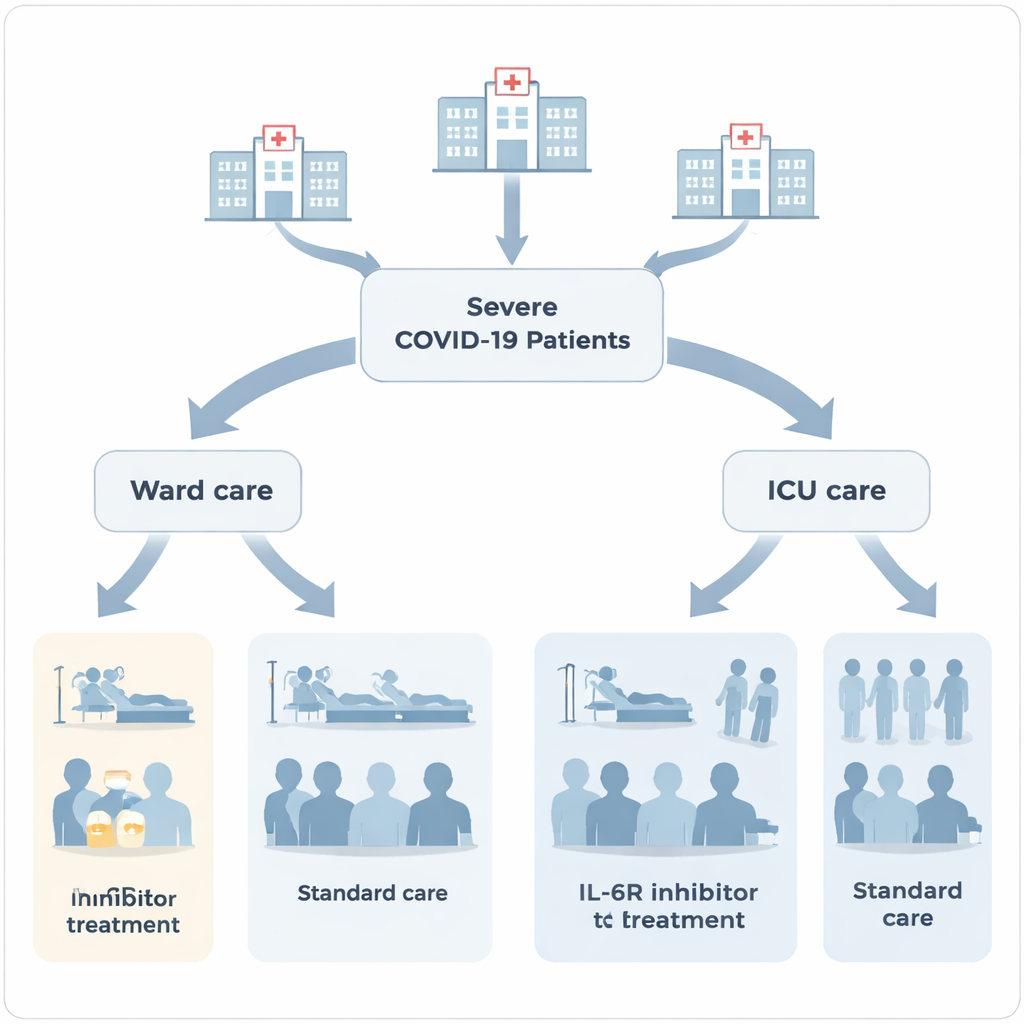
Qué ocurrió con los pacientes en las plantas
Entre los 1.603 pacientes que permanecieron en plantas, los tratados con IL‑6Ri tendían a estar más graves: con más frecuencia necesitaron oxígeno de alto flujo, permanecieron más tiempo en el hospital y recibieron con mayor frecuencia otros tratamientos como corticosteroides y anticoagulantes. En este grupo, el riesgo de morir en el hospital fue mayor para los pacientes que recibieron IL‑6Ri (alrededor del 19%) frente a los que no los recibieron (aproximadamente el 10%). Al mismo tiempo, la duración de la estancia fue mayor —10 días frente a 7 días de media. Aunque estas diferencias podrían en parte reflejar que los médicos reservaron los IL‑6Ri para los pacientes más frágiles, plantearon dudas sobre si los fármacos mejoraban claramente los resultados fuera de la UCI.
Qué sucedió en cuidados intensivos
En los 984 pacientes que necesitaron atención en UCI, los patrones de tratamiento fueron algo distintos. Aquí, 133 pacientes recibieron un IL‑6Ri. Tanto los pacientes de la UCI tratados como los no tratados requirieron altas tasas de soporte avanzado como ventilación mecánica, decúbito prono y, en ocasiones, oxigenación por membrana extracorpórea (ECMO), una forma de bypass corazón‑pulmón. En este grupo más grave, las tasas de mortalidad hospitalaria fueron similares tanto si los pacientes recibieron IL‑6Ri como si no: aproximadamente una de cada cuatro murió en cada grupo. Las estancias en UCI y el tiempo total de hospitalización también fueron, en líneas generales, parecidos. En otras palabras, en esta población de UCI en el mundo real, bloquear la IL‑6 no mejoró la supervivencia de forma clara, pero tampoco la empeoró.
El riesgo clave: más infecciones
El hallazgo más llamativo surgió cuando los investigadores analizaron las nuevas infecciones desarrolladas durante la hospitalización, como la neumonía asociada al ventilador, infecciones del tracto urinario, bacteriemias y otras infecciones nosocomiales. En toda la población, los pacientes que recibieron un IL‑6Ri presentaron más infecciones secundarias que los que no lo recibieron. Tras ajustar cuidadosamente por edad, peso, comorbilidades y gravedad de la enfermedad, el uso de IL‑6Ri seguía asociado a un mayor riesgo de infección —aproximadamente un aumento relativo del 40% al 100%, dependiendo del método de análisis. Este riesgo añadido no se limitó a un tipo concreto de germen ni a un sitio de infección específico. En contraste, las hemorragias digestivas graves y las complicaciones hematológicas ocurrieron a tasas similares con o sin tratamiento con IL‑6Ri, lo que sugiere que estos temidos efectos adversos no se amplificaron de forma apreciable por los fármacos en este contexto.
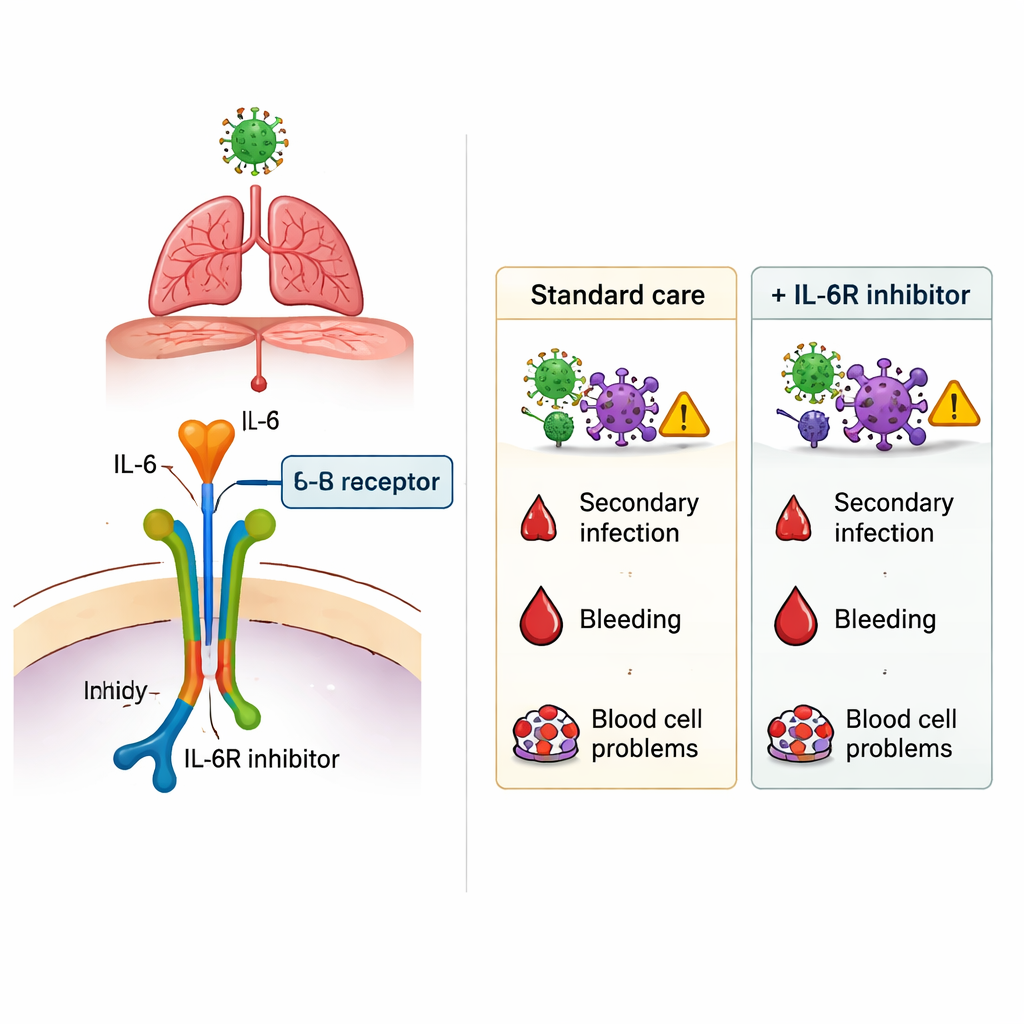
Qué implica esto de cara al futuro
Para el lector no especializado, la conclusión es que fármacos como el tocilizumab y el sarilumab pueden modificar de forma modesta la evolución del COVID‑19 grave, pero no están exentos de coste. En este amplio estudio francés, su uso se asoció a una mayor probabilidad de infecciones nosocomiales, mientras que la supervivencia en los pacientes más graves en UCI no mejoró de forma clara y los pacientes en planta que los recibieron murieron con más frecuencia. El estudio no prueba que los bloqueadores de IL‑6 causaran directamente estos resultados —los médicos pudieron elegirlos para quienes ya estaban en mayor riesgo—, pero refuerza la necesidad de decisiones cuidadosas caso por caso. Al considerar fármacos que bloquean la IL‑6, los clínicos deben sopesar el posible beneficio de frenar una inflamación peligrosa frente a la posibilidad real de favorecer nuevas infecciones, sobre todo en pacientes vulnerables.
Cita: Lefèvre, C., Funck-Brentano, T., Cachanado, M. et al. Benefit and risk associated with interleukin-6 receptor inhibitor administration during severe COVID-19: a retrospective multicentric study. Sci Rep 16, 5978 (2026). https://doi.org/10.1038/s41598-026-36864-w
Palabras clave: COVID-19, inhibidor de la interleucina-6, tocilizumab, infecciones secundarias, cuidados intensivos