Clear Sky Science · es
Farmacocinética, patología y eficacia del inhibidor de la proteasa principal de SARS-CoV-2 VPC285785 en un modelo murino de infección por coronavirus
Por qué seguimos necesitando mejores antivirales orales contra la COVID
Las primeras pastillas antivirales para la COVID-19, como Paxlovid, supusieron un punto de inflexión en la pandemia. Pero no son perfectas: deben tomarse muy pronto, requieren múltiples comprimidos al día y pueden interactuar de forma peligrosa con otros medicamentos. Este estudio explora nuevos candidatos farmacológicos diseñados para bloquear el coronavirus de más de una manera, funcionar bien como comprimidos orales únicos y ocasionar menos problemas de interacciones medicamentosas, usando un modelo murino de infección por coronavirus.
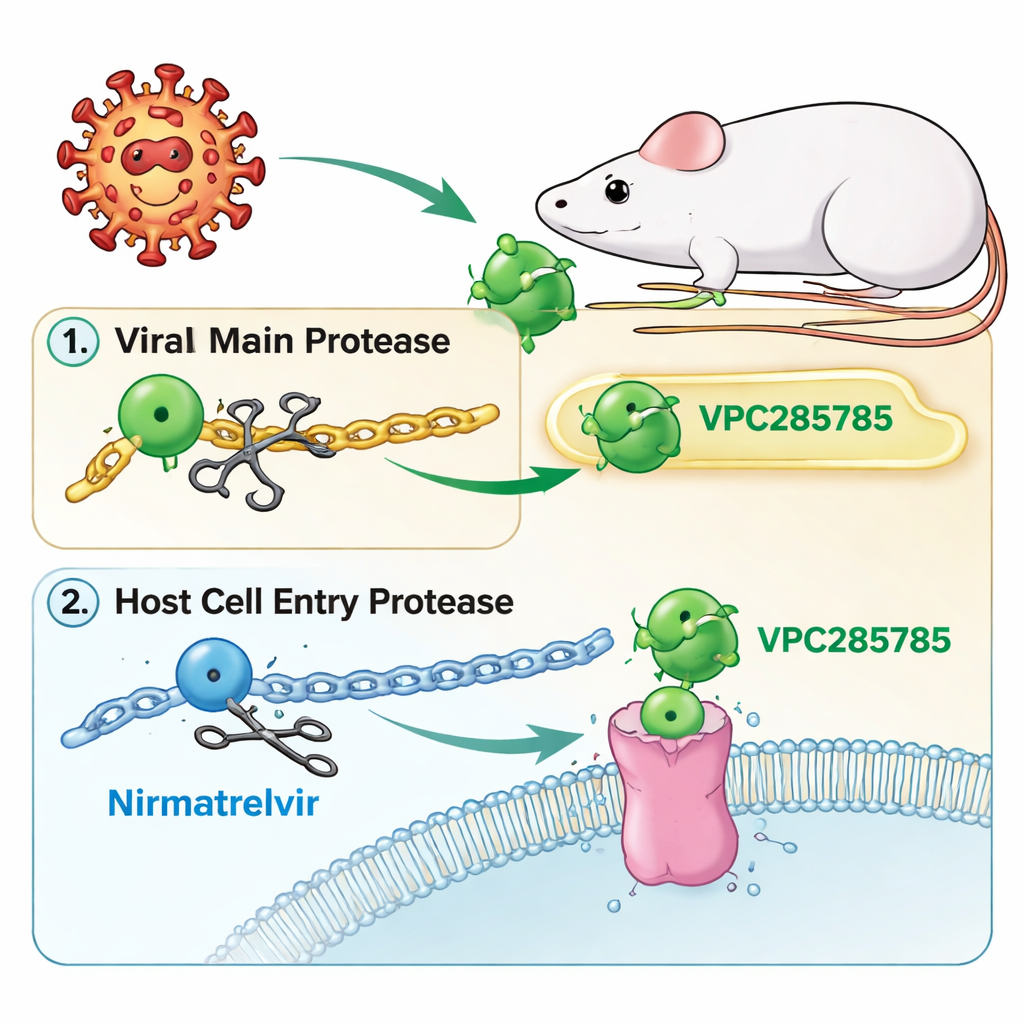
Una nueva variante sobre el blanco proteasa del COVID-19
Al igual que Paxlovid, los nuevos compuestos —llamados VPC285785 y VPC285786— se dirigen a la “proteasa principal” del virus, unas tijeras moleculares que cortan proteínas víricas largas en partes funcionales. Si estas tijeras se bloquean, el virus no puede completarse y se detiene. Los investigadores también diseñaron las moléculas para afectar una segunda proteína de nuestras propias células, la catepsina L, que ayuda a algunos coronavirus a entrar. Al atacar tanto las tijeras víricas como un facilitador de entrada del huésped, el equipo esperó crear una pastilla de acción dual que pudiera ser más difícil de eludir para el virus y que no necesitara un fármaco potenciador.
Diseñadas para durar en el organismo, no para necesitar un potenciador
Paxlovid combina nirmatrelvir con otro fármaco, ritonavir, cuyo papel no es combatir el virus sino ralentizar la degradación del nirmatrelvir en el hígado. Sin embargo, el ritonavir interfiere con muchas enzimas que procesan medicamentos comunes, lo que conlleva interacciones complejas y a veces peligrosas. VPC285785 y VPC285786 se ajustaron químicamente para resistir la degradación por sí mismos, empleando características como átomos de flúor y el “rigidizado” de anillos que los hacen menos atractivos para las enzimas hepáticas. En ensayos de laboratorio con preparaciones hepáticas humanas y murinas, ambos compuestos nuevos demostraron ser al menos tan estables como el nirmatrelvir, y VPC285786 fue en ciertos aspectos incluso más resistente, sin necesidad de ritonavir.
Cómo se comportan y se distribuyen los fármacos en ratones
El equipo examinó luego cómo viajan los compuestos por el organismo de los ratones, midiendo la rapidez con la que desaparecen de la sangre y cuán bien se absorben por vía oral. Tras inyección, VPC285785 y VPC285786 permanecieron en la circulación aproximadamente el mismo tiempo que el nirmatrelvir y alcanzaron una exposición total superior. Sin embargo, administrados por vía oral, sus trayectorias diver gieron: VPC285785 logró una absorción moderada pero viable (alrededor del 15% de la dosis ingerida alcanzando la circulación), mientras que VPC285786 casi no llegó al torrente sanguíneo (alrededor del 3%). Dado que los comprimidos deben cruzar la pared intestinal para ser tratamientos prácticos, solo VPC285785 se continuó en los experimentos de infección.
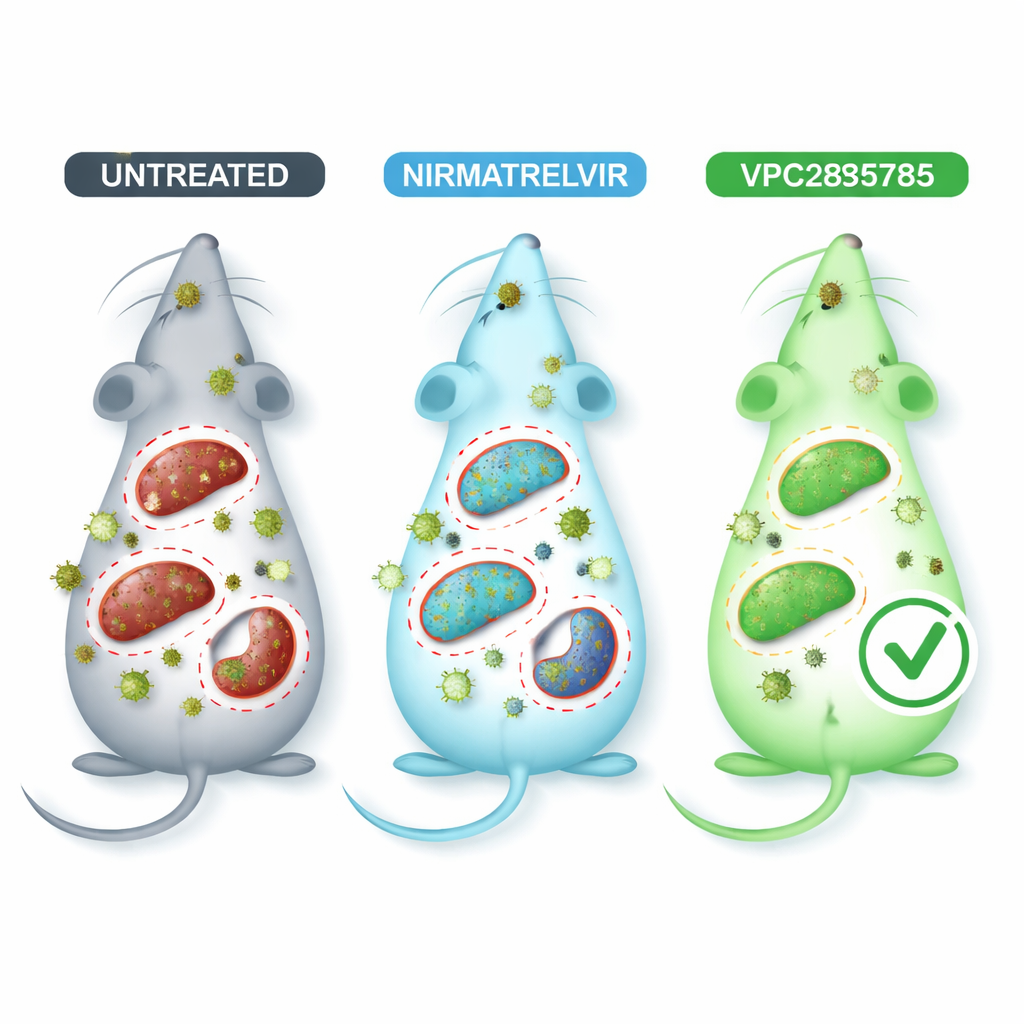
Poner a prueba la nueva pastilla en ratones infectados
Para imitar la enfermedad por coronavirus en un entorno más seguro, los investigadores usaron un coronavirus murino llamado MHV-A59, que invade múltiples órganos y causa daños pulmonares y hepáticos similares en muchos aspectos a la infección humana. Los ratones infectados fueron tratados por vía oral con VPC285785, con nirmatrelvir como comparación, o con un vehículo inactivo. Análisis de sangre mostraron que la infección afectó al hígado y los riñones, pero los animales que recibieron VPC285785 o nirmatrelvir tendieron a presentar marcadores de función hepática y renal más saludables que los ratones no tratados. De forma más llamativa, VPC285785 redujo de forma notable la cantidad de material genético viral en hígado, cerebro y bazo, mientras que nirmatrelvir produjo una disminución clara solo en el cerebro. En pulmón, corazón y riñones, ninguno de los tratamientos mostró una diferencia contundente en las condiciones evaluadas.
Qué podría significar esto para los tratamientos futuros contra la COVID
Aunque VPC285785 es menos potente contra la proteasa vírica en un tubo de ensayo que el nirmatrelvir, funciona bien en animales vivos, reduciendo de forma significativa los niveles de virus en varios órganos clave mientras preserva la función orgánica, todo ello sin un potenciador de ritonavir. Su compuesto hermano, VPC285786, demuestra que es posible un objetivo dual aún más fuerte sobre la proteasa vírica y la catepsina L, pero su mala absorción debe corregirse. En conjunto, estos resultados sugieren que las próximas generaciones de pastillas contra la COVID podrían diseñarse como fármacos orales únicos que ataquen tanto objetivos víricos como del huésped, ofrezcan menos interacciones peligrosas con otros medicamentos y sigan brindando una fuerte protección en tejidos vitales.
Cita: Smith, J.R., Toro, A., Sabater, A. et al. Pharmacokinetics, pathology and efficacy of SARS-CoV-2 main protease inhibitor VPC285785 in a murine model of coronavirus infection. Sci Rep 16, 6905 (2026). https://doi.org/10.1038/s41598-026-36842-2
Palabras clave: antivirales SARS-CoV-2, inhibidores de la proteasa principal, alternativas a Paxlovid, modelo murino de coronavirus, tratamiento oral contra la COVID