Clear Sky Science · es
YTHDC1 modula el fenotipo maligno del retinoblastoma a través de la autofagia mediada por SQSTM1
Por qué esto importa en el cáncer ocular infantil
El retinoblastoma es el cáncer de ojo más frecuente en niños pequeños. Los médicos a menudo pueden curarlo si se detecta pronto, pero una vez que el tumor empieza a invadir los tejidos alrededor del ojo o a propagarse hacia el cerebro, salvar tanto la vida como la visión del niño se vuelve mucho más difícil. Este estudio explora un “freno” molecular dentro de las células tumorales: dos moléculas llamadas YTHDC1 y SQSTM1, que parecen ayudar a mantener el retinoblastoma menos agresivo. Comprender cómo funciona este freno podría abrir nuevas vías para tratamientos más dirigidos y menos invasivos.
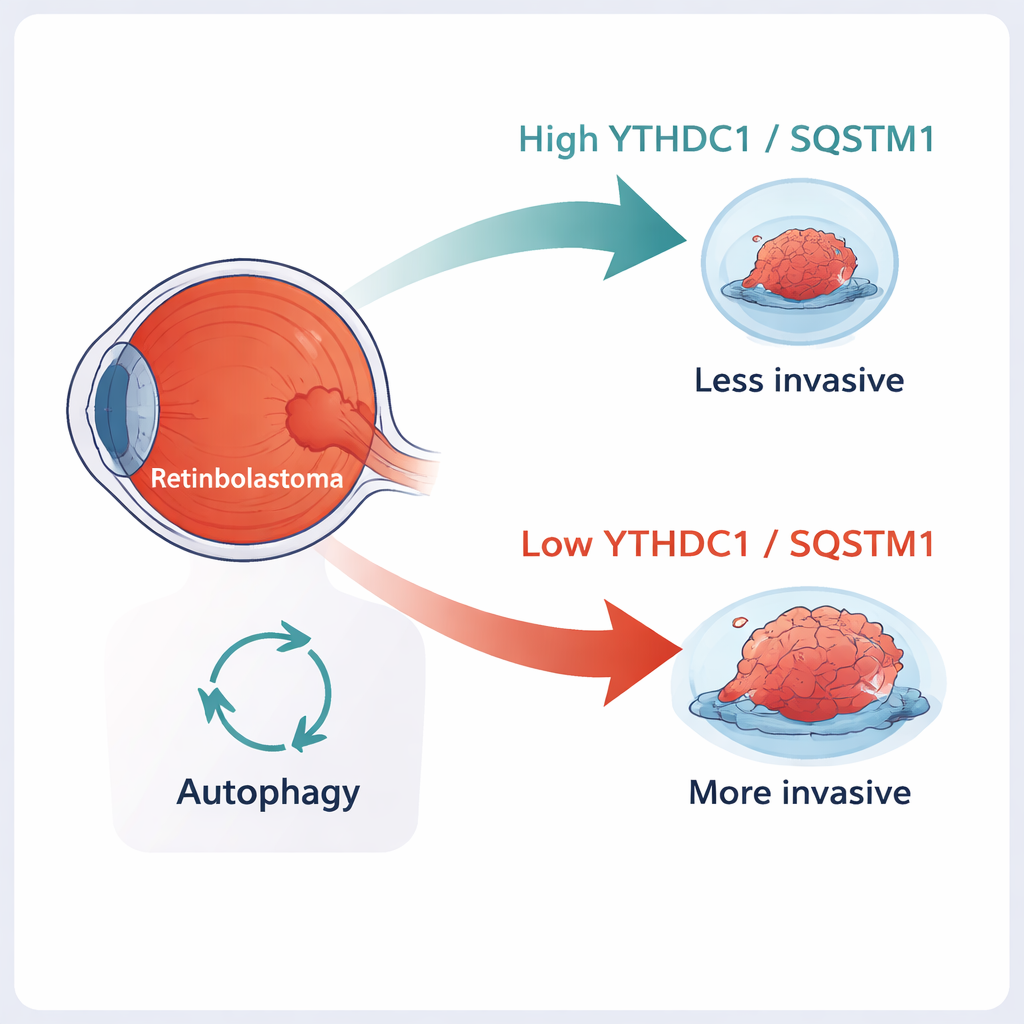
Una mirada más cercana a los tumores oculares infantiles
El retinoblastoma surge de la capa sensible a la luz del ojo, la retina, y suele aparecer en niños menores de cinco años. Clásicamente, la enfermedad comienza cuando se pierden las dos copias de un gen guardián, RB1. Pero la pérdida de RB1 por sí sola no explica por qué algunos tumores permanecen confinados en el ojo mientras que otros se infiltran en tejidos cercanos o se diseminan a lo largo del nervio óptico. Cada vez más, los investigadores reconocen que marcas químicas añadidas al ARN —los mensajes temporales que indican a las células qué proteínas producir— pueden influir fuertemente en el comportamiento del cáncer. Una de las marcas más comunes, llamada m6A, puede alterar la estabilidad de estos mensajes y su duración dentro de la célula.
Descubriendo un freno molecular ausente
Los autores empezaron comparando la actividad genética en tumores que se mantuvieron dentro del ojo con la de tumores ya invasivos. Usando un conjunto público de datos de secuenciación de ARN de muestras de retinoblastoma, identificaron miles de genes cuya actividad difería entre los dos grupos y luego se centraron en los “reguladores” clave de m6A. Estos incluyen enzimas que añaden o eliminan m6A y proteínas “lectoras” que interpretan esa marca. Entre diez reguladores principales, hallaron que una lectora, YTHDC1, estaba consistentemente más baja en los tumores invasivos. Al examinar muestras de 50 niños y realizar pruebas de laboratorio en tejido tumoral, confirmaron que los niveles de YTHDC1 —tanto su ARN como su proteína— estaban reducidos en los cánceres más agresivos.
Poniendo a prueba a YTHDC1
Para ver qué hace realmente YTHDC1, el equipo manipuló sus niveles en dos líneas celulares humanas de retinoblastoma. Cuando disminuyeron YTHDC1 mediante herramientas genéticas, las células se multiplicaron más rápido y fueron mejores para atravesar membranas artificiales que imitan barreras tisulares —signos de un tumor más invasivo. En ratones, las células sin YTHDC1 formaron tumores más grandes y pesados. También ocurrió lo contrario: forzar a las células a producir YTHDC1 adicional frenó su crecimiento y redujo su capacidad de migrar e invadir. Estos experimentos sugieren que YTHDC1 actúa como supresor tumoral, contribuyendo a contener los comportamientos más peligrosos del retinoblastoma.
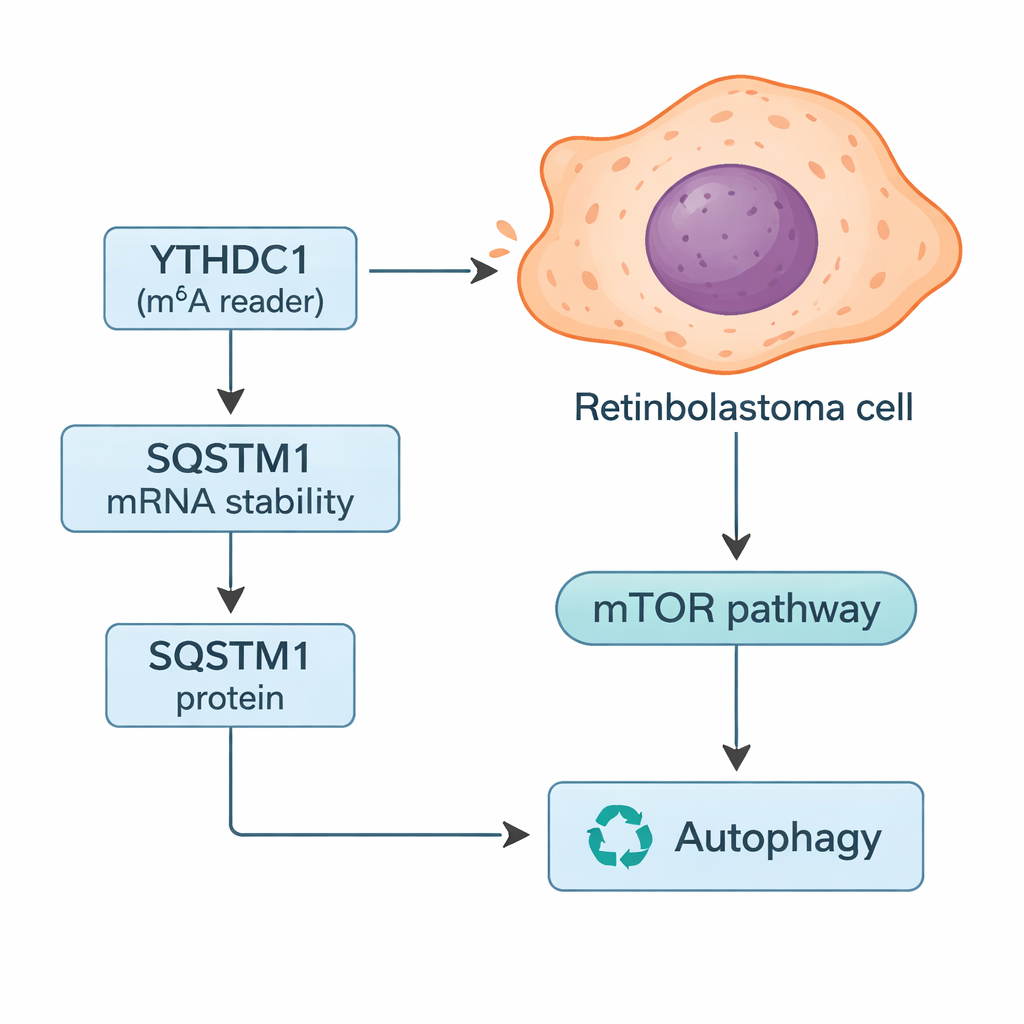
Cómo YTHDC1 controla el sistema de reciclaje celular
Profundizando, los investigadores buscaron genes específicos cuyos mensajes pudieran estar controlados por YTHDC1. Combinando búsquedas en bases de datos con sus datos tumorales, se centraron en SQSTM1, una proteína más conocida como p62. SQSTM1 participa en la gestión de la autofagia, el sistema de reciclaje celular que degrada componentes dañados y puede proporcionar energía cuando los recursos escasean. El estudio mostró que YTHDC1 se une físicamente al ARN de SQSTM1 y lo estabiliza, permitiendo que se produzca más proteína SQSTM1. Cuando YTHDC1 se reducía, los niveles de SQSTM1 bajaban y su ARN se degradaba con mayor rapidez. Silenciar SQSTM1 por sí solo hizo que las células de retinoblastoma crecieran e invadieran más, y borró en parte los efectos protectores observados al sobreexpresar YTHDC1, situando a SQSTM1 como un intermediario clave en esta vía.
Autofagia, energía y agresividad tumoral
Dado que SQSTM1 es central para la autofagia, el equipo evaluó cómo alterar YTHDC1 y SQSTM1 afectaba este proceso de reciclaje. Usando una combinación de marcadores fluorescentes y mediciones de proteínas, encontraron que reducir YTHDC1 o SQSTM1 aumentaba el “flujo” autófago: más material celular se dirigía hacia y a través del sistema de reciclaje. También observaron cambios en la vía mTOR, un interruptor principal que detecta nutrientes y normalmente mantiene la autofagia bajo control. Con menos SQSTM1, la actividad de mTOR disminuyó, lo cual es consistente con una activación de la autofagia. En el retinoblastoma invasivo, los autores proponen que la reducción de YTHDC1 conduce a señales más débiles de SQSTM1, una actividad mTOR atenuada y una autofagia intensificada que ayuda a las células tumorales a sobrevivir el estrés y a diseminarse.
Qué implica esto para tratamientos futuros
Para un público no especializado, el mensaje principal es que este estudio identifica una cadena de eventos dentro de las células de retinoblastoma —YTHDC1 controlando a SQSTM1, que a su vez modula el sistema de reciclaje celular— que influye en cuán agresivo se vuelve el cáncer. Cuando esta cadena se debilita, los tumores crecen más rápido y son más invasivos. Aunque queda mucho trabajo antes de que estos hallazgos puedan llegar a la clínica, la vía ofrece nuevas ideas terapéuticas: restaurar la función de YTHDC1, estabilizar SQSTM1 o ajustar la autofagia y la actividad de mTOR podrían algún día complementar las quimioterapias existentes. Para los niños afectados por este cáncer ocular, tales estrategias dirigidas podrían ayudar a limitar la diseminación tumoral, preservar más visión y reducir los efectos secundarios del tratamiento.
Cita: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
Palabras clave: retinoblastoma, YTHDC1, SQSTM1, autofagia, vía mTOR