Clear Sky Science · es
Impacto neurotoxicogenómico del 4‑nonilfenol en Heteropneustes fossilis mediante análisis molecular, histopatológico y bioinformático
Por qué esta historia de peces te importa
Muchos productos cotidianos —desde detergentes hasta plásticos— dejan tras de sí un químico llamado 4‑nonilfenol (4‑NP) que acaba en ríos y estanques. Este estudio exploró qué le ocurre al cerebro de un pez de consumo común, el pez gato picador Heteropneustes fossilis, cuando vive en agua contaminada con niveles realistas de 4‑NP. Dado que estos contaminantes se transfieren por la cadena trófica y algunos pueden afectar el cerebro y las hormonas humanas, entender su impacto en los peces ofrece una alerta temprana sobre riesgos ambientales y de salud pública más amplios.
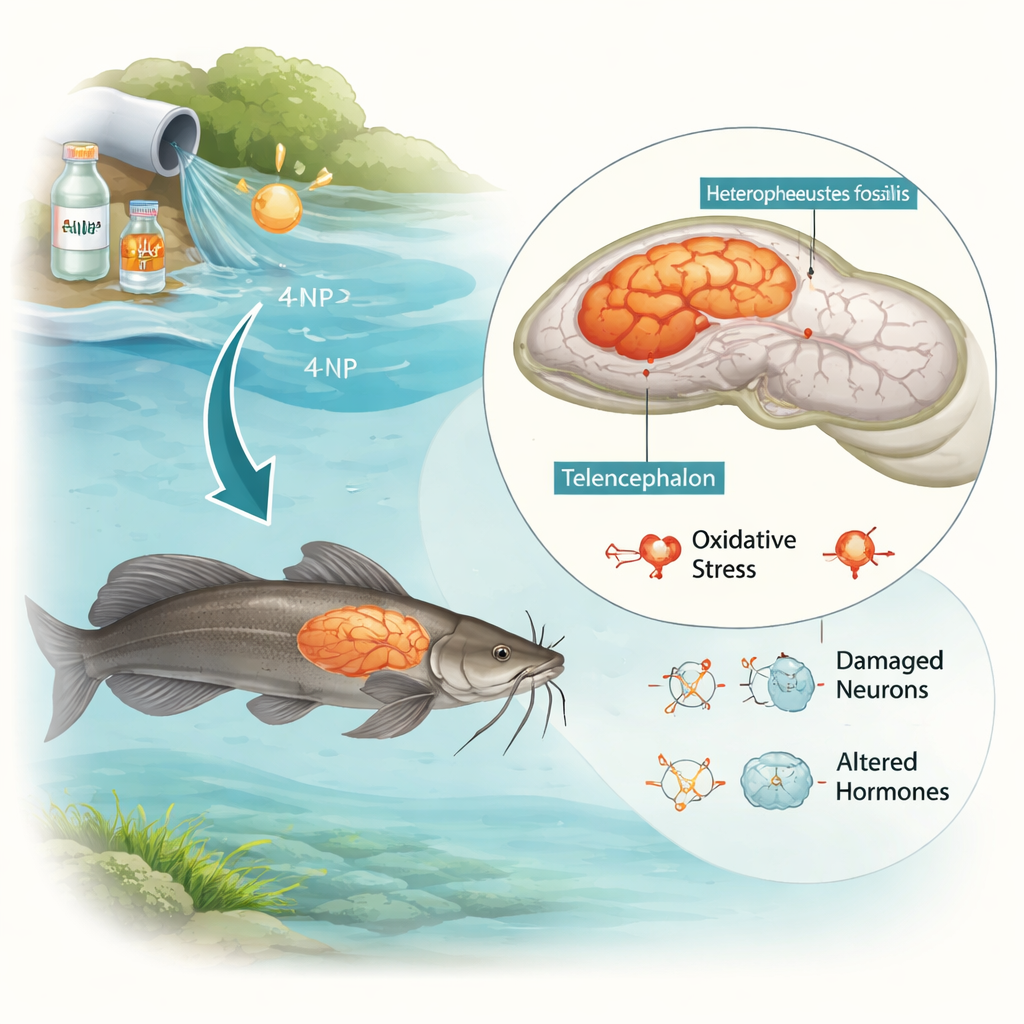
Un contaminante común con un efecto oculto
El 4‑NP es un producto de degradación de tensioactivos industriales usados en limpiadores, plásticos y otros productos. Es oleoso, se degrada lentamente y se acumula en los tejidos vivos. Trabajos previos mostraron que se acumula especialmente en los cerebros de los peces gato. Los investigadores expusieron machos de esta especie a concentraciones bajas y altas de 4‑NP, similares a las encontradas en aguas contaminadas, durante 30 o 60 días abarcando su temporada reproductiva. Luego examinaron los cerebros mediante microscopía, pruebas bioquímicas, análisis de expresión génica y modelado por ordenador para ver si el 4‑NP podía cruzar al cerebro, alterar la química cerebral e interferir con la reproducción.
Daño en regiones cerebrales clave
El examen microscópico reveló que el 4‑NP daña físicamente el cerebro del pez gato. En el telencéfalo, que ayuda a controlar el olfato, el aprendizaje y aspectos del comportamiento, las neuronas normales observadas en los controles fueron reemplazadas por células difusas y degeneradas, espacios vacíos (vacuolas), pequeñas hemorragias y células inflamatorias. El cerebelo, importante para el movimiento y el equilibrio, también mostró separación entre sus capas, vacuolización del tejido circundante y neuronas necróticas (muertas), especialmente a dosis más altas y con exposiciones prolongadas. Estas lesiones estructurales sugieren que los peces expuestos probablemente sufran deterioro en la natación, la navegación y posiblemente cambios en el comportamiento reproductivo.
Estrés oxidativo, hormonas de estrés y muerte celular
Dentro del tejido cerebral dañado, el equilibrio químico cambió en una dirección peligrosa. El 4‑NP redujo la actividad de enzimas antioxidantes clave que normalmente neutralizan las especies reactivas de oxígeno (ROS). Al mismo tiempo, los marcadores de peroxidación lipídica —cicatrices químicas dejadas cuando las ROS atacan las membranas grasas— aumentaron con la dosis y el tiempo de exposición. La capacidad antioxidante total disminuyó, mientras que el estado oxidante total aumentó. Los niveles cerebrales de la hormona del estrés, el cortisol, también se incrementaron, particularmente al inicio de la exposición, indicando una fuerte respuesta al estrés. Ensayos por citometría de flujo mostraron que tras 30 días, más células cerebrales morían por necrosis (muerte celular no controlada), mientras que tras 60 días la apoptosis (muerte celular programada) se volvió más prominente. Ensayos tipo “cometa” del ADN confirmaron que las hebras de material genético se fragmentaban cada vez más a dosis mayores y con exposiciones más largas.
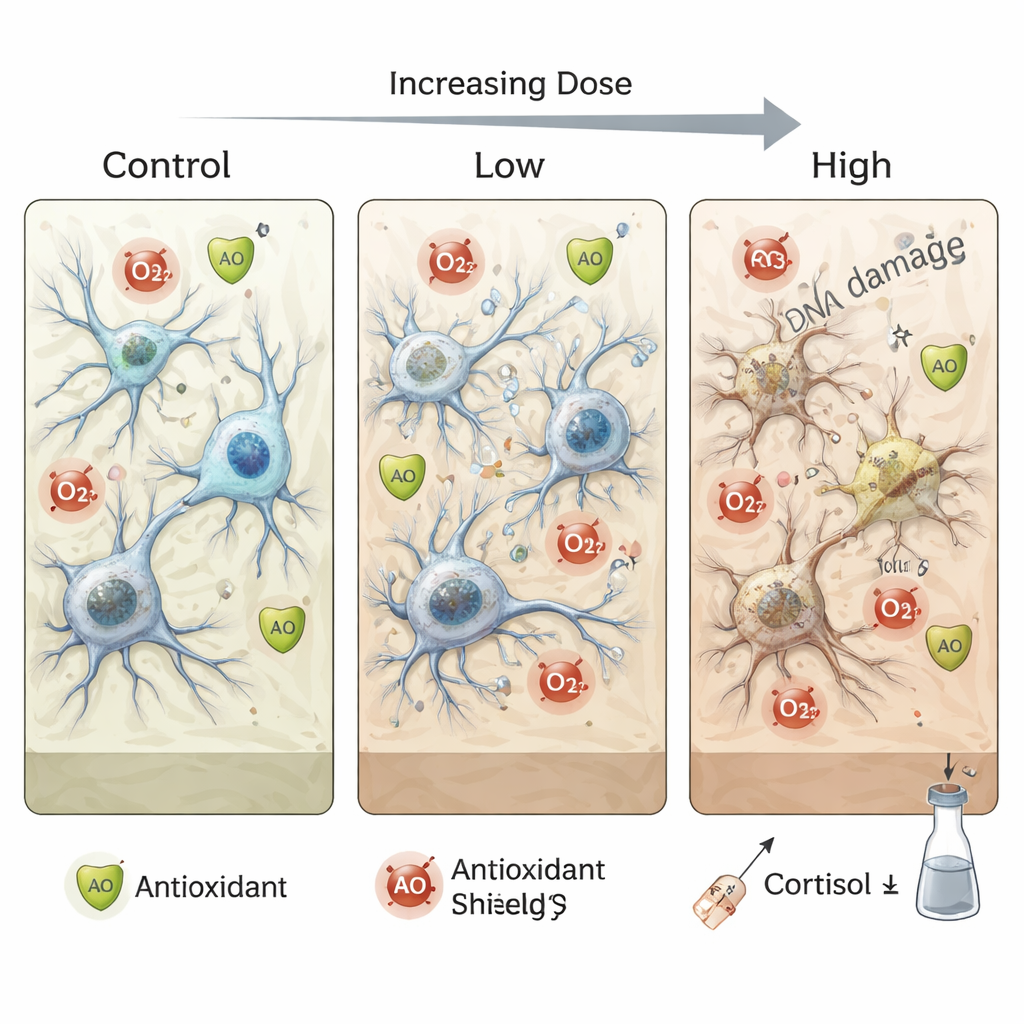
Química cerebral alterada y señales reproductivas interrumpidas
Más allá del daño físico, el 4‑NP alteró moléculas clave que mantienen la señalización cerebral y la reproducción. La actividad de la acetilcolinesterasa, una enzima que elimina el neurotransmisor acetilcolina, descendió de forma dependiente de la dosis y del tiempo, lo que puede perturbar la comunicación nerviosa y el comportamiento. Los investigadores también midieron genes cerebrales que controlan la reproducción: la hormona liberadora de gonadotropina (GnRH) y la aromatasa cerebral (Cyp19a1b), la enzima que convierte andrógenos en estrógenos. Ambos genes se vieron fuertemente reprimidos por el 4‑NP. Esto significa que el contaminante no solo lesiona las células cerebrales, sino que también debilita las señales hormonales que desencadenan el desove, amenazando la fertilidad y la salud poblacional de los peces.
Los ordenadores confirman un blanco cerebral directo
Para entender cómo el 4‑NP alcanza y afecta el cerebro, el equipo usó herramientas bioinformáticas. Simulaciones con SwissADME predijeron que el 4‑NP se absorbe bien desde el intestino, puede cruzar la barrera hematoencefálica y posee propiedades similares a pequeñas moléculas tipo fármaco. Estudios de acoplamiento y simulaciones de dinámica molecular a largo plazo mostraron que el 4‑NP encaja de forma ajustada en el bolsillo activo de la acetilcolinesterasa, formando interacciones estables con varios aminoácidos. Las energías de unión calculadas indicaron que esta asociación es lo bastante fuerte como para inhibir la enzima, en consonancia con la reducción de la actividad de la acetilcolinesterasa observada en tejido cerebral real. El mismo modelado también sugirió que el 4‑NP puede interferir con enzimas hepáticas que normalmente detoxicifican compuestos extraños, amplificando aún más sus efectos tóxicos.
Qué significa esto para los peces y para nosotros
En conjunto, los resultados dibujan un panorama claro: incluso a niveles subletales, el 4‑nonilfenol llega al cerebro de machos de pez gato, donde debilita las defensas antioxidantes, aumenta el estrés oxidativo y hormonal, daña el ADN, mata neuronas y silencia genes esenciales para la reproducción. Estos cambios amenazan la salud y el éxito reproductivo de los peces que viven en aguas contaminadas y ponen de relieve cómo un químico industrial de uso generalizado puede actuar como un neurotóxico sigiloso. Dado que el 4‑NP persiste en el medio ambiente y se bioacumula en la cadena trófica, limitar su liberación y vigilar sus niveles en los ecosistemas acuáticos son pasos importantes para proteger tanto la vida silvestre como a las personas que dependen de ella.
Cita: Suman, Agrawal, S., Mishra, R. et al. Neurotoxicogenomic impact of 4-nonylphenol on Heteropneustes fossilis via molecular, histopathological and bioinformatic analysis. Sci Rep 16, 5974 (2026). https://doi.org/10.1038/s41598-026-36820-8
Palabras clave: contaminación acuática, neurotoxicidad, disruptores endocrinos, estrés oxidativo, nonilfenol