Clear Sky Science · es
Caracterización experimental de la administración de terapia con minihaz de protones bajo condiciones de tasa de dosis FLASH
Rayos más rápidos y menos agresivos
La radioterapia es un pilar del tratamiento del cáncer, pero puede dañar el tejido sano además de los tumores. Este estudio explora una nueva forma de administrar radiación de protones que pretende golpear con fuerza a los tumores al tiempo que reduce el impacto en los órganos normales. Al combinar dos ideas emergentes —minihaz muy finos y tasas de dosis ultrarrápidas tipo FLASH— los investigadores demuestran que es técnicamente posible aplicar tratamientos muy precisos en apenas unos segundos usando equipos similares a los que ya existen en hospitales modernos.
¿Por qué convertir la radiación en haces diminutos?
Los campos de radiación tradicionales parecen homogéneos: la dosis se distribuye de forma relativamente uniforme en la región tratada. La radioterapia fraccionada espacialmente rompe esa regla a propósito. En la terapia con minihaz de protones, la radiación se divide en muchos haces delgados, submilimétricos, separados por huecos. Cerca de la superficie, esto crea un patrón de “picos” de alta dosis y “valles” de baja dosis. El tejido sano entre los picos tiene más posibilidades de repararse, mientras que más profundo en el cuerpo los haces se dispersan y solapan, proporcionando al tumor una dosis más uniforme y efectiva. Estudios iniciales en laboratorio y en animales sugieren que este patrón puede reducir los efectos secundarios e incluso provocar respuestas inmunitarias beneficiosas contra el cáncer.
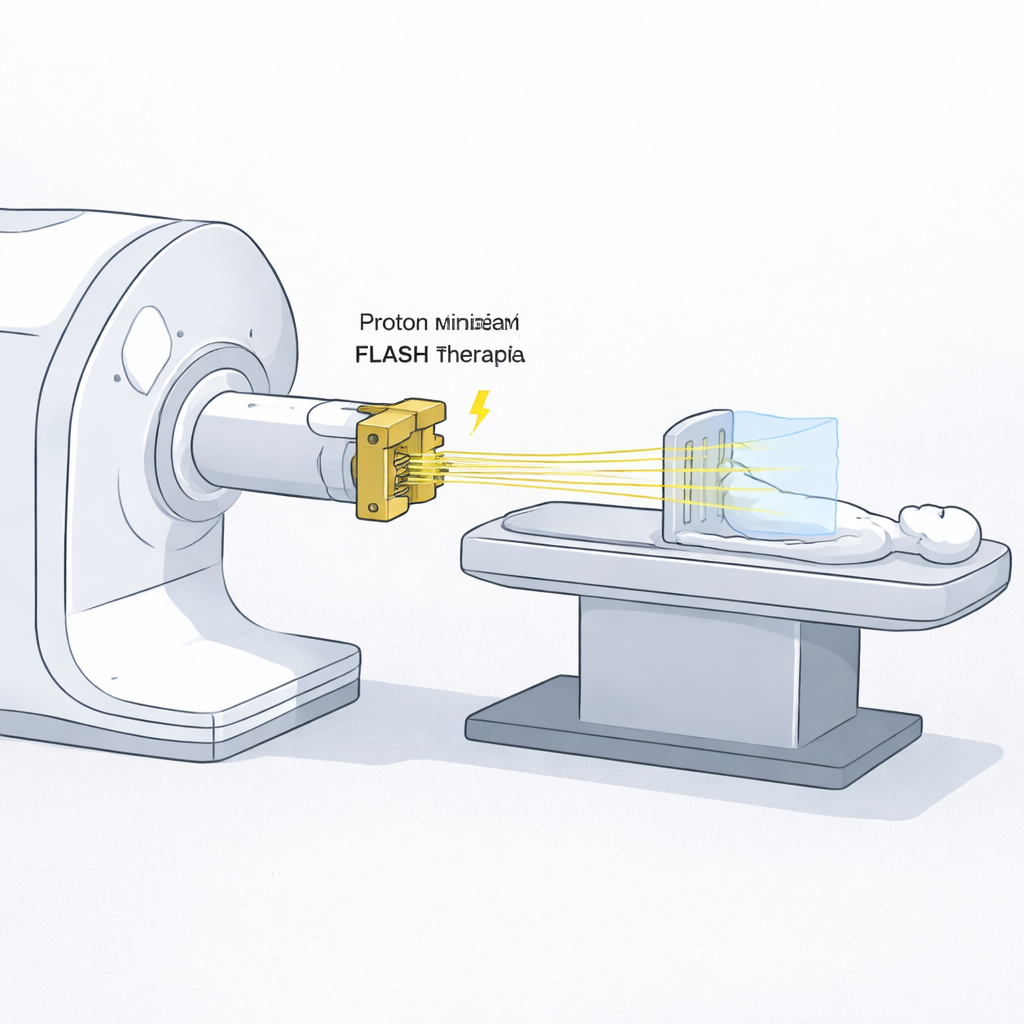
¿Qué es FLASH y por qué importa la velocidad?
La terapia FLASH es una nueva forma de considerar el tiempo en la administración de radiación. En lugar de administrar una dosis lentamente durante decenas de segundos o minutos, FLASH entrega la misma dosis en una fracción de segundo a tasas de dosis ultraltas—decenas a cientos de gray por segundo. Sorprendentemente, muchos experimentos han mostrado que los tejidos normales pueden conservarse mejor bajo estas condiciones extremas, mientras que los tumores siguen siendo igual de vulnerables. Para las minihaz de protones, sin embargo, existía un obstáculo práctico: los bloques metálicos de varias ranuras usados para dividir el haz en rayos finos desperdician gran parte de las partículas entrantes, por lo que los tratamientos pueden durar varios minutos. Si las minihaz pudieran administrarse en modo FLASH, el tiempo perdido podría recuperarse y los beneficios biológicos de ambos métodos podrían combinarse.
Implementando minihaz y FLASH en una máquina clínica
El equipo trabajó con un sistema clínico compacto de protones que normalmente trata a los pacientes con un haz de protones de escaneo suave. Acoplaron colimadores personalizados de latón con múltiples ranuras—cada uno con cinco ranuras estrechas de solo 1 milímetro de ancho y separadas 2,8 milímetros—al extremo de la boquilla de tratamiento. Aumentando la corriente del haz y ajustando cuidadosamente la óptica del haz, operaron el sistema en un modo de tasa de dosis ultralta a 228 MeV, manteniendo la capacidad de volver a la configuración clínica habitual. Luego midieron cómo se distribuía la dosis en bloques plásticos de tipo acuoso usando películas radiosensibles especiales y compararon esas mediciones con simulaciones por ordenador detalladas que siguen las interacciones individuales de los protones.
¿Qué tan bien funcionó el nuevo haz?
Bajo condiciones FLASH, el haz de protones mantuvo un patrón claro de minihaz: picos nítidos a lo largo de las ranuras y valles profundos entre ellas. Las mediciones y las simulaciones coincidieron estrechamente en cómo evolucionaba este patrón con la profundidad y en la rapidez con que se difuminaba a medida que los haces se dispersaban. Un colimador más grueso de 10 cm produjo una separación más limpia entre picos y valles que una versión de 6,5 cm, especialmente cerca de la superficie, lo que significa que protegía mejor las regiones de “valle”. De manera crucial, operar la máquina en modo FLASH redujo el tiempo de administración de un campo de minihaz típico de 3 por 3 centímetros de unos 3 minutos a apenas 2,5 segundos. Cálculos basados en los registros temporales de la máquina mostraron que las tasas de dosis locales en las regiones de pico superaron fácilmente los umbrales de FLASH comúnmente utilizados, todo esto preservando la fina estructura espacial de las minihaz.
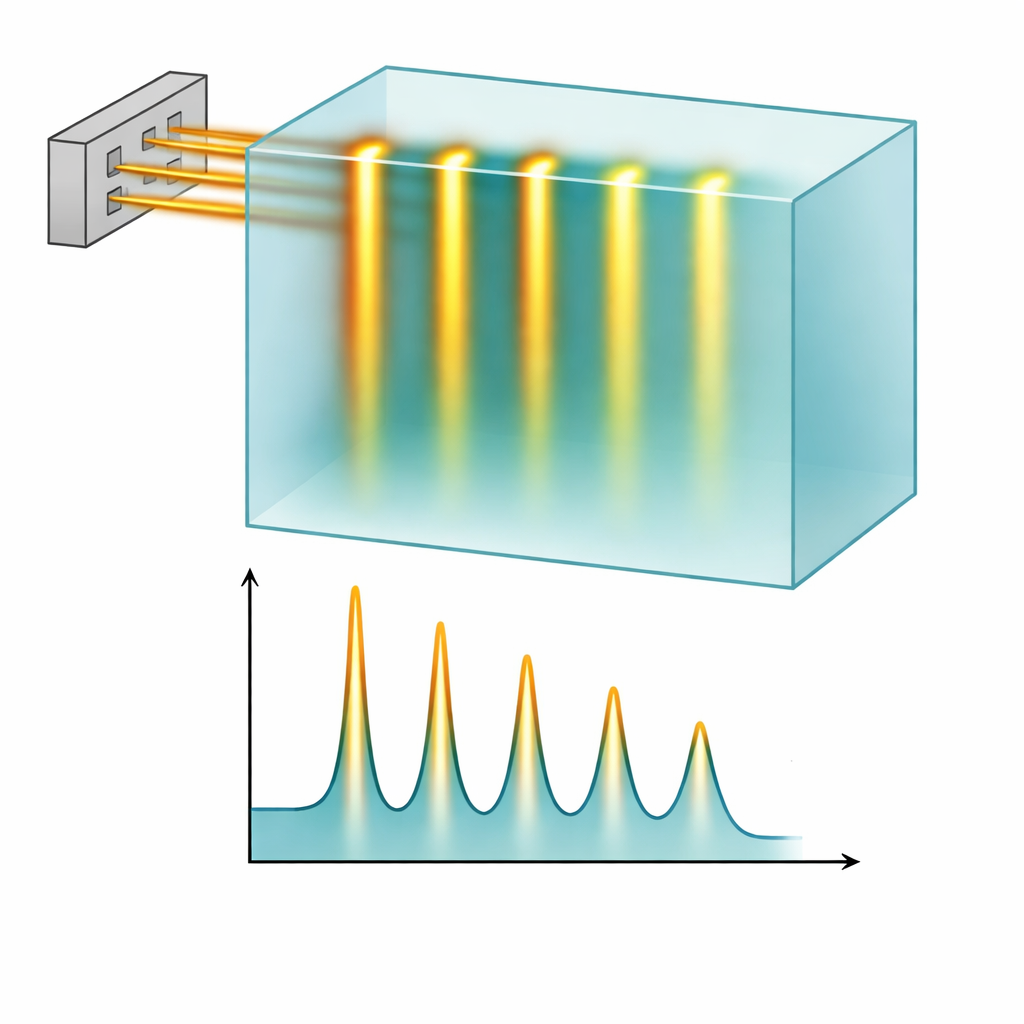
Qué podría significar esto para la atención del cáncer en el futuro
Este trabajo es una prueba de concepto temprana pero importante. Muestra que un sistema clínico estándar de terapia con protones puede adaptarse para entregar minihaz de protones a tasas de dosis FLASH sin sacrificar la precisión ni la calidad del haz. Aún no se trata a pacientes de esta manera: los experimentos se realizaron en montajes de prueba, y se utilizó un único haz de alta energía en lugar de los patrones de energía escalonada que requieren los tumores reales. Además, los efectos biológicos de combinar patrones espaciales de minihaz con la administración ultrarrápida tipo FLASH siguen por demostrarse en animales y, eventualmente, en humanos. Aun así, el estudio sienta las bases técnicas para futuros tratamientos que podrían controlar los tumores tan eficazmente como los mejores métodos actuales mientras reducen drásticamente el daño a los órganos sanos aprovechando tanto dónde como con qué rapidez se administra la radiación.
Cita: Lin, Y., Wu, W., Setianegara, J. et al. Experimental characterization of proton minibeam therapy delivery under FLASH dose-rate conditions. Sci Rep 16, 7803 (2026). https://doi.org/10.1038/s41598-026-36739-0
Palabras clave: terapia con protones, radioterapia FLASH, radiación con minihaz, tratamiento del cáncer, tasa de dosis de radiación