Clear Sky Science · es
Sistema de defensa frente a fagos tipo RexAB codificado por profagos en Pseudomonas putida
Guardianes ocultos que viven dentro de las bacterias
Las bacterias son objeto de caza constante por virus llamados fagos, que pueden arrasar poblaciones microbianas enteras. Este estudio examina cómo los virus “dormidos” ocultos en el ADN de una bacteria pueden actuar en secreto como guardianes, sacrificando las células infectadas para salvar al resto. Comprender estos trucos defensivos naturales es relevante para las terapias con fagos, la biotecnología y también para mantener la fiabilidad de cultivos microbianos industriales.
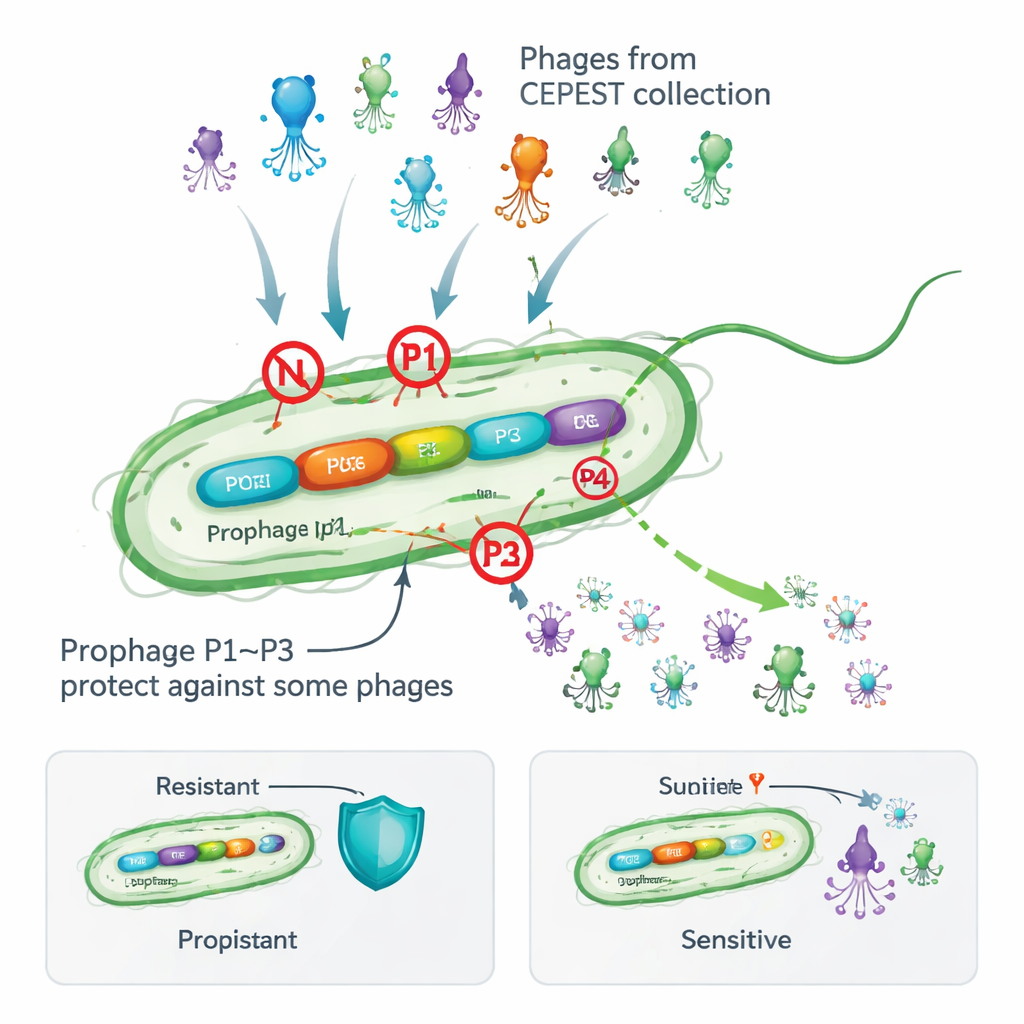
Virus que se convierten de enemigos en aliados
Muchas bacterias albergan fagos temperados en una forma latente llamada profago, integrados en sus cromosomas. A primera vista esto parece arriesgado: estos pasajeros víricos pueden despertarse y dañar la célula huésped, además de aumentar el tamaño del genoma. Sin embargo, muestreos de miles de genomas bacterianos muestran que la mayoría de las especies conservan profagos, lo que sugiere que aportan ventajas. Trabajos previos con la bacteria del suelo Pseudomonas putida mostraron que eliminar sus cuatro profagos crípticos (no productivos) hacía a las células más vulnerables al ataque por una colección experimental de fagos llamada CEPEST. Esto apuntaba a que los profagos portaban armas anti‑fago, pero los genes y mecanismos exactos eran desconocidos.
Tres virus residentes ofrecen protección dirigida
Los autores diseccionaron la contribución de cada profago eliminándolos uno por uno y probando cómo de bien 26 fagos diferentes de CEPEST podían formar placas sobre monocapas bacterianas. Encontraron que los profagos denominados P1, P2 y P3 proporcionan protección, pero solo frente a grupos particulares de fagos, mientras que P4 parece neutro. P1 por sí solo puede reducir la infección por algunos fagos aproximadamente mil veces, P2 ofrece una protección más modesta y P3 es espectacularmente eficaz —pero solo contra ciertos fagos gigantes “jumbo”. En la mayoría de los casos, un único profago explica el patrón de resistencia observado, aunque para algunos fagos varios profagos parecen cooperar. Estos resultados muestran que incluso profagos “silenciosos” pueden actuar como un escudo personalizado afinado a amenazas víricas específicas.
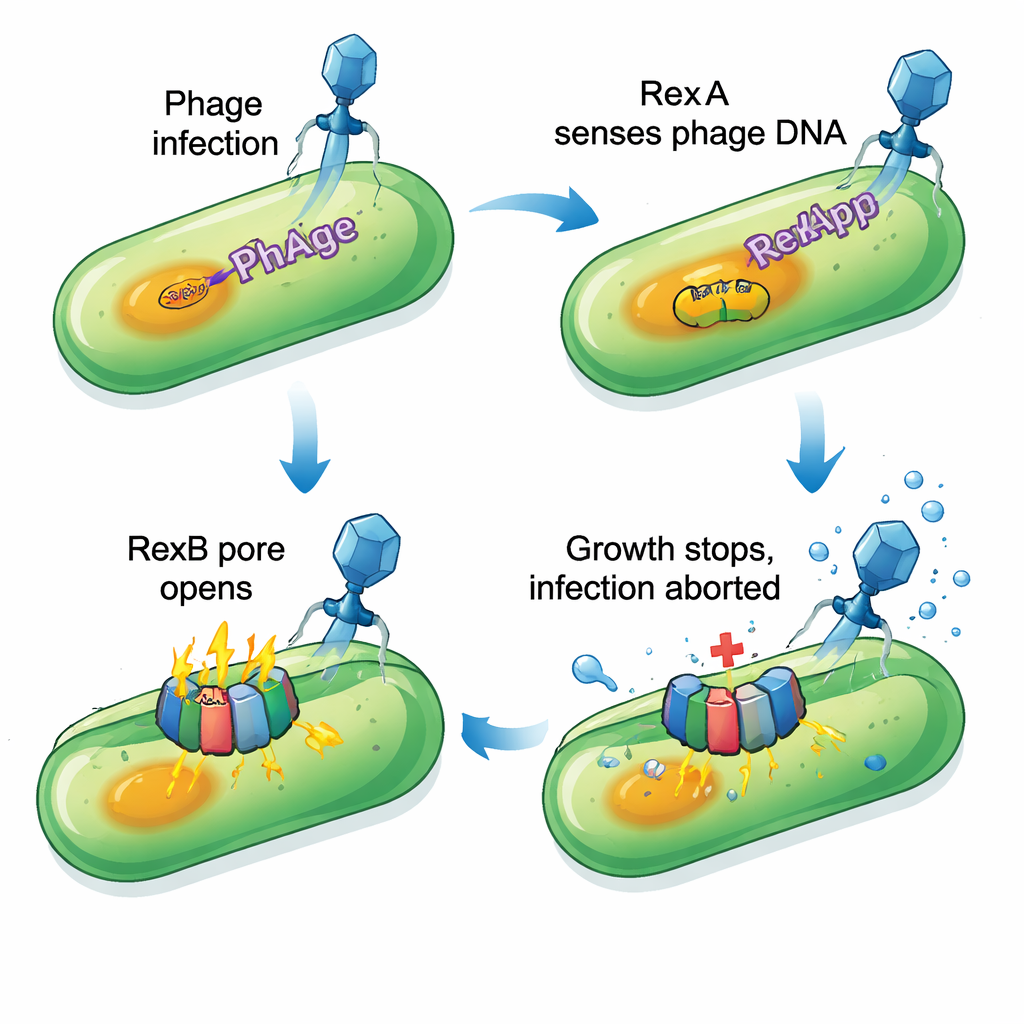
Rastreando una alarma molecular de dos piezas
Centrados en la protección fuerte y relativamente amplia proporcionada por P1, el equipo eliminó sistemáticamente bloques de genes de P1 hasta que la defensa desapareció. Acotando la búsqueda, descubrieron que perder solo dos genes vecinos, PP_5643 y PP_5644, hacía a las células tan sensibles como si todo el profago P1 hubiera sido eliminado. Herramientas bioinformáticas revelaron que PP_5643 se parece a RexA, una proteína fijadora de ADN de estudios clásicos del fago lambda, mientras que PP_5644 parece una proteína de membrana con varias hélices que podría formar un poro, similar a RexB. Juntos, este par coincide con un tipo bien conocido de sistema de “infección abortiva”: una vez detectado un fago específico, la célula infectada detiene deliberadamente su propio crecimiento para que el virus no pueda multiplicarse ni propagarse a los vecinos.
Cómo la defensa sabotea a las células infectadas
Los experimentos confirmaron que la versión de RexA de P1 (llamada RexApp) se une al ADN sin mostrar gran preferencia por secuencias concretas, lo que la hace idónea para detectar estructuras de ADN inusuales generadas durante la replicación vírica. La proteína compañera RexBpp se inserta en la membrana celular. Cuando RexApp se sobreproduce artificialmente, las células que todavía llevan el gen rexBpp muestran una detención severa del crecimiento y signos de daño en la membrana: tintes que normalmente no atraviesan membranas intactas entran de repente, y pequeñas cantidades de una enzima citoplasmática se filtran al exterior. Si rexBpp falta o está mutado, la sobreproducción de RexApp deja de dañar las células. Esto indica que RexApp actúa como disparador, mientras que RexBpp es el efector que daña el envoltorio celular. De forma interesante, la mayoría de las células afectadas no estallan por completo; en su lugar entran en un estado profundamente ralentizado, casi estacionario, que parece incompatible con la multiplicación del fago.
Por qué renunciar a unas pocas células puede salvar a la población
El panorama que emerge es el de una defensa altruista: cuando un fago sensible infecta a P. putida, RexApp probablemente detecta complejos ADN‑proteína víricos y activa RexBpp, que compromete la membrana y detiene abruptamente el crecimiento. La célula infectada paga el precio, pero el ciclo de vida del fago se aborta y la comunidad bacteriana más amplia queda protegida. Sistemas de este tipo RexAB se han encontrado ahora en solo unas pocas familias de fagos, pero comparten la misma lógica central: un sensor intracelular conectado a un efector de membrana que puede convertir rápidamente una célula productiva en un callejón sin salida para el virus. Para las bacterias, conservar profagos crípticos que portan módulos defensivos así puede compensar los costes de albergar ADN vírico, ayudándolas a sobrevivir en un mundo donde los fagos están por todas partes.
Cita: Rosendahl, S., Kängsep, A., Ainelo, A. et al. Prophage-encoded RexAB-type phage defense system in Pseudomonas putida. Sci Rep 16, 5898 (2026). https://doi.org/10.1038/s41598-026-36734-5
Palabras clave: defensa frente a bacteriófagos, profago, Pseudomonas putida, infección abortiva, sistema RexAB