Clear Sky Science · es
Desarrollo y validación de un modelo murino de cáncer de mama triple negativo PSMA-positivo para terapias radionúclidas dirigidas preclínicas
Por qué importa esta investigación
El cáncer de mama triple negativo es una de las formas más difíciles de tratar. Suele diseminarse con rapidez, ofrece a los pacientes menos opciones de tratamientos dirigidos y con frecuencia reaparece tras las terapias estándar. Al mismo tiempo, una nueva clase de fármacos radiactivos “inteligentes” que se fijan a una molécula específica llamada PSMA ha transformado el tratamiento del cáncer de próstata avanzado. Este estudio plantea una pregunta simple pero potente: ¿podemos construir un modelo de laboratorio realista de cáncer de mama triple negativo que presente el mismo objetivo PSMA, para poder evaluar de forma rigurosa si estos fármacos radiactivos también podrían ayudar a pacientes con este cáncer de mama agresivo?
Del objetivo prostático al reto del cáncer de mama
PSMA, siglas de antígeno de membrana específico de próstata, es una pequeña estructura en la superficie de ciertas células. Es abundante en muchos cánceres de próstata y puede ser reconocida por fármacos radiactivos que tanto revelan tumores en exploraciones como entregan radiación directamente a ellos. Recientemente, los investigadores han descubierto que PSMA también aparece, en distintos grados, en los vasos sanguíneos y células de varios otros cánceres, incluido el cáncer de mama triple negativo. Sin embargo, en estos tumores no prostáticos PSMA tiende a ser parcheado y más débil, lo que dificulta saber si las terapias dirigidas a PSMA funcionarán. Antes de probar nuevos tratamientos en pacientes, los científicos necesitan modelos animales que reproduzcan fielmente este patrón de PSMA en tumores mamarios—algo que ha resultado sorprendentemente difícil de lograr.
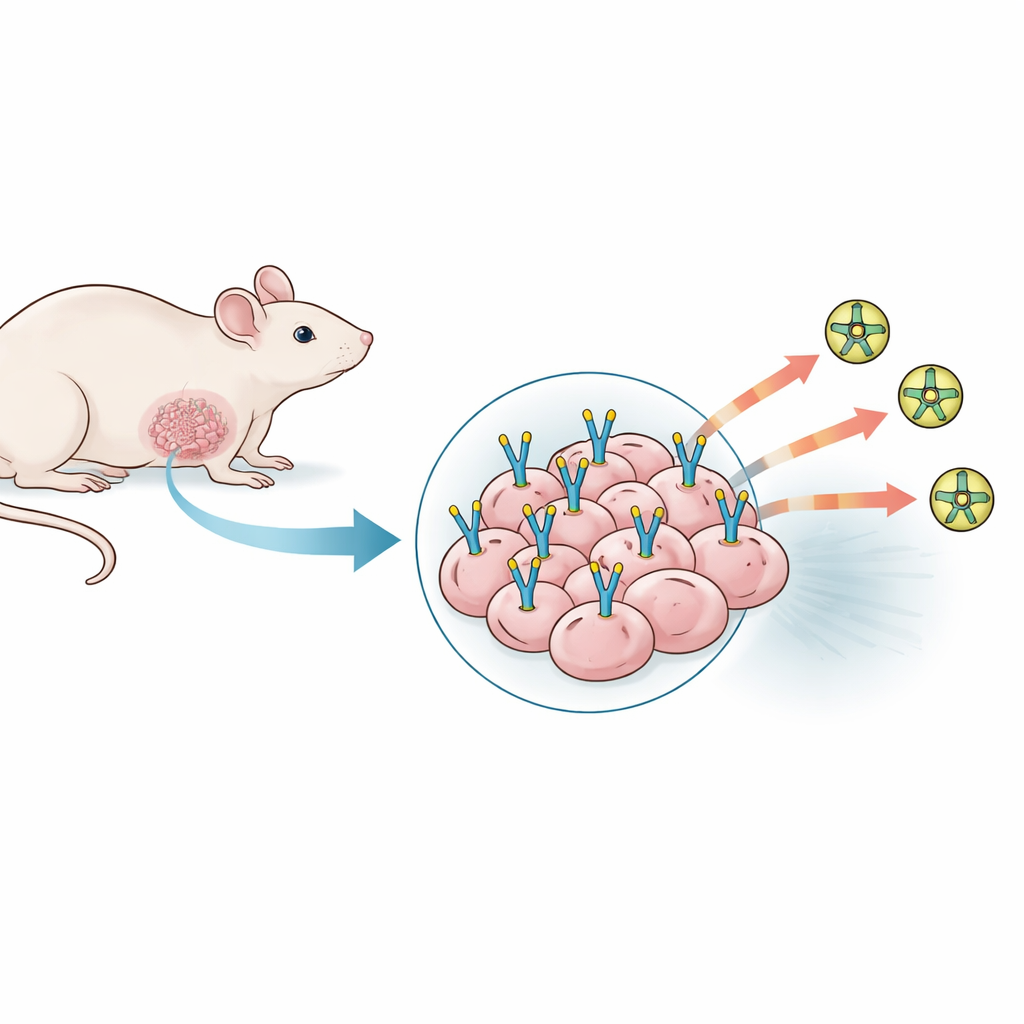
Probando muchos modelos tumorales que se negaron a cooperar
El equipo exploró primero una amplia gama de modelos murinos existentes de cáncer de mama triple negativo, usando líneas celulares cancerosas tanto de ratón como humanas implantadas en diferentes localizaciones y bajo distintas condiciones. Variaron el número de células inyectadas, añadieron geles de soporte para promover el crecimiento de vasos sanguíneos e incluso mezclaron células endoteliales humanas con la esperanza de aumentar los niveles de PSMA. Para cada modelo midieron con qué fiabilidad los tumores se establecían y crecían, inspeccionaron cortes tumorales al microscopio y usaron un trazador PET buscador de PSMA para ver si los tumores se iluminaban en exploraciones corporales completas. A pesar de un crecimiento tumoral robusto y redes vasculares abundantes, ninguno de estos 23 modelos mostró una presencia significativa de PSMA, ni en la tinción tisular ni en la imagen PET. Los tumores parecían activos y bien irrigados, pero el “sitio de acoplamiento” específico de PSMA que los investigadores necesitaban estaba esencialmente ausente.
Ingeniería de un tumor que exhibe el objetivo correcto
Ante este escollo, los investigadores tomaron una ruta más directa. Modificaron genéticamente una línea celular humana ampliamente usada de cáncer de mama triple negativo, MDA-MB-231, para obligarla a producir PSMA en su superficie. Estas células alteradas se implantaron posteriormente en la grasa mamaria de ratones inmunodeficientes, un sitio que imita mejor el entorno natural de la mama. Los científicos crearon dos versiones del modelo: una en la que todas las células tumorales expresaban PSMA y otro tumor “mixto” que contenía partes iguales de células PSMA-positivas y células cancerosas ordinarias, para imitar los patrones dispares observados en pacientes. Ambos modelos formaron tumores con la misma fiabilidad y crecieron a velocidades similares que los tumores formados por células no modificadas, lo que mostró que añadir PSMA no alteró de forma extraña el comportamiento del cáncer.
Ver el nuevo objetivo en exploraciones y al microscopio
Al inyectar el trazador PET dirigido a PSMA en estos ratones, los tumores modificados brillaron intensamente en las exploraciones, con una captación tumoral aproximadamente diez veces mayor que la del hígado o el músculo. Esta señal fuerte y selectiva confirmó que PSMA estaba ahora presente en abundancia en las células cancerosas y era accesible para un fármaco circulante. El análisis microscópico del tejido tumoral confirmó lo observado: la tinción de PSMA era alta pero desigual, con parches de expresión más intensa y otros más débiles, semejando el patrón heterogéneo observado en cánceres de mama triple negativos humanos. Es importante que el PSMA añadido quedó confinado a las células tumorales y no a los vasos sanguíneos circundantes, manteniendo el modelo enfocado en terapias dirigidas a las células. Las áreas de tejido muerto dentro de tumores más grandes no captaban el trazador, coincidiendo con lo observado clínicamente.
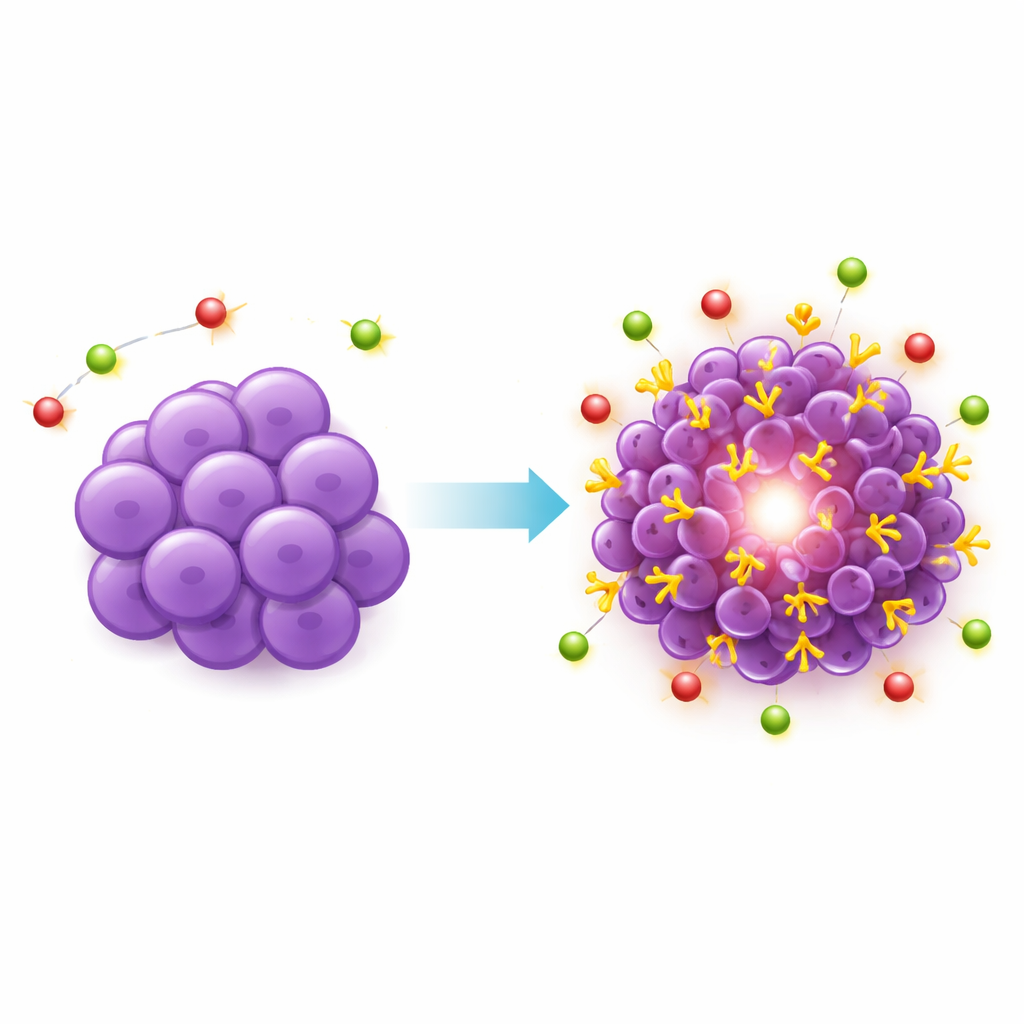
Qué significa esto para tratamientos futuros
Al mostrar de forma sistemática que los modelos murinos estándar de cáncer de mama no expresan PSMA de manera fiable y luego construir un nuevo modelo que sí lo hace, este trabajo proporciona un terreno de prueba crucial para las próximas generaciones de tratamientos de radiación dirigidos. El modelo de cáncer de mama triple negativo PSMA-positivo es estable, crece de manera predecible y muestra una mezcla realista de zonas con alta y baja expresión de PSMA, lo que lo hace idóneo para evaluar cómo se comportan los fármacos dirigidos a PSMA antes de probarlos en pacientes. Aunque este modelo no puede capturar todos los aspectos de la enfermedad humana—como la influencia de un sistema inmunitario completamente funcional—ofrece una herramienta poderosa para explorar si el éxito de las terapias basadas en PSMA en el cáncer de próstata podría algún día extenderse a personas que viven con esta forma particularmente agresiva de cáncer de mama.
Cita: Chaussin, B., Sanchez, L., Levesque, S. et al. Development and validation of a PSMA-positive triple-negative breast cancer mouse model for preclinical targeted radionuclide therapies. Sci Rep 16, 9348 (2026). https://doi.org/10.1038/s41598-026-36724-7
Palabras clave: cáncer de mama triple negativo, PSMA, terapia radionúclida dirigida, modelo murino preclínico, imagen PET