Clear Sky Science · es
Eliminación parcial de la isoforma larga de la quinasa WNK1 mitiga la glomerulonefritis anti-membrana basal glomerular en ratones
Por qué importa para la salud renal
Las enfermedades renales de rápida progresión pueden destruir los diminutos filtros del órgano en cuestión de semanas, a menudo conduciendo a diálisis o trasplante. Este estudio explora si reducir la actividad de una única proteína, llamada L-WNK1, puede ralentizar esa destrucción en ratones. Dado que ya se están desarrollando fármacos contra esta proteína para problemas de presión arterial, los hallazgos apuntan a una posible nueva forma de proteger los riñones bajo ataque.
Un control de tráfico dentro de los filtros renales
Cada riñón contiene cientos de miles de filtros microscópicos, o glomérulos, que limpian la sangre. Dentro de estos filtros, dos tipos celulares clave trabajan en conjunto: los podocitos, que se enrollan alrededor de los vasos como dedos entrelazados, y las células epiteliales parietales (CEP), que recubren la cápsula exterior. En una condición peligrosa llamada glomerulonefritis rápidamente progresiva (GNRP), los podocitos resultan dañados y las CEP se vuelven hiperactivas, acumulándose en “medias lunas” que bloquean la filtración. La proteína L-WNK1, un interruptor de señalización mejor conocido por ayudar a equilibrar la sal y la presión arterial, en realidad se produce en grandes cantidades en estas células glomerulares. Los autores se preguntaron si un exceso de L-WNK1 empeora la GNRP y si reducirla podría atenuar la enfermedad.
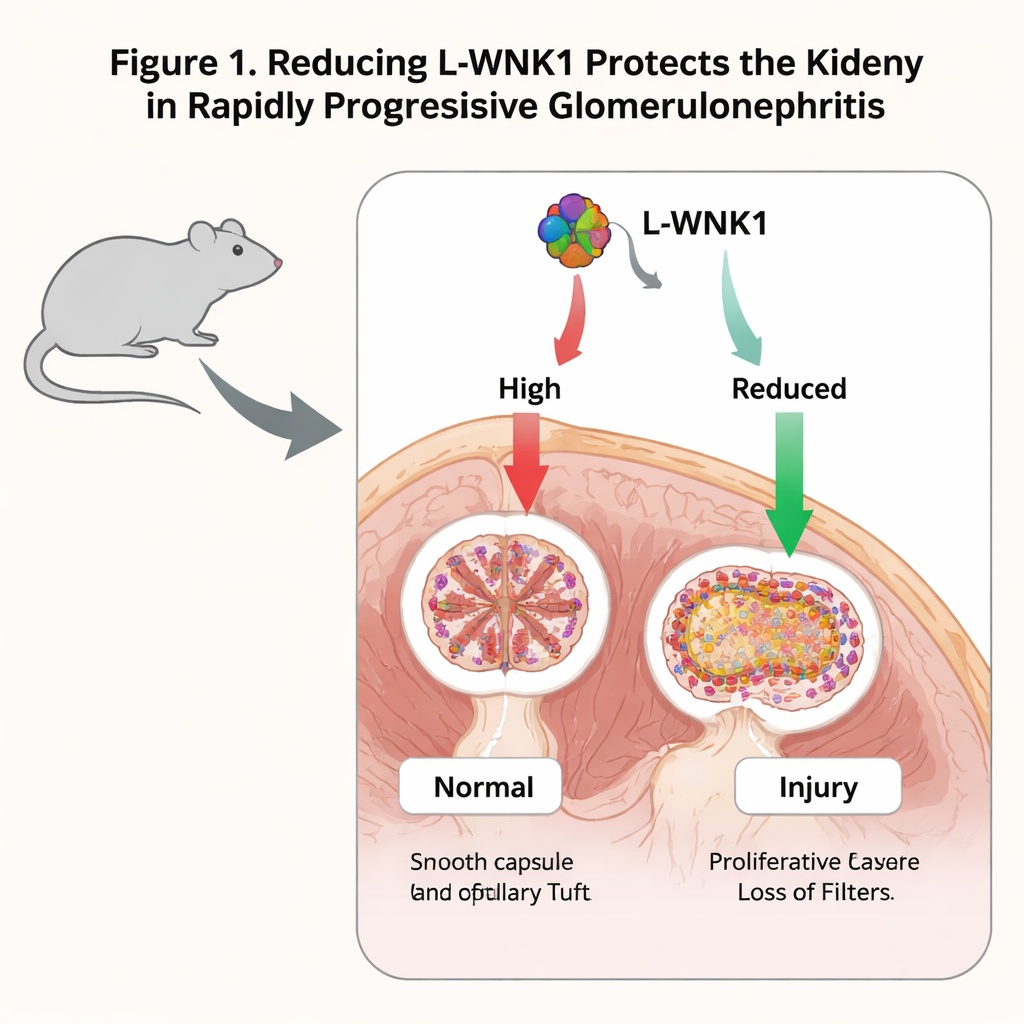
Reducir L-WNK1 alivia el daño renal en ratones
Los investigadores primero usaron un modelo clásico de ratón de GNRP desencadenado por anticuerpos que atacan la membrana basal glomerular, un componente clave del filtro. Encontraron que los niveles de L-WNK1 aumentaron en los glomérulos tras la lesión, no solo en ratones sino también en biopsias renales de pacientes con enfermedades relacionadas. Para probar causalidad, estudiaron ratones nacidos con una sola copia funcional del gen L-WNK1. Estos animales desarrollaron insuficiencia renal tras la lesión por anticuerpos, pero sus niveles de desechos en sangre fueron menores y el tejido renal mostró menos medias lunas y menos cicatrización que en los ratones normales. Marcadores de inflamación y fibrosis, como las moléculas de señalización MCP-1, TGF-β1 y genes de colágeno, también se redujeron. En conjunto, esto sugiere que la pérdida parcial de L-WNK1 hace que la enfermedad sea más leve en lugar de más grave.
Acercándose a los podocitos y sus vecinos
Puesto que los podocitos son centrales para la salud glomerular y expresan fuertemente L-WNK1, el equipo a continuación eliminó WNK1 específicamente en estas células mediante un truco genético. En condiciones normales, estos ratones tenían riñones sanos, lo que demuestra que los podocitos no necesitan L-WNK1 para desarrollarse o funcionar en la vida cotidiana. Cuando se indujo la GNRP, los ratones con eliminación específica en podocitos volvieron a presentar mejoría respecto a los controles: sus análisis de sangre mejoraron y tendieron a tener menos medias lunas y menos CEP que expresaban CD44, un marcador de activación. Sin embargo, la protección fue más débil que en los ratones con reducción más amplia y generalizada de L-WNK1, y los niveles de algunos marcadores inflamatorios no disminuyeron. Esto apunta a un papel de L-WNK1 no solo en podocitos sino también en otras células glomerulares o inmunitarias que participan en la enfermedad.
Ralentizando el movimiento celular nocivo
Para explorar cómo L-WNK1 podría impulsar la formación de medias lunas, los investigadores recurrieron a cultivos celulares. Usando una pequeña molécula que bloquea las quinasas WNK, trataron podocitos humanos cultivados en placas y observaron la velocidad con que se desplazaban para cubrir una brecha artificial de “herida”. Bloquear la actividad de L-WNK1 ralentizó notablemente su movimiento. Observaron un efecto similar en CEP cultivadas: cuando se añadía un factor de crecimiento, las CEP normalmente se expandían para llenar la brecha, pero esta respuesta se atenuó cuando el inhibidor de WNK estaba presente. Curiosamente, el fármaco no perturbó de forma apreciable el andamiaje interno de los podocitos en su sistema, a pesar de trabajos anteriores en células de ratón que sugerían problemas estructurales importantes. Esto respalda la idea de que, al menos en animales vivos, el papel principal de L-WNK1 aquí puede ser controlar cómo las células glomerulares e inmunitarias se desplazan y responden durante la lesión, más que mantener la arquitectura básica del filtro.
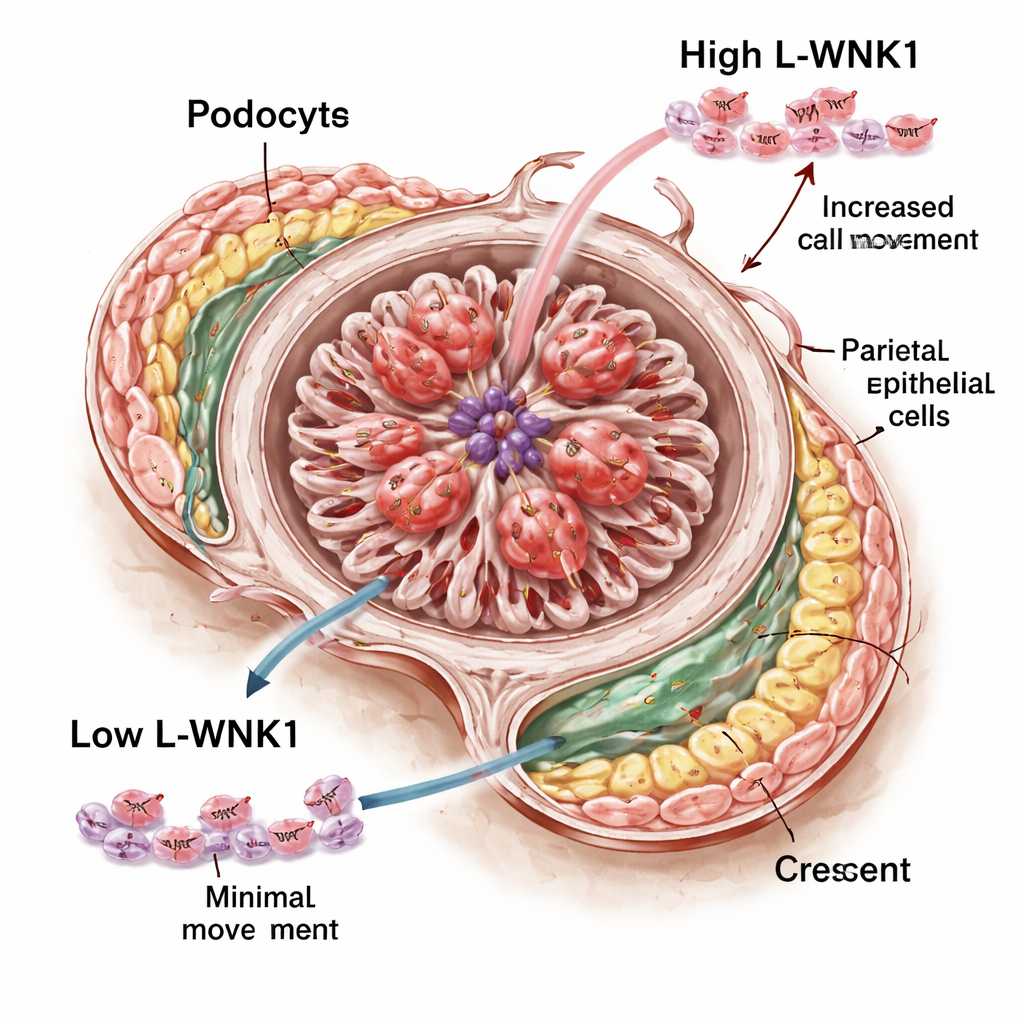
Qué significa esto para tratamientos futuros
En conjunto, el estudio revela a L-WNK1 como un acelerador dañino en una forma violenta de inflamación renal: cuando esta proteína aumenta, las células clave del glomérulo se mueven y se multiplican de formas que obstruyen y cicatrizan los filtros; cuando su actividad se reduce, el daño se suaviza. Dado que L-WNK1 ya se estudia como diana farmacológica para la presión arterial, estos hallazgos plantean la posibilidad de que inhibidores finamente ajustados puedan algún día ayudar a proteger a pacientes con enfermedades renales de rápida progresión. Queda mucho trabajo por hacer para traducir los resultados en ratones y cultivos celulares en terapias seguras, pero L-WNK1 destaca ahora como un nuevo y prometedor punto de intervención en una condición que por lo demás es devastadora.
Cita: Mousseaux, C., Migeon, T., Frère, P. et al. Knock-down of the long isoform of the WNK1 kinase mitigates the anti-glomerular basement membrane glomerulonephritis in mice. Sci Rep 16, 7335 (2026). https://doi.org/10.1038/s41598-026-36715-8
Palabras clave: glomerulonefritis rápidamente progresiva, inflamación renal, podocitos, medias lunas glomerulares, inhibición de WNK1