Clear Sky Science · es
Identificación y verificación de SPP1 en anoikis como biomarcador pronóstico para la metaplasia intestinal y el cáncer gástrico
Por qué esto importa para la salud del estómago
El cáncer gástrico (de estómago) es uno de los cánceres más mortales del mundo, en gran parte porque suele diagnosticarse en fases avanzadas. Antes de que aparezca un tumor plenamente desarrollado, el revestimiento del estómago a menudo atraviesa una etapa de aviso llamada metaplasia intestinal, en la que las células estomacales normales empiezan a asemejarse a las del intestino. Este estudio sigue todo ese recorrido —desde tejido sano, pasando por la metaplasia intestinal, hasta el cáncer gástrico— para buscar una señal única y medible en el tejido que pueda indicar riesgo alto de forma temprana y ayudar a los médicos a predecir qué pacientes tienen más probabilidades de tener mal pronóstico y podrían beneficiarse de un seguimiento más estrecho o de nuevos tratamientos.
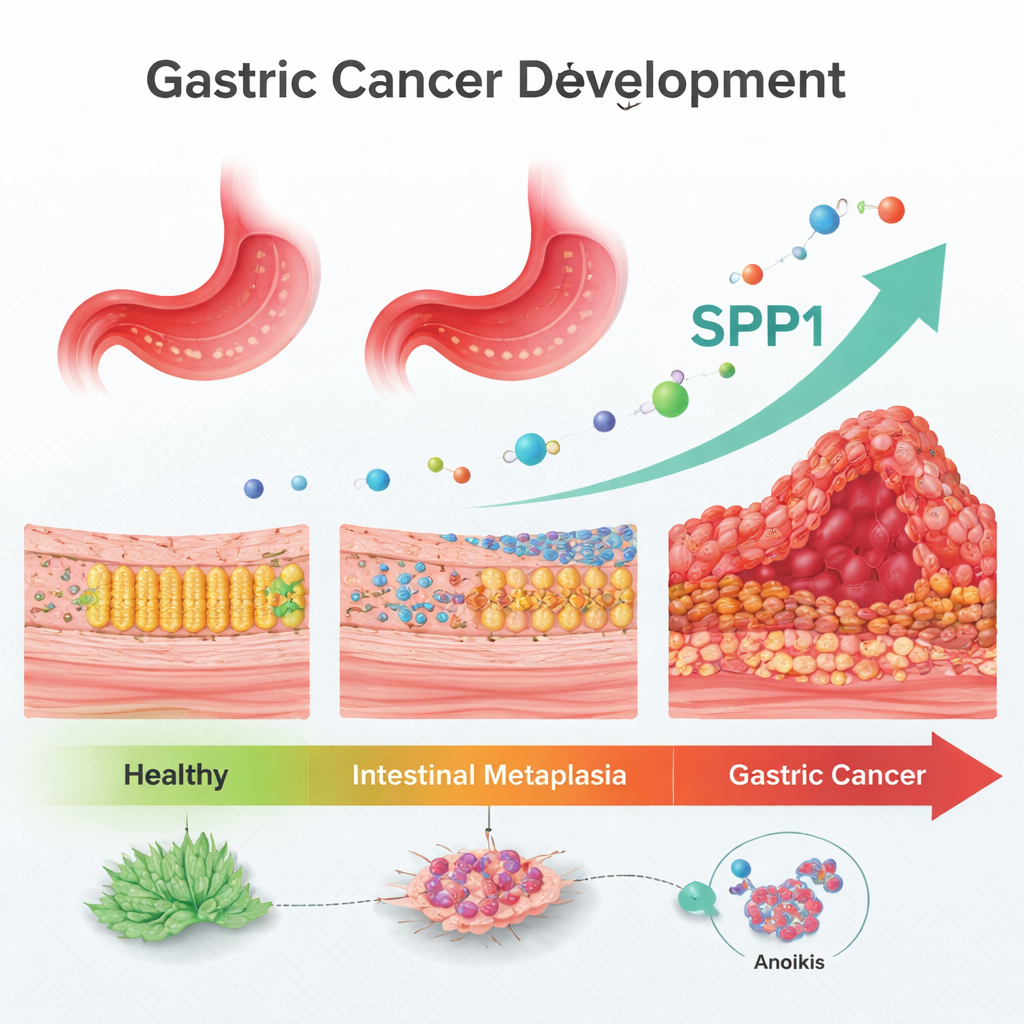
Un peldaño en el camino hacia el cáncer
Los médicos saben desde hace tiempo que la metaplasia intestinal es una condición premaligna, pero carecen de marcadores fiables que indiquen quién progresará realmente a cáncer. Los investigadores se centraron en un tipo de muerte celular llamado anoikis, que normalmente elimina las células que se desprenden de su lugar correcto en un tejido. Las células cancerosas deben aprender a resistir la anoikis para poder desplazarse, sobrevivir en el torrente sanguíneo e implantarse en órganos distantes. Mediante la explotación de grandes bases de datos públicas de genes procedentes de cientos de pacientes, el equipo buscó genes relacionados con la anoikis que cambiaran de forma sostenida a lo largo de la “cascada de Correa”: mucosa gástrica sana, metaplasia intestinal y finalmente cáncer gástrico.
Focalizando una molécula clave de aviso
Usando herramientas estadísticas avanzadas y análisis de redes, los científicos identificaron repetidamente un gen destacado: SPP1, que codifica una proteína también conocida como osteopontina. En tres conjuntos de datos independientes, los niveles de SPP1 fueron consistentemente bajos en tejido gástrico sano, más altos en la metaplasia intestinal y máximos en el cáncer gástrico. Este patrón por etapas se mantuvo incluso tras corregir las diferencias técnicas entre estudios. Análisis informáticos adicionales de miles de genes mostraron que la alta expresión de SPP1 tendía a aparecer junto con cambios en vías relacionadas con la inmunidad y las respuestas al estrés ambiental y químico, lo que sugiere que la molécula podría estar conectando la supervivencia celular, la irritación crónica y el sistema inmune durante el desarrollo del cáncer.
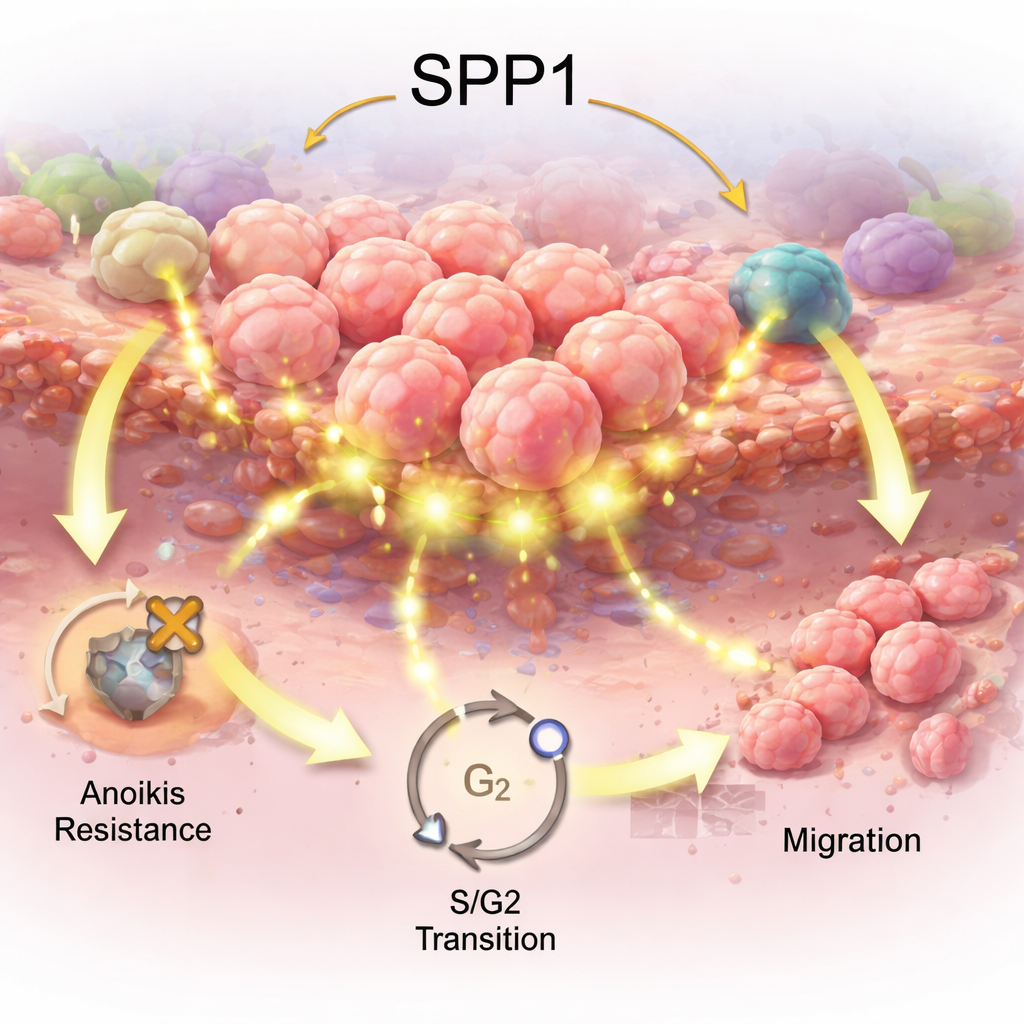
Pistas desde las células de defensa del organismo
El equipo examinó a continuación cómo se relaciona SPP1 con las células inmunitarias que infiltran los tumores. En muestras tumorales globales, una mayor expresión de SPP1 se asoció con cambios en el equilibrio de células inmunitarias, incluyendo aumentos en ciertos macrófagos y linfocitos T que pueden o bien atacar a los tumores o ser desactivados por ellos. La secuenciación de ARN a nivel de célula única —leer la actividad génica célula por célula— reveló que SPP1 se activaba de forma intensa en macrófagos asociados al tumor y en otras células del microambiente tumoral. Las señales que involucran SPP1 y un receptor asociado llamado CD44 parecieron conectar a estos macrófagos con linfocitos T colaboradores, sugiriendo que esta vía podría ayudar a crear un “vecindario” inmunológico que favorece la supervivencia tumoral en lugar de su eliminación. Aunque estos vínculos son correlativos, apuntan a SPP1 como un posible actor en la forma en que los tumores gástricos eluden el ataque inmunitario.
De los macrodatos a los tejidos y células reales
Para comprobar que los hallazgos computacionales coincidían con la realidad, los investigadores midieron SPP1 en 32 muestras humanas de tejido gástrico. Tanto las pruebas de gen como las de proteína mostraron la misma tendencia: niveles más bajos en tejido normal, más altos en metaplasia intestinal y más altos aún en cáncer gástrico. Los pacientes cuyos tumores expresaban más SPP1 tuvieron una supervivencia global sustancialmente peor, y los modelos estadísticos sugirieron que SPP1 ayudaba a predecir los resultados a uno, tres y cinco años. En cultivos celulares, reducir la expresión de SPP1 en una línea celular de cáncer gástrico ralentizó el crecimiento celular, disminuyó su capacidad de migrar, aumentó la muerte celular programada y provocó que las células se detuvieran en una fase crítica del ciclo celular. Estos experimentos respaldan la idea de que SPP1 contribuye activamente a que las células cancerosas resistan la muerte y sigan dividiéndose.
Qué podría significar esto para los pacientes
Para el público general, la conclusión es que SPP1 actúa como una alarma creciente a lo largo del camino desde un revestimiento gástrico “de riesgo pero aún no canceroso” hasta el cáncer establecido. Los niveles altos de esta molécula señalan tejidos con mayor probabilidad de progresar y pacientes con más probabilidad de tener malos resultados. Aunque se necesita más trabajo —especialmente estudios con más pacientes y experimentos en animales— monitorizar SPP1 en biopsias de metaplasia intestinal podría en el futuro ayudar a los médicos a decidir quién necesita una vigilancia más estrecha o un tratamiento precoz. En el cáncer gástrico establecido, fármacos que bloqueen SPP1 o sus socios clave podrían debilitar las defensas del tumor, tanto haciendo a las células cancerosas más vulnerables a la muerte como remodelando las células inmunitarias circundantes para combatir la enfermedad de forma más eficaz.
Cita: Wu, K., Ye, Y., Pei, B. et al. Identification and verification of SPP1 in anoikis as a prognostic biomarker for intestinal metaplasia and gastric cancer. Sci Rep 16, 5842 (2026). https://doi.org/10.1038/s41598-026-36714-9
Palabras clave: cáncer gástrico, metaplasia intestinal, biomarcadores, osteopontina SPP1, microambiente tumoral