Clear Sky Science · es
Exosomas derivados del colangiocarcinoma atenúan las funciones antitumorales de las células NK
Cómo un cáncer oculto engaña al sistema inmune
El colangiocarcinoma, un cáncer de los conductos biliares intrahepáticos, es notoriamente difícil de detectar de forma temprana y complejo de tratar. Este estudio explora una táctica sutil que estos tumores usan para eludir las defensas naturales del cuerpo: envían pequeños paquetes llamados exosomas que debilitan discretamente a las células asesinas naturales (NK), un destacamento de la respuesta inmune especializado en buscar y eliminar células cancerosas. Comprender esta estrategia sigilosa podría abrir nuevas vías terapéuticas para restaurar la capacidad del sistema inmune de contraatacar.
Los primeros intervinientes del cuerpo contra el cáncer
Las células NK pertenecen al sistema inmune innato, la fuerza de respuesta rápida del organismo. A diferencia de muchas células inmunitarias que necesitan tiempo para reconocer una amenaza específica, las NK pueden atacar con rapidez células anormales, incluidas las infectadas por virus y las cancerosas. Lo hacen adhiriéndose a los blancos y liberando moléculas tóxicas como la granzima B y proteínas señalizadoras como el interferón gamma (IFN-γ) que, a la vez que matan células tumorales, reclutan a otros defensores inmunes. En muchas neoplasias hematológicas y algunos tumores sólidos, potenciar la actividad de las NK ha mostrado ser una estrategia terapéutica prometedora. Pero en tumores sólidos como el cáncer de vía biliar, las NK a menudo parecen escasas y poco activas justo donde más se necesitan.
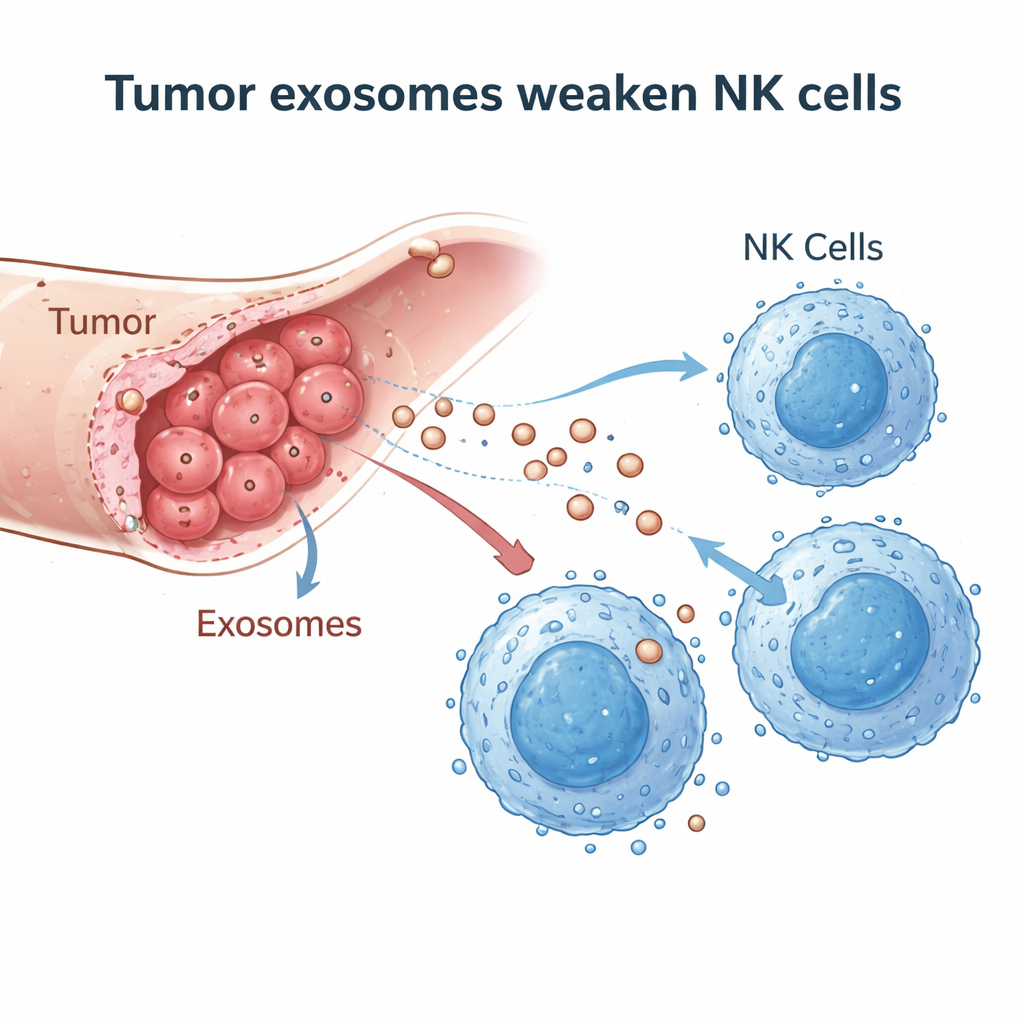
Vesículas diminutas con gran impacto
Los investigadores sospecharon que las células de colangiocarcinoma podrían estar saboteando a las NK mediante exosomas: burbujas de membrana de tamaño nanométrico cargadas de proteínas y material genético que las células liberan para comunicarse. Recolectaron exosomas de una línea celular humana de cáncer de conducto biliar y de la sangre de pacientes con colangiocarcinoma, y confirmaron su identidad y tamaño mediante microscopia electrónica, seguimiento de partículas y marcadores estándar de exosomas. En muestras de tejido tumoral de 20 pacientes, compararon áreas cancerosas con tejido hepático no canceroso cercano y encontraron muchas menos células NK infiltrando los tumores, lo que sugiere que algo en el microambiente tumoral mantenía a las NK alejadas o las desactivaba.
Apagando señales de supervivencia y de muerte del tumor
Para ver cómo estos exosomas tumorales afectan a las NK, el equipo expuso una línea celular de NK (NK-92) a exosomas de células tumorales y a exosomas de sangre de pacientes. Las NK empezaron a experimentar niveles más altos de muerte celular programada, especialmente al tratarlas con exosomas de la línea celular tumoral. A nivel molecular, las NK redujeron la producción de proteínas clave de “permanecer vivas” (BCL-2 y BCL-XL), inclinando el balance hacia la muerte celular. Curiosamente, su crecimiento y división global no cambiaron, lo que indica que los exosomas hicieron que las NK fueran más propensas a morir en lugar de ralentizar su proliferación. Las NK tratadas con exosomas también secretaron menos IFN-γ y menos granzima B, debilitando tanto su capacidad de matar directamente a los blancos como de coordinar respuestas inmunes más amplias. Pruebas de laboratorio que midieron la capacidad de las NK para matar células diana estándar mostraron que ese poder citotóxico disminuyó tras la exposición a exosomas de colangiocarcinoma.
Rompiendo la colaboración entre células inmunes
Las NK necesitan adherirse entre sí y a las células tumorales para funcionar eficazmente, recurriendo a moléculas de adhesión en la superficie que actúan como un velcro molecular. Tras el tratamiento con exosomas derivados del cáncer, las NK perdieron su patrón normal de crecimiento en cúmulos y parecieron más dispersas. Los investigadores hallaron que los niveles de varias moléculas de adhesión importantes (CD11a, CD18 y CD54) descendieron tanto a nivel de gen como de proteína, mientras que otro marcador de adhesión, CD2, permaneció sin cambios. Esta pérdida de adhesión probablemente dificulta que las NK lleguen a los tumores, formen contactos estables con las células cancerosas y asesten golpes letales. De manera crucial, al estudiar directamente las NK de la sangre de pacientes con colangiocarcinoma, esas células mostraron las mismas características: menor actividad citotóxica y niveles más bajos de las mismas moléculas de adhesión en comparación con NK de donantes sanos.
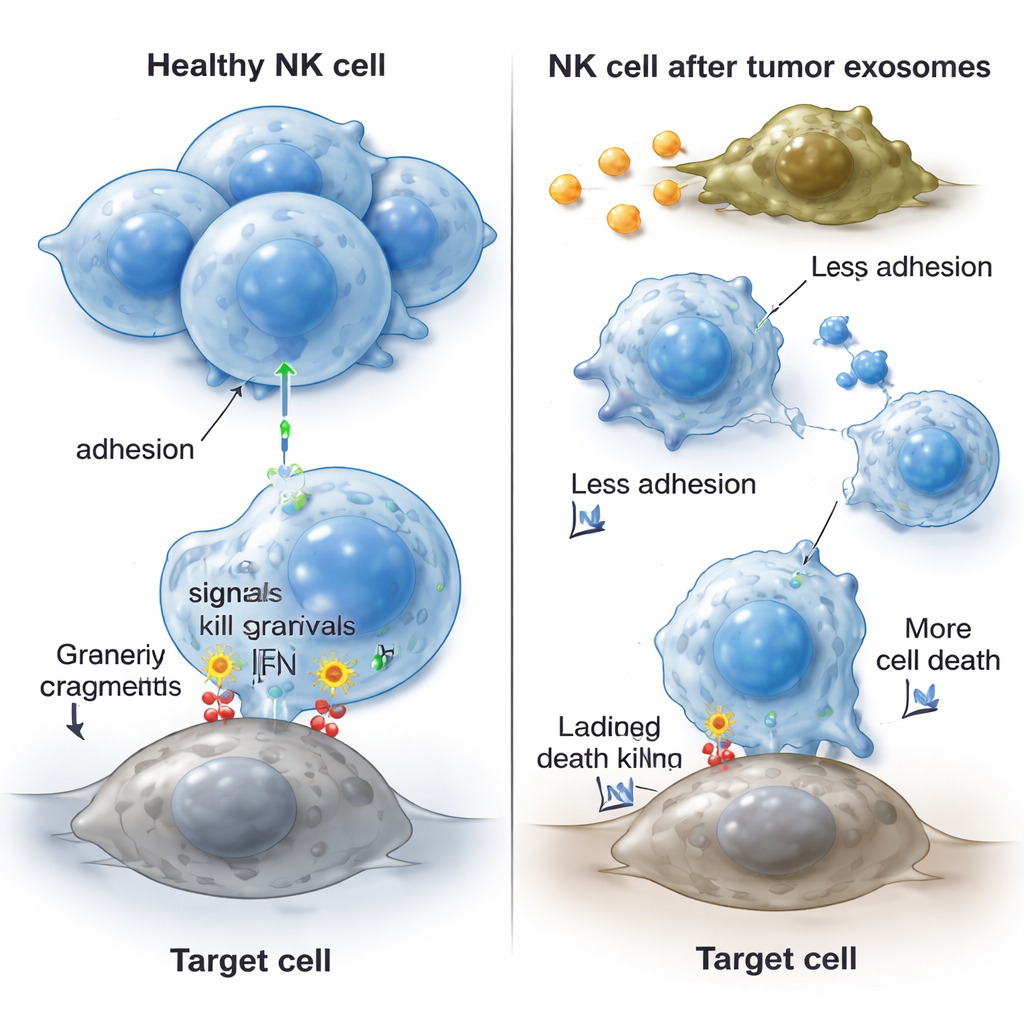
Qué significa esto para los pacientes y tratamientos futuros
En conjunto, los hallazgos sugieren que el colangiocarcinoma utiliza exosomas como una forma de sabotaje molecular para evadir el ataque inmune. Estas diminutas vesículas contribuyen a empujar a las NK hacia la muerte, reducen su producción de factores clave de muerte celular y eliminan las proteínas adhesivas que les permiten agruparse y atacar tumores. El resultado es menos NK funcionales en y alrededor del tumor y una respuesta inmune atenuada que permite al cáncer crecer con mayor libertad. Aunque gran parte de este trabajo se realizó en condiciones de laboratorio controladas y con un número limitado de muestras de pacientes, apunta a nuevas estrategias: bloquear los exosomas tumorales, restaurar las señales de supervivencia de las NK o potenciar las moléculas de adhesión podrían ayudar a reactivar las defensas naturales del organismo contra este letal cáncer de los conductos biliares.
Cita: Wang, X., Zhang, F., Cao, Z. et al. Cholangiocarcinoma derived exosomes attenuate the anti-tumor functions of NK cells. Sci Rep 16, 5810 (2026). https://doi.org/10.1038/s41598-026-36706-9
Palabras clave: colangiocarcinoma, células asesinas naturales, exosomas, escape inmune tumoral, microambiente tumoral