Clear Sky Science · es
Caracterización bioinformática y detección automatizada de subpoblaciones de monocitos metabolicamente activados en dislipidemia
Por qué importan las células inmunitarias ocultas para la salud del corazón
Los problemas de colesterol suelen contarse en términos de dieta, cifras en un análisis de sangre y riesgo de infarto. Pero bajo esas cifras, nuestro sistema inmunitario está cambiando silenciosamente. Este estudio analiza un grupo especial de glóbulos blancos en la sangre de adultos jóvenes con colesterol LDL («malo») alto. Estas células parecen volverse “metabólicamente activadas” y conservar memoria por exposiciones previas a exceso de grasas, lo que podría aumentar la inflamación arterial —y la probabilidad de enfermedad cardiaca futura. Comprender estos tipos celulares ocultos podría ayudar a los médicos a detectar problemas antes y diseñar tratamientos más precisos.
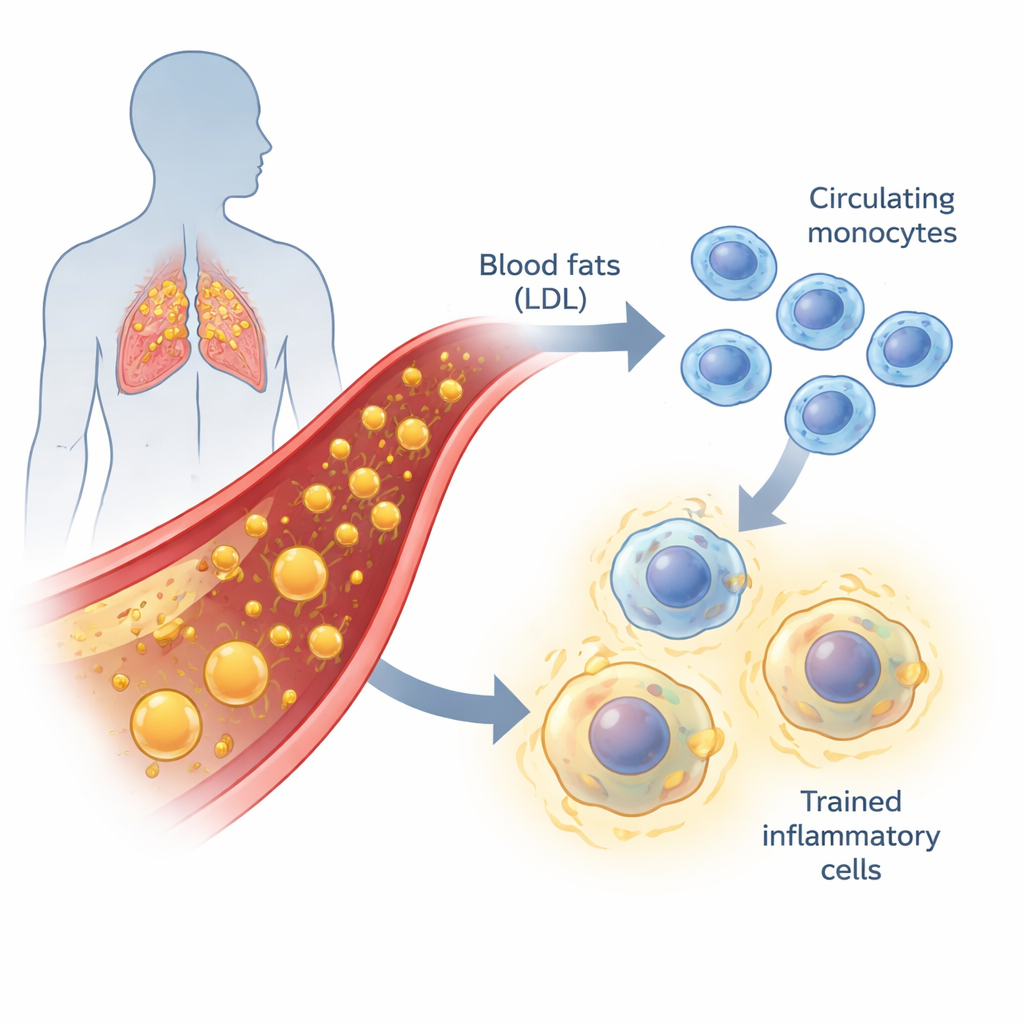
Grasa en la sangre e inflamación de bajo grado
La aterosclerosis, el proceso que conduce a las arterias obstruidas, no se trata solo de grasa que se adhiere a las paredes vasculares. También es una enfermedad inflamatoria lenta y crónica. Cuando el colesterol LDL es alto, especialmente en sus formas oxidadas, irrita el revestimiento de los vasos. Los monocitos —glóbulos blancos circulantes— y las células macrofágicas en las que se convierten son atraídos a estas zonas y comienzan a engullir grasa. Si este proceso de limpieza está mal regulado, las células se transforman en «células espumosas» y contribuyen a la formación de placas grasas. Tradicionalmente, los científicos han dividido los monocitos sanguíneos en tres grupos según marcadores de superficie, cada uno con roles distintos en el patrullaje vascular, la activación inflamatoria o el mantenimiento tisular.
Más allá de las etiquetas simples: descubriendo nuevos tipos de monocitos
Los autores sospechaban que algunos monocitos circulantes en personas con dislipidemia (niveles de lípidos en sangre no saludables) podrían ya estar reprogramados hacia un estado metabólicamente activo, preparados para convertirse en macrófagos dañinos. Para investigarlo, tomaron sangre de 23 adultos jóvenes con colesterol LDL alto y de 17 participantes sanos con perfiles lipídicos normales. Ninguno tomaba fármacos para bajar el colesterol ni tenía otras enfermedades importantes, lo que ayudó a aislar el impacto de la dislipidemia en sí. Usando una técnica llamada citometría de flujo, midieron no solo los marcadores de superficie clásicos sino también proteínas implicadas en el manejo de grasas y marcas químicas en histonas —pequeños carretes proteicos que ayudan a controlar qué genes se activan o silencian en cada célula.
Algoritmos inteligentes para leer paisajes inmunitarios complejos
En lugar de basarse únicamente en el «gating» manual (dibujar fronteras a ojo en gráficos de dos marcadores), el equipo construyó una canalización bioinformática que trató cada célula como un punto en un espacio de alta dimensión. Limpió y estandarizó los datos, y luego usó t-SNE, un método matemático que convierte mediciones con muchos marcadores en un mapa bidimensional donde las células similares se agrupan. A continuación aplicaron algoritmos de clustering (X-shift y FlowSOM) para agrupar automáticamente células con patrones de marcadores similares. Esto les permitió ir más allá de los tres tipos clásicos de monocitos e identificar cuatro poblaciones mononucleares principales definidas por combinaciones de proteínas de manejo de lípidos (ABCA1, PLIN2, CD36) y los marcadores habituales CD14 y CD16.
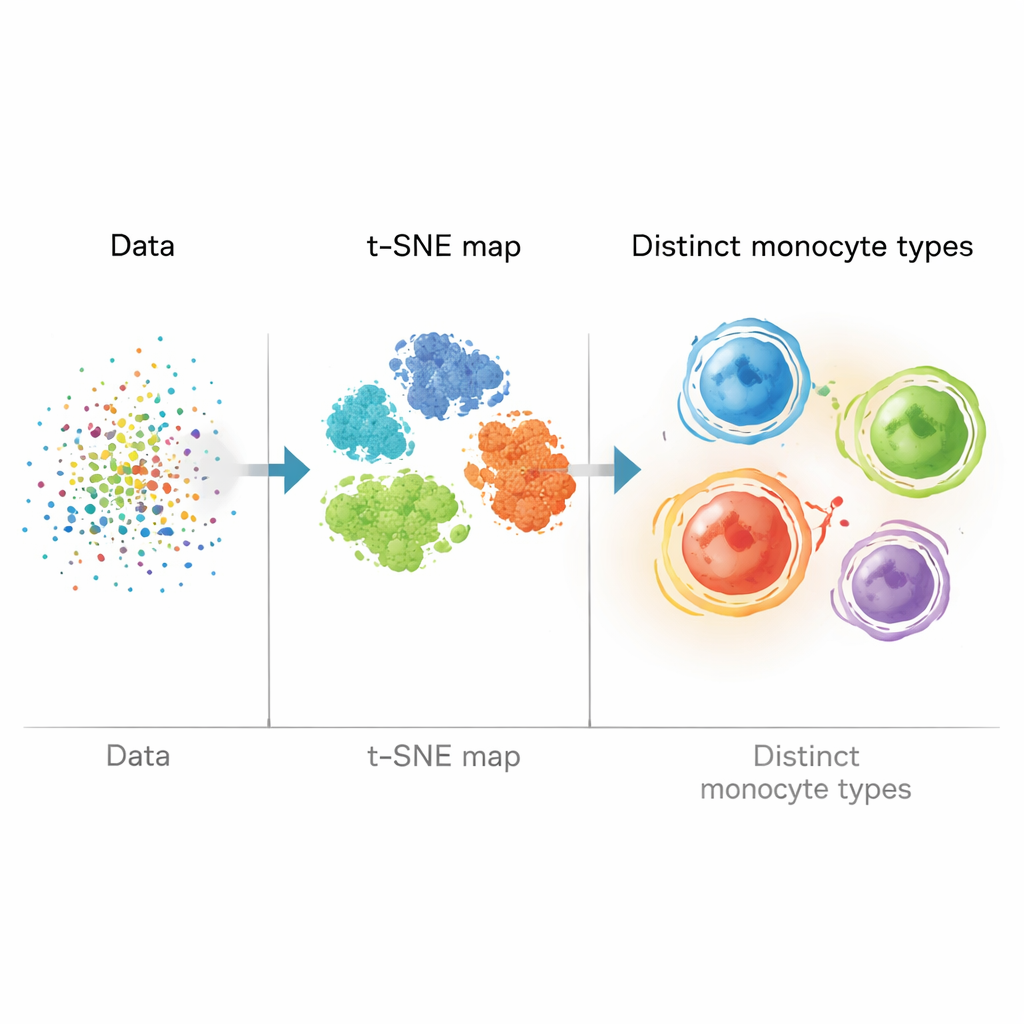
Una población inflamatoria primada en dislipidemia
Dos de estas cuatro agrupaciones de monocitos llamaron la atención. Una en particular —caracterizada por alto CD14, ausencia de CD16 y fuerte expresión de ABCA1 con PLIN2 y CD36 variables— coincidía con el perfil de monocitos “metabólicamente activados” (MoMe). En personas con dislipidemia, esta población MoMe y otro grupo relacionado fueron significativamente más abundantes que en los controles sanos. Al examinar las marcas epigenéticas —específicamente H3K4me3 y H3K27me3, que son etiquetas químicas en proteínas histonas vinculadas a la actividad génica— encontraron que las células MoMe de individuos dislipidémicos mostraban niveles más altos de H3K4me3. Esta marca se asocia con genes que promueven la inflamación, lo que sugiere que estas células tienen una forma de “memoria” innata, o inmunidad entrenada, tras exposiciones repetidas a LDL elevado.
De células circulantes a macrófagos que construyen placa
Para ver en qué podrían convertirse estos monocitos dentro de los tejidos, el equipo cultivó monocitos purificados en un entorno de laboratorio que imitaba el síndrome metabólico, impulsándolos a diferenciarse en macrófagos. De nuevo emplearon análisis avanzados para identificar subgrupos de macrófagos y midieron sus marcas epigenéticas. Curiosamente, los macrófagos derivados de donantes sanos con frecuencia mostraron niveles más altos de marcas histonas activadoras que los provenientes de pacientes dislipidémicos, lo que sugiere que el entrenamiento inflamatorio puede manifestarse de forma diferente una vez que las células abandonan el torrente sanguíneo. Aunque el tamaño de la muestra fue modesto, los hallazgos respaldan la idea de que la exposición prolongada a lípidos sanguíneos en exceso remodela los monocitos tanto a nivel proteico como epigenético, predisponiéndolos a respuestas inflamatorias más potentes.
Qué significa esto para los pacientes y la atención futura
Para el público general, la conclusión es que el colesterol LDL alto no es solo un problema de «demasiada grasa» sino también de células inmunitarias «reprogramadas». Este estudio muestra que incluso en adultos jóvenes, la dislipidemia se asocia con una población distintiva de monocitos que parecen metabólicamente cargados y epigenéticamente predispuestos a alimentar la inflamación arterial. Al combinar potentes herramientas computacionales con mediciones celulares detalladas, los investigadores pueden ahora detectar estos tipos celulares de riesgo en la sangre mucho antes de que ocurra un infarto. En el futuro, tales enfoques podrían ayudar a los médicos a evaluar mejor el riesgo cardiovascular, monitorizar si los tratamientos revierten el entrenamiento inmunitario perjudicial y, en última instancia, diseñar terapias que apunten no solo a los niveles de colesterol sino también a las células inmunitarias que responden a ellos.
Cita: Ramírez-Torres, R., Ramírez-Segovia, S.G., González-Huerta, M.J. et al. Bioinformatic characterization and automated detection of metabolically activated monocyte subpopulations in dyslipidemia. Sci Rep 16, 6170 (2026). https://doi.org/10.1038/s41598-026-36678-w
Palabras clave: dislipidemia, monocitos, inmunidad entrenada, aterosclerosis, citometría de flujo