Clear Sky Science · es
Aplicación de Lactococcus que expresa la proteína similar al colágeno 1 del estreptococo del grupo A como una nueva inmunoterapia contra el adenocarcinoma ductal pancreático
Convertir bacterias amigas en combatientes contra el cáncer
El cáncer de páncreas es uno de los más letales, en parte porque se protege detrás de defensas potentes que inactivan el sistema inmunitario del organismo. Este estudio explora un aliado inesperado en la lucha contra esta enfermedad: una bacteria «buena» común del ámbito lácteo, reingenierizada para localizar tumores pancreáticos y ayudar al sistema inmune a atacarlos con mayor eficacia. Tomando una proteína de superficie adhesiva de un estreptococo peligroso, los investigadores transformaron un microbio inocuo en una herramienta anticancerígena dirigida en ratones.
Un cáncer duro que supera al sistema inmune
El adenocarcinoma ductal pancreático es notoriamente letal: solo alrededor de uno de cada ocho pacientes vive cinco años después del diagnóstico. Una razón principal es su microambiente tumoral: una cáscara densa, similar a una cicatriz, repleta de células y moléculas de soporte que amortiguan los ataques inmunitarios y bloquean muchos fármacos. Entre los culpables están las trampas extracelulares de neutrófilos, o NETs: redes de ADN y proteínas que las células blancas proyectan al entorno. En el cáncer de páncreas, estas redes pegajosas hacen más daño que bien: ayudan al crecimiento tumoral, mantienen a las células T asesinas alejadas y se asocian con peores resultados. Inactivar las NETs, al tiempo que se reactiva la inmunidad antitumoral, se ha convertido en una estrategia atractiva.
Tomar prestada una proteína adhesiva, pero no el germen peligroso
Trabajos previos mostraron que una proteína de superficie del Streptococcus del grupo A, llamada Scl1, puede tanto adherirse a las fibras asociadas al tumor como reducir la formación de NETs, ralentizando el crecimiento tumoral pancreático en ratones. Pero el estreptococo del grupo A también es la bacteria que causa la faringitis estreptocócica y las infecciones invasivas graves, por lo que no es adecuada como terapia viva. Para conservar la proteína útil evitando el germen dañino, el equipo diseñó Lactococcus lactis —un probiótico ampliamente usado en alimentación y considerado seguro— para mostrar Scl1 en su superficie. Esta nueva cepa, denominada Lactococcus::620, se probó en ratones portadores de tumores pancreáticos, usando tanto tumores subcutáneos simples como modelos más realistas con tumores creciendo en el propio páncreas.
Bacterias guiadas reducen el crecimiento tumoral y prolongan la supervivencia
Cuando se inyectó una sola dosis de las bacterias modificadas directamente en tumores subcutáneos, o se administró en la cavidad abdominal, los tumores crecieron más despacio y pesaron menos que en ratones tratados con Lactococcus ordinario o con un control salino. En el modelo pancreático más exigente se necesitaron dosis múltiples cada tres días, pero los beneficios fueron llamativos. Lactococcus::620 redujo el tamaño de los tumores, disminuyó su peso y alargó la supervivencia de los animales sin causar muertes relacionadas con el tratamiento. La microscopía y el cultivo de tejido tumoral mostraron que las bacterias portadoras de Scl1 se acumulaban de forma fiable en la zona tumoral, especialmente en la matriz fibrosa depositada por fibroblastos asociados al cáncer, mientras que en gran medida respetaban el bazo. En contraste, Lactococcus no modificado se diseminó más ampliamente por el organismo y a veces fue tóxico cuando se administró sistémicamente.
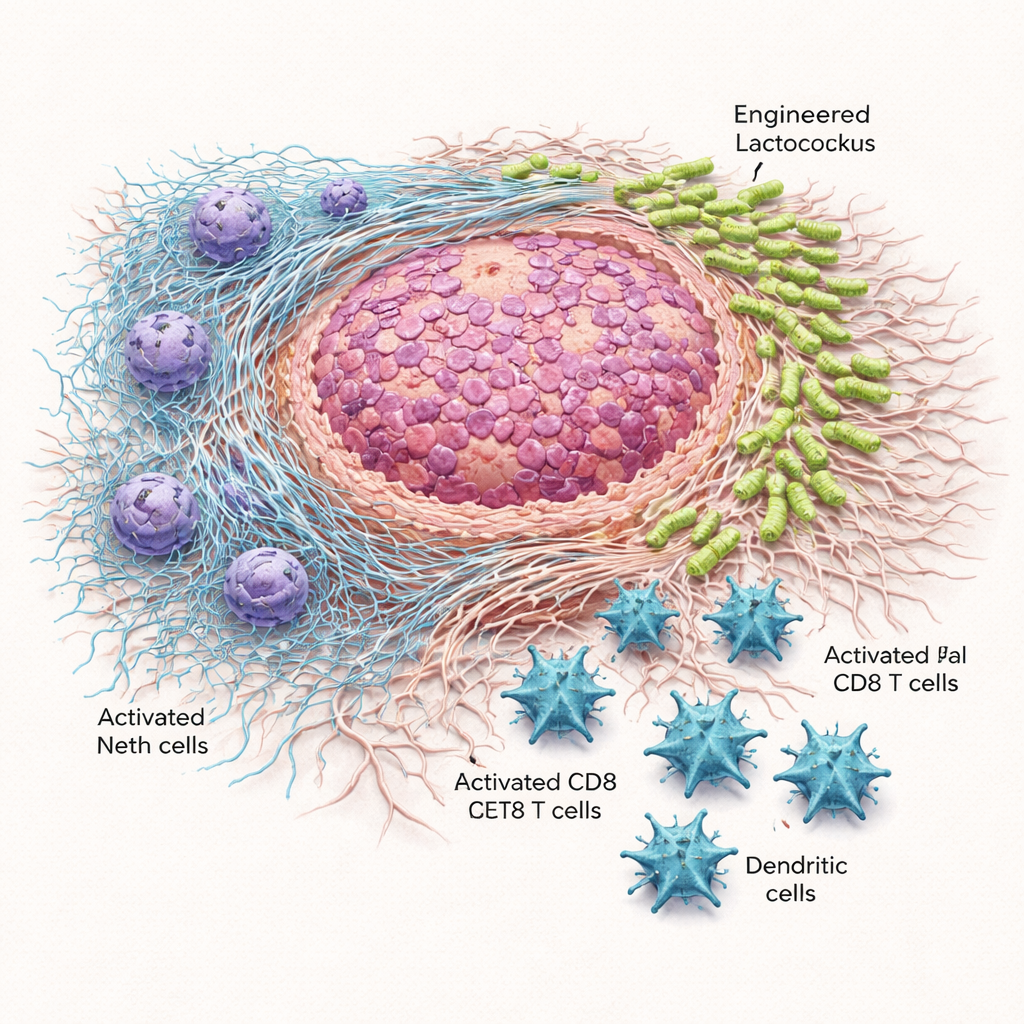
Desarmar redes dañinas y permitir la entrada de células inmunitarias
Las bacterias modificadas también remodelaron el paisaje inmune alrededor de los tumores. Los tumores de ratones tratados con Lactococcus::620 contenían más células T CD8 «asesinas» y más células dendríticas —actores clave en el reconocimiento y destrucción de células cancerosas—, y esas células T mostraron menos marcadores de agotamiento y más moléculas asociadas a la actividad. Al mismo tiempo, las medidas de actividad de las NETs disminuyeron. En pruebas de laboratorio, los neutrófilos expuestos a Lactococcus::620 liberaron menos ADN libre y mostraron menor actividad de mieloperoxidasa, una enzima necesaria para construir NETs. En los ratones tratados, el ADN circulante ligado a NETs se redujo. De forma crucial, cuando los mismos experimentos se realizaron en ratones genéticamente incapaces de formar NETs, las bacterias modificadas dejaron de frenar el crecimiento tumoral. Esa pérdida de beneficio sugiere con fuerza que la inhibición de las NETs es central para el poder de la terapia.
Lo que esto podría significar para la atención del cáncer en el futuro
En conjunto, los hallazgos delinean un concepto nuevo: usar una bacteria segura, de grado alimentario, como vehículo programable para llevar una proteína que bloquea NETs y se dirige al tumor directamente al ambiente hostil del cáncer de páncreas. En ratones, este enfoque redujo la carga tumoral, mejoró la supervivencia y abrió la puerta para que las células inmunitarias cumplan mejor su función. Aunque queda mucho trabajo antes de que tal estrategia pueda probarse en personas —incluyendo ensayos en modelos de enfermedad metastásica y su combinación con inmunoterapias modernas—, el estudio muestra que bacterias “buenas” cuidadosamente diseñadas podrían algún día ayudar a inclinar la balanza contra uno de nuestros cánceres más resistentes.
Cita: Godfrey, E.A., Choi, S.J., Sestito, M. et al. Application of group A streptococcal collagen-like protein 1-expressing Lactococcus as a novel immunotherapeutic against pancreatic ductal adenocarcinoma. Sci Rep 16, 5911 (2026). https://doi.org/10.1038/s41598-026-36657-1
Palabras clave: cáncer de páncreas, terapia probiótica, microambiente tumoral, modulación inmune, trampas extracelulares de neutrófilos