Clear Sky Science · es
Efectos combinados del nitrato y compuestos antimicrobianos sobre biofilms subgingivales in vitro
Por qué tus encías y la salud intestinal están conectadas
Las encías sangrantes y la enfermedad periodontal suelen atribuirse a bacterias “malas”. Para combatirlas, los dentistas recurren a menudo a enjuagues bucales potentes y a antibióticos. Este estudio plantea una pregunta más amplia: ¿y si algunos de estos tratamientos dañan silenciosamente las bacterias beneficiosas que necesitamos, mientras que un nutriente sencillo presente en las verduras de hoja empuja a los microbios de la boca hacia un estado saludable?
La enfermedad de las encías como un problema de comunidad
La periodontitis es una infección crónica alrededor de los dientes que destruye los tejidos que los sostienen y se asocia con enfermedades cardíacas, diabetes e incluso trastornos cerebrales. En lugar de ser causada por un único germen, surge cuando toda la comunidad bacteriana de la boca cambia a un estado dañino, llamado disbiosis. El tratamiento moderno sigue apoyándose mucho en fármacos de acción amplia: antibióticos como la amoxicilina y el metronidazol, y enjuagues antisépticos como la clorhexidina. Estos productos pueden eliminar a los agentes problemáticos, pero también pueden borrar bacterias beneficiosas y fomentar la resistencia a los fármacos.
Una mirada más cercana a biofilms de pacientes reales
Para ver qué hacen realmente estos tratamientos a las bacterias de las encías, los investigadores recogieron placa de los bolsillos profundos alrededor de los dientes de 12 personas con periodontitis. En el laboratorio hicieron crecer estas muestras como capas finas de bacterias, o biofilms, durante ocho horas bajo ocho condiciones diferentes: sin tratamiento, nitrato solo, cada fármaco por separado y cada fármaco combinado con nitrato. El nitrato, un compuesto natural abundante en espinacas, lechuga y remolacha, puede ser transformado por ciertas bacterias bucales en óxido nítrico, un gas que ayuda a relajar los vasos sanguíneos y puede frenar el crecimiento de microbios asociados a la enfermedad. El equipo midió cuánto biofilm se formó, qué tan bien convertían el nitrato y qué especies bacterianas prosperaron bajo cada tratamiento.
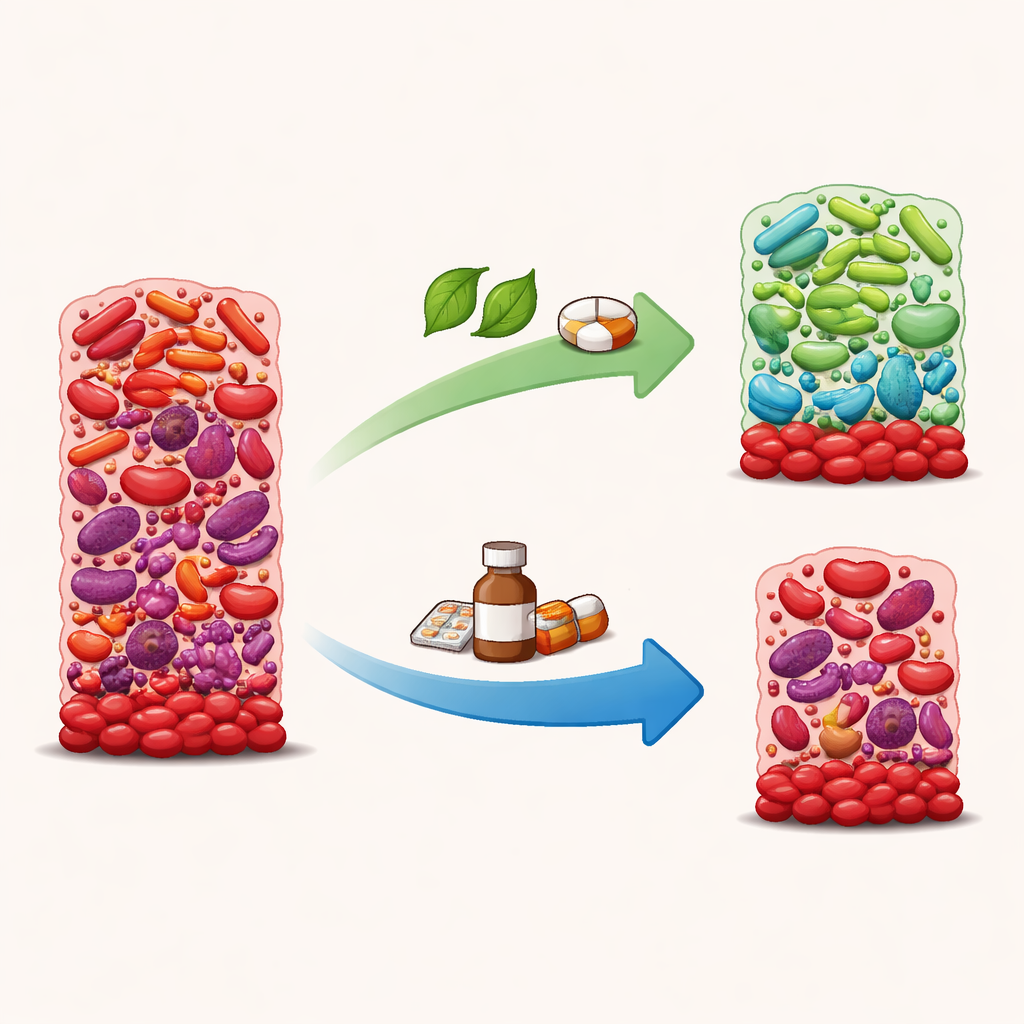
Fármacos que reducen el crecimiento pero pueden empeorar el equilibrio
Dosis bajas de clorhexidina y amoxicilina redujeron el crecimiento del biofilm aproximadamente a la mitad y disminuyeron con fuerza la capacidad de las bacterias para procesar el nitrato. Pero esto no fue una “limpieza” selectiva beneficiosa. La secuenciación del ADN mostró que, en estas condiciones, bacterias asociadas a la salud como Rothia, Gemella y Kingella tendieron a descender, mientras que varias especies vinculadas con la enfermedad periodontal —incluidos Fusobacterium, Treponema y Eubacterium— se mantuvieron o ganaron protagonismo. Un índice que puntúa cuán “enferma” parece una comunidad bajo el microscopio fue más alto con clorhexidina y amoxicilina que con nitrato, lo que sugiere que estos fármacos pueden empujar al biofilm hacia un estado más dañino y desequilibrado aun cuando suprimen el crecimiento total.
Combustible de hojas verdes y un antibiótico más suave
El nitrato contó una historia diferente. Cuando la placa se cultivó con nitrato solo, aumentaron las bacterias que se especializan en transformar el nitrato en productos útiles, como Neisseria y algunas especies de Aggregatibacter. La puntuación de disbiosis cayó en comparación con las condiciones de clorhexidina o amoxicilina, apuntando a una comunidad más saludable. El metronidazol, a un nivel similar al que realmente alcanza los bolsillos gingivales en pacientes, no redujo con fuerza el crecimiento ni el uso de nitrato por sí solo. Pero cuando se combinó con nitrato, pareció inclinar la balanza de forma favorable: especies asociadas a la enfermedad como Fusobacterium y Treponema disminuyeron, mientras que Neisseria y Kingella —usadoras de nitrato— aumentaron. Esta combinación pareció recortar a los peores infractores sin eliminar funciones clave.
Lo que esto significa para el cuidado cotidiano
Para las personas con enfermedad periodontal, estos hallazgos sugieren que “más fuerte” no siempre es “mejor” en lo que respecta a los antimicrobianos. En este modelo de laboratorio, clorhexidina y amoxicilina a baja dosis ralentizaron el crecimiento bacteriano pero también debilitaron una vía natural basada en nitrato que apoya la salud bucal y sistémica, y se asociaron con patrones microbianos más propios de la enfermedad. El nitrato, especialmente cuando se combina con metronidazol, favoreció bacterias vinculadas con encías más sanas y preservó el metabolismo del nitrato. Aunque las bocas reales son más complejas que los platos de laboratorio, este trabajo respalda la idea de estrategias más suaves y respetuosas con el microbioma —como dietas ricas en nitrato y antibióticos seleccionados con cuidado— para manejar la enfermedad de las encías sin socavar las bacterias que nos ayudan a mantenernos bien.
Cita: Moran, S.P., Nadal-Ruiz, M., Mira, A. et al. Combined effects of nitrate and antimicrobial compounds on in vitro subgingival biofilms. Sci Rep 16, 6686 (2026). https://doi.org/10.1038/s41598-026-36588-x
Palabras clave: enfermedad de las encías, microbioma oral, nitrato, enjuague bucal, antibióticos