Clear Sky Science · es
Diagnóstico de la enfermedad de Alzheimer con alta precisión mediante el modelado con redes de Petri de vías de señalización
Por qué la detección temprana de enfermedades cerebrales nos importa a todos
La enfermedad de Alzheimer va erosionando la memoria y la independencia de forma gradual, a menudo mucho antes de que aparezcan síntomas claros. Las herramientas diagnósticas actuales, como las exploraciones cerebrales y las pruebas cognitivas, pueden ser costosas, de difícil acceso y poco sensibles en las fases más tempranas. Este estudio presenta una nueva manera de leer el “cableado” molecular del cuerpo usando muestras de sangre o cerebro y un marco matemático llamado red de Petri. El objetivo es sencillo pero profundo: determinar, con muy alta precisión, si el patrón de actividad génica de una persona se parece más al de una persona sana o al de una con Alzheimer—idealmente lo bastante pronto como para modificar el curso de la enfermedad.
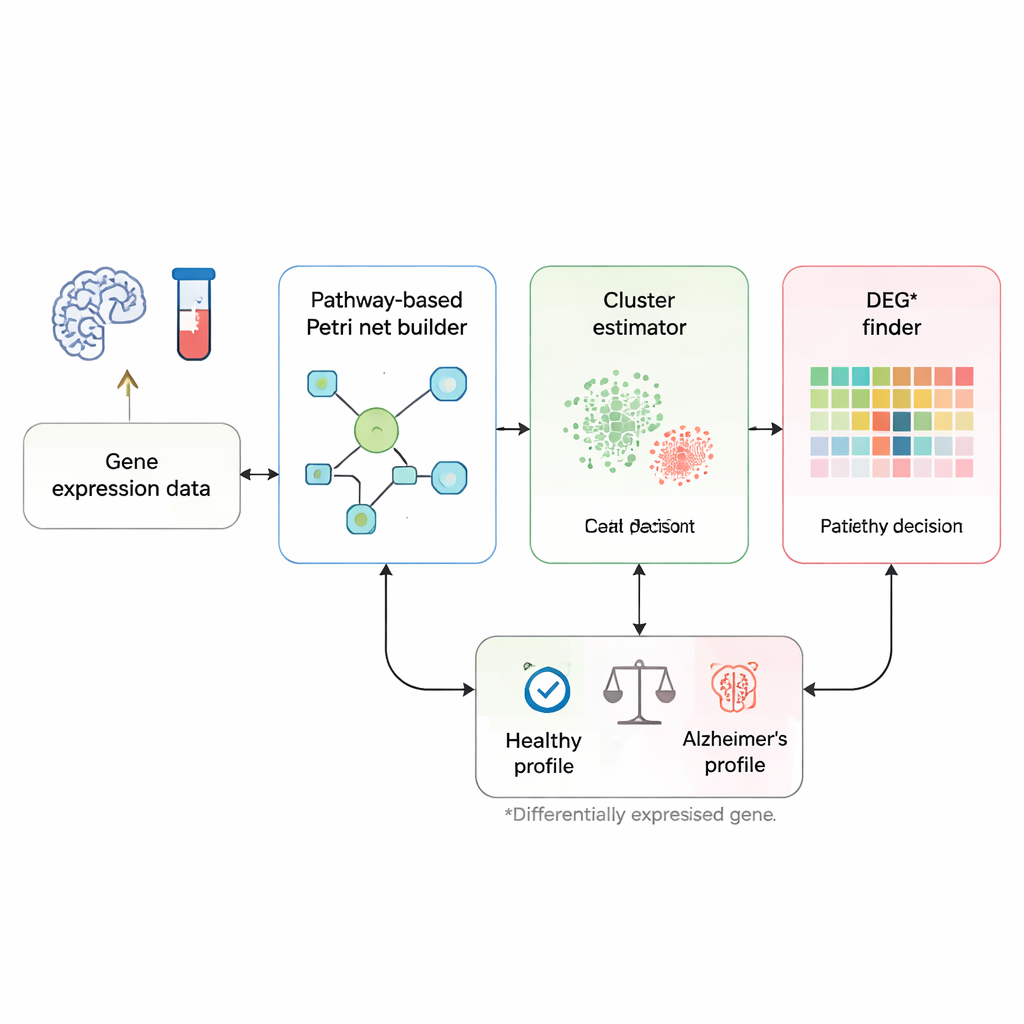
Leer la enfermedad en los “circuitos” de señalización del cuerpo
En lugar de tratar cada gen como un marcador aislado, los investigadores se centran en cómo los genes se comunican entre sí a lo largo de vías biológicas conocidas vinculadas al Alzheimer. Parten de un mapa de la vía cuidadosamente curado de la base de datos KEGG, que enumera genes y las relaciones de activación o inhibición entre ellos. Esa vía se convierte en una red de Petri—una especie de diagrama de flujo donde los círculos representan genes, los rectángulos interacciones y tokens pequeños señales que se mueven por la red. Cuando un token viaja desde un extremo de la vía hasta nodos especiales de “enfermedad”, representa una cadena de eventos génicos que podría conducir a la muerte de las células cerebrales y a la demencia.
De una muestra de sangre a una respuesta de sí o no
El método comienza con perfiles de expresión génica: mediciones que indican cuán activos están miles de genes en la sangre o el tejido cerebral de una persona. Primero, un “estimador de clúster” personalizado compara una nueva muestra con muestras previamente etiquetadas como sanas o de pacientes, enfocándose en genes ya conocidos por diferir entre estos grupos. Para cada uno de esos genes, la herramienta comprueba qué muestras de entrenamiento tienen niveles de expresión más similares y usa una especie de votación por vecindario para dar a la nueva muestra una etiqueta inicial como probablemente sana o probablemente enferma. Este paso conforma dos grupos de trabajo, o clústeres, de muestras: uno que representa patrones típicos sanos y otro que representa patrones típicos de Alzheimer.
Encontrar los genes más reveladores para cada persona
A continuación viene un paso más personalizado. Para una persona dada, el método examina gen por gen para ver dónde sus niveles de expresión realmente destacan. Para cada gen, compara el valor de esa persona con el rango observado en el clúster sano y en el clúster de pacientes, usando estadísticas robustas que restan importancia a la influencia de valores atípicos ruidosos. Si la expresión de un gen se sitúa claramente dentro del rango “enfermo” y fuera del rango sano, se marca como un DEG*, un gen particularmente informativo para ese individuo. A estos genes DEG* se les asignan tokens iniciales en la red de Petri, señalando dónde aparece primero la actividad anómala en el circuito de señalización.
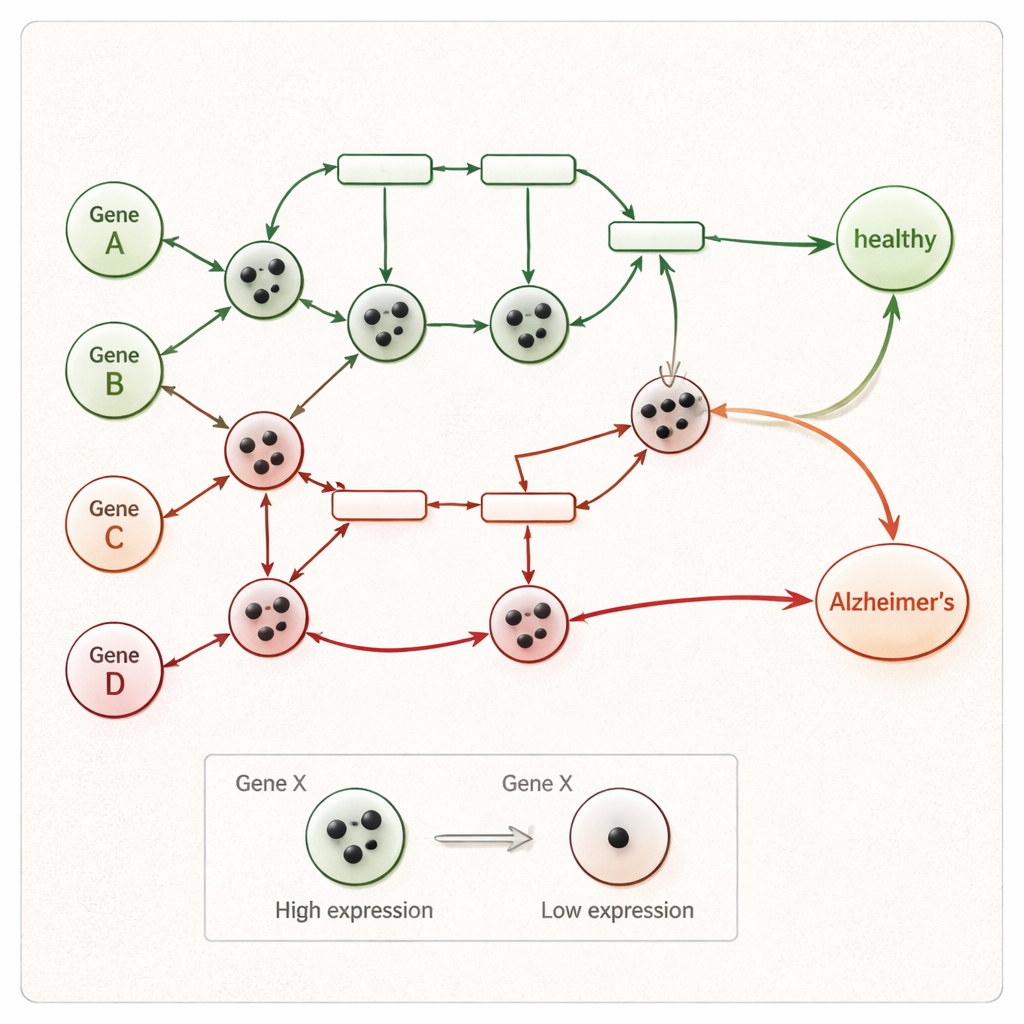
Dejar que la red evolucione hasta llegar a un diagnóstico
Una vez colocados los tokens, la red de Petri se ejecuta paso a paso. En cada paso, cada interacción cuyos genes de entrada tengan suficientes tokens “dispara”, moviendo tokens hacia genes aguas abajo y respetando las reglas de activación e inhibición. Esto continúa hasta que no son posibles más movimientos. Si, al final, al menos un token alcanza el nodo final de enfermedad de la red—que representa procesos como la muerte neuronal o la neurodegeneración—la muestra se clasifica como Alzheimer; si no, se etiqueta como sana. Como cada paso de disparo queda registrado, los investigadores pueden trazar una ruta clara desde la actividad génica inusual de una persona hasta un resultado sano o enfermo, en lugar de depender de una puntuación estadística opaca.
¿Qué tan preciso es este enfoque en la práctica?
El equipo probó su marco en varios grandes conjuntos de datos públicos de expresión génica tanto de sangre como de tejido cerebral. En dos conjuntos de datos de sangre ampliamente usados, su método distinguió correctamente a pacientes con Alzheimer de individuos sanos en aproximadamente el 98–99% de los casos, superando con creces enfoques previos de aprendizaje automático que a menudo alcanzaban solo entre el 65 y el 81% de precisión. También mostraron un rendimiento sólido en conjuntos de datos adicionales de cerebro y sangre, incluso cuando el número de muestras era pequeño. Es importante destacar que, a diferencia de muchos competidores, su método no descartó muestras ruidosas o difíciles de interpretar; en su lugar, usa su diseño interno para manejar la variabilidad manteniendo todos los datos en el análisis.
Qué significa esto para las futuras pruebas de Alzheimer
Para un público no especializado, el mensaje principal es que el estudio convierte la genética compleja y los diagramas de vías en un proceso de decisión claro y por pasos que puede leer los signos tempranos de la enfermedad de Alzheimer a partir de una muestra sencilla, potencialmente incluso solo de sangre. Al modelar cómo trabajan juntos los genes anómalos, no solo cómo se comportan aisladamente, el marco de la red de Petri ofrece tanto alta precisión diagnóstica como una “historia” comprensible de cómo la enfermedad puede desarrollarse en cada persona. Aunque este trabajo sigue siendo investigación y aún no es una prueba clínica, apunta hacia herramientas futuras que podrían detectar el Alzheimer antes, orientar opciones de tratamiento y, eventualmente, adaptarse a otras enfermedades cerebrales y cánceres usando la misma idea subyacente.
Cita: Ebrahimian, H., Asadzadeh, F., Rahgozar, M. et al. Diagnosis of Alzheimer’s disease with high accuracy via Petri net modeling of signaling pathways. Sci Rep 16, 6457 (2026). https://doi.org/10.1038/s41598-026-36585-0
Palabras clave: Diagnóstico de Alzheimer, expresión génica, vías de señalización, modelado con redes de Petri, biomarcadores en sangre