Clear Sky Science · es
Construcción y validación inicial de una red génica clave para la resistencia a la progesterona en el cáncer de endometrio basada en un cribado genómico con CRISPR
Por qué algunos cánceres uterinos dejan de responder a las hormonas
Para muchas personas con cáncer de endometrio en etapas tempranas que desean conservar la fertilidad, píldoras hormonales que imitan la progesterona natural pueden reducir los tumores mientras preservan el útero. Sin embargo, hasta un tercio de estos cánceres nunca responden o desarrollan resistencia rápidamente, obligando a los pacientes a optar por cirugía o tratamientos más agresivos. Este estudio utiliza una potente herramienta de edición genética para mapear qué genes hacen que las células del cáncer de endometrio ignoren la progesterona, apuntando hacia futuras pruebas y fármacos que podrían prolongar la eficacia de esta terapia.
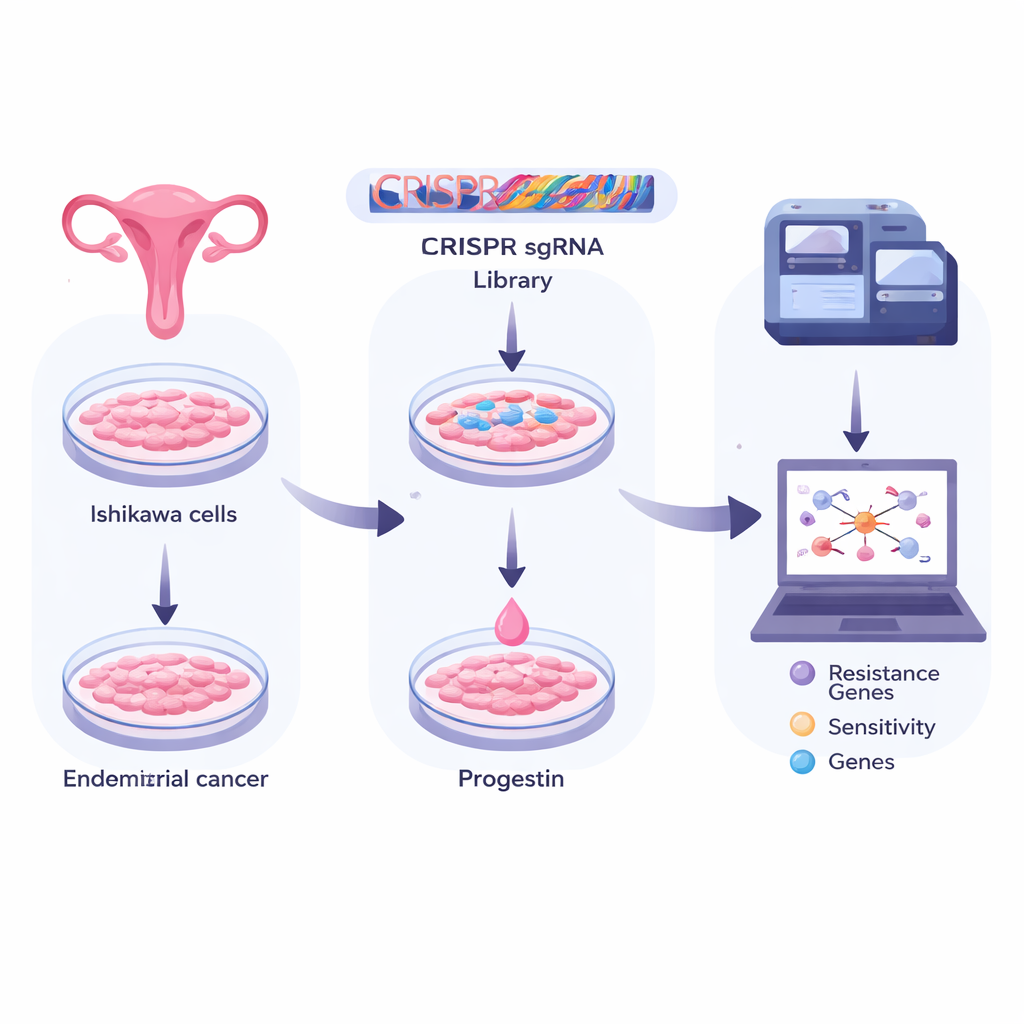
Usando tijeras genéticas para explorar todo el genoma
Los investigadores trabajaron con células Ishikawa, un modelo ampliamente empleado del cáncer de endometrio. Infectaron millones de estas células con una biblioteca de “tijeras” CRISPR, cada una programada para apagar un gen humano distinto. Así crearon una enorme población en la que, en principio, cada célula tenía un gen único desactivado. El equipo dividió luego las células en grupos: uno congelado como línea de base, otro expuesto solo a un disolvente inocuo y otro tratado durante muchos días con una progesterona sintética común (medroxiprogesterona, o MPA). Mediante secuenciación profunda de las etiquetas CRISPR supervivientes en cada grupo, pudieron ver qué inactivaciones génicas ayudaban a las células a sobrevivir o morir bajo el tratamiento con progesterona.
Separando genes que ayudan o dificultan la respuesta al fármaco
Analizar este aluvión de datos requirió estadísticas sofisticadas. El equipo aplicó dos métodos complementarios, RRA y MLE, para clasificar los genes según cuánto protegían a las células de la progesterona (genes de resistencia) o cuánto las hacían más propensas a morir (genes de sensibilidad). Encontraron cientos de candidatos en cada dirección. Muchos de estos genes se agruparon en vías relacionadas con la replicación y reparación del ADN, la síntesis y el procesamiento del ARN y el metabolismo celular general. En otras palabras, la maquinaria básica que permite a las células leer, mantener y actuar sobre su información genética parece estar estrechamente vinculada a si las células del cáncer de endometrio obedecen la señal de la progesterona de “dejar de crecer”.
Reduciendo la lista hasta los actores más importantes
Para evitar seguir pistas falsas, los científicos cotejaron los candidatos obtenidos por CRISPR con un conjunto de datos anterior de su laboratorio, en el que habían comparado células cancerosas ordinarias con una cepa que había desarrollado resistencia a la progesterona con el tiempo. Al buscar genes que aparecieran en ambas pantallas y mostraran cambios consistentes, destilaron la lista hasta cinco genes que parecen promover la resistencia y veinte que parecen combatirla. Bases de datos públicas sobre cáncer mostraron que muchos de los genes que bloquean la resistencia están más activos en el tipo más común de cáncer de endometrio, mientras que varios genes que promueven la resistencia se correlacionan con peores resultados en pacientes, lo que sugiere que estas señales importan en tumores reales, no solo en platos de cultivo.
Probando genes clave en células y en ratones
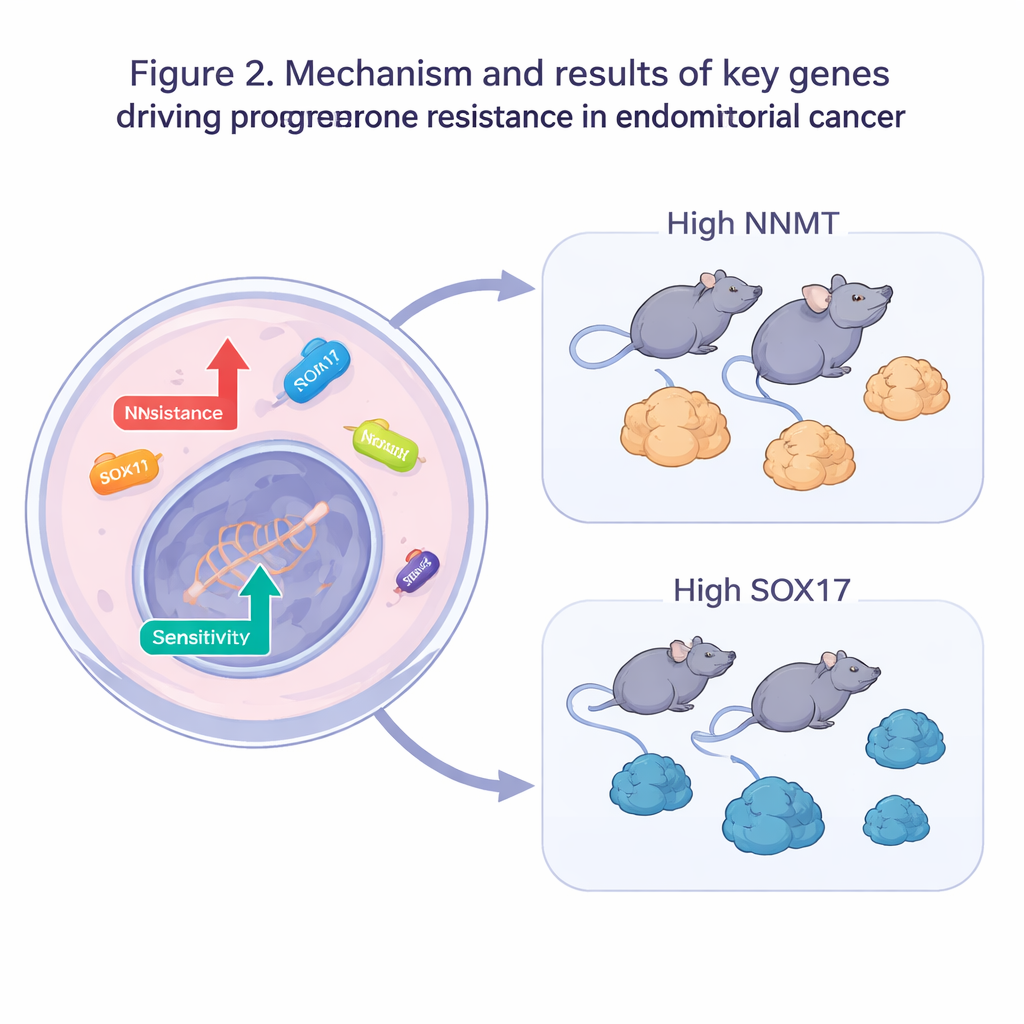
El equipo pasó entonces de los grandes datos a experimentos prácticos. En células resistentes a la progesterona, silenciaron cada uno de los cinco genes sospechosos de promover la resistencia o potenciaron los cinco genes sospechosos de conferir sensibilidad. Cuando estas células modificadas se expusieron a progesterona, muchas más murieron y se necesitaron dosis mucho más bajas del fármaco para frenar su crecimiento, confirmando que alterar genes individuales podía restaurar la sensibilidad hormonal. Dos genes destacaron: NNMT, implicado en el metabolismo celular, y SOX17, un gen que ayuda a controlar cómo se desarrollan y comportan las células. En modelos tumorales en ratones, aumentar la expresión de NNMT hizo que los tumores respondieran menos a la progesterona, mientras que incrementar SOX17 hizo que tumores resistentes se redujeran más con el mismo tratamiento.
Qué podrían significar estos hallazgos para los pacientes
En términos sencillos, el estudio construye un primer “diagrama de cableado” de cómo las células del cáncer de endometrio deciden si atender a la progesterona. Sugiere que la resistencia no se reduce únicamente a la pérdida del receptor de progesterona, sino que implica cambios más profundos en el manejo del ADN y el ARN y en genes de control clave como NNMT y SOX17. En el futuro, pruebas en sangre o tejido que evalúen esta red génica podrían ayudar a los médicos a predecir quién se beneficiará de la terapia hormonal que preserva la fertilidad. Aún más prometedor, fármacos que atenúen genes de resistencia o potencien genes de sensibilidad podrían combinarse algún día con la progesterona para mantener esta opción de tratamiento más suave eficaz para más personas y durante más tiempo.
Cita: Li, X., Wang, S., Qiu, Z. et al. Construction and initial validation of key gene network for progesterone resistance in endometrial cancer based on genome-wide CRISPR screening. Sci Rep 16, 8030 (2026). https://doi.org/10.1038/s41598-026-36534-x
Palabras clave: cáncer de endometrio, resistencia a la progesterona, cribado CRISPR, redes génicas, terapia hormonal