Clear Sky Science · es
Las modificaciones m6A del huésped moldean la microbiota que impulsa la ferroptosis específica de células como vía causal de las enfermedades respiratorias crónicas
Por qué tus microbios importan para tus pulmones
Los problemas respiratorios crónicos como el asma y la enfermedad pulmonar obstructiva crónica (EPOC) suelen atribuirse al tabaquismo, la contaminación o las alergias. Este estudio plantea otro factor, menos obvio: los billones de microbios que viven en nuestro intestino y en la piel. Usando datos genéticos a gran escala, los autores muestran que ciertos microbios podrían no limitarse a acompañar la enfermedad pulmonar, sino contribuir a causarla —actuando a través de cambios químicos sutiles en nuestras células y de una forma de daño celular impulsada por el hierro. Comprender esta red oculta podría con el tiempo abrir vías para prevenir o tratar las enfermedades respiratorias crónicas mediante la modificación de nuestros microbios y sus rutas moleculares hacia estados más saludables.
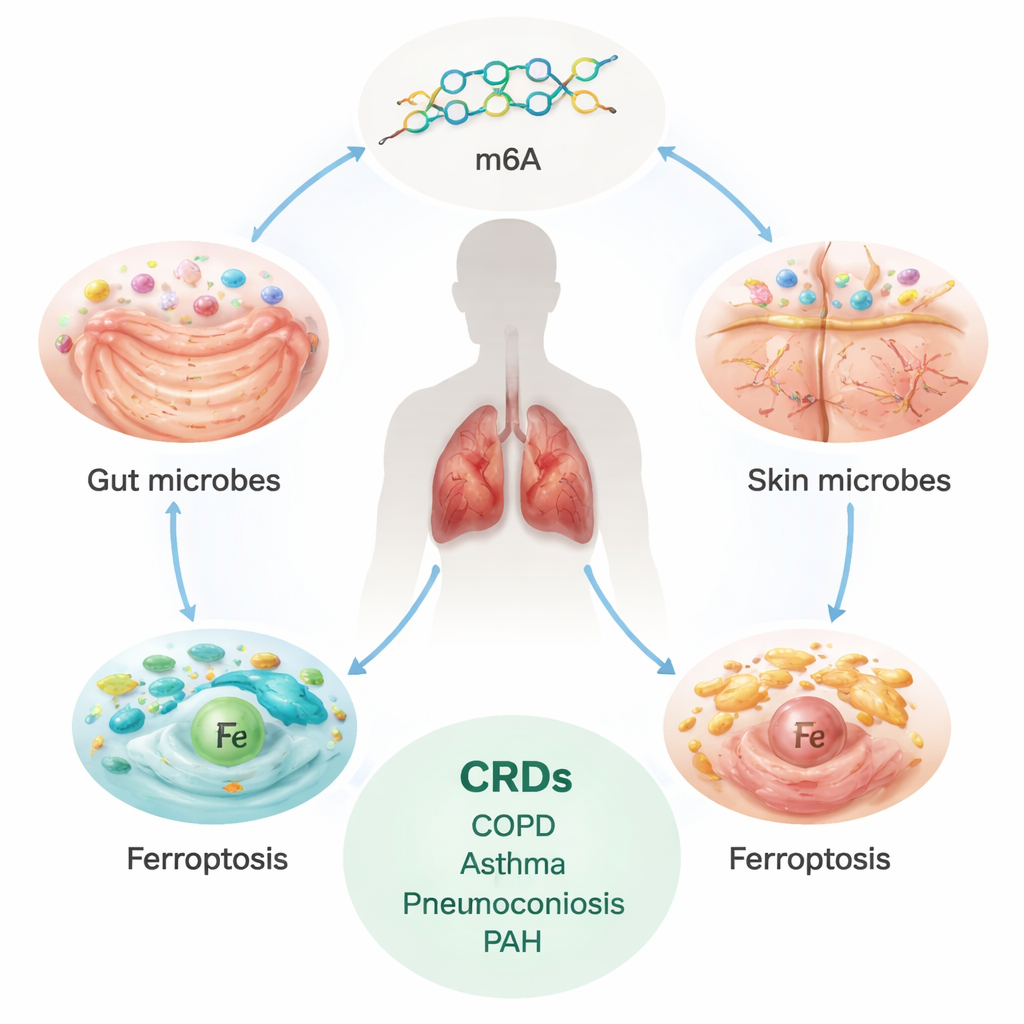
La carga oculta de las enfermedades pulmonares crónicas
Las enfermedades respiratorias crónicas, incluidas la EPOC, el asma, la enfermedad pulmonar intersticial (EPI), la neumoconiosis y la hipertensión arterial pulmonar (HAP), afectan a cientos de millones de personas en todo el mundo y causan millones de muertes cada año. Estas afecciones suelen progresar de forma lenta pero constante, provocando cicatrización o remodelado de los pulmones y los vasos sanguíneos y dejando a las personas con dificultad para respirar. Los tratamientos actuales gestionan principalmente los síntomas; no detienen ni revierten por completo el daño subyacente. Eso ha impulsado a los científicos a buscar causas más profundas y fundamentales, especialmente aquellas que podrían modificarse antes de que la enfermedad se vuelva grave.
Vecinos microbianos en el intestino y la piel
Hoy sabemos que el intestino y la piel albergan comunidades microbianas complejas que ayudan a educar el sistema inmunitario, moldear el metabolismo y mantener las defensas de barrera. Pero, ¿estos microbios están realmente impulsando la enfermedad pulmonar o simplemente cambian a medida que las personas enferman? Para desenredar causa y efecto, los investigadores emplearon un método llamado randomización mendeliana, que aprovecha las diferencias genéticas naturales entre las personas como una especie de “experimento” de por vida. Combinaron datos genéticos sobre cientos de tipos de microbios intestinales y cutáneos con datos sobre cinco grandes enfermedades pulmonares crónicas procedentes de estudios europeos de gran tamaño, probando si las tendencias hereditarias a tener niveles más altos o más bajos de microbios concretos se relacionan con el riesgo de cada enfermedad.
Microbios que ayudan o perjudican a los pulmones
El análisis identificó docenas de microbios intestinales que aumentaban o disminuían el riesgo de cada enfermedad respiratoria, a menudo con patrones específicos según la enfermedad. Por ejemplo, ciertas bacterias intestinales parecían proteger frente a la EPOC, el asma o la HAP, mientras que otras aumentaban las probabilidades de EPI o EPOC. Los microbios de la piel mostraron vínculos más modestos pero aún detectables, con algunas especies asociadas a mayor riesgo y otras a menor riesgo en distintas condiciones. El equipo también invirtió la dirección del análisis y encontró que el riesgo genético para EPOC, asma y otras enfermedades pulmonares, a su vez, predecía cambios tanto en la microbiota intestinal como en la cutánea. Este tráfico bidireccional sugiere un bucle de retroalimentación: los microbios pueden influir en la enfermedad pulmonar, y la enfermedad pulmonar puede remodelar nuestros ecosistemas microbianos.
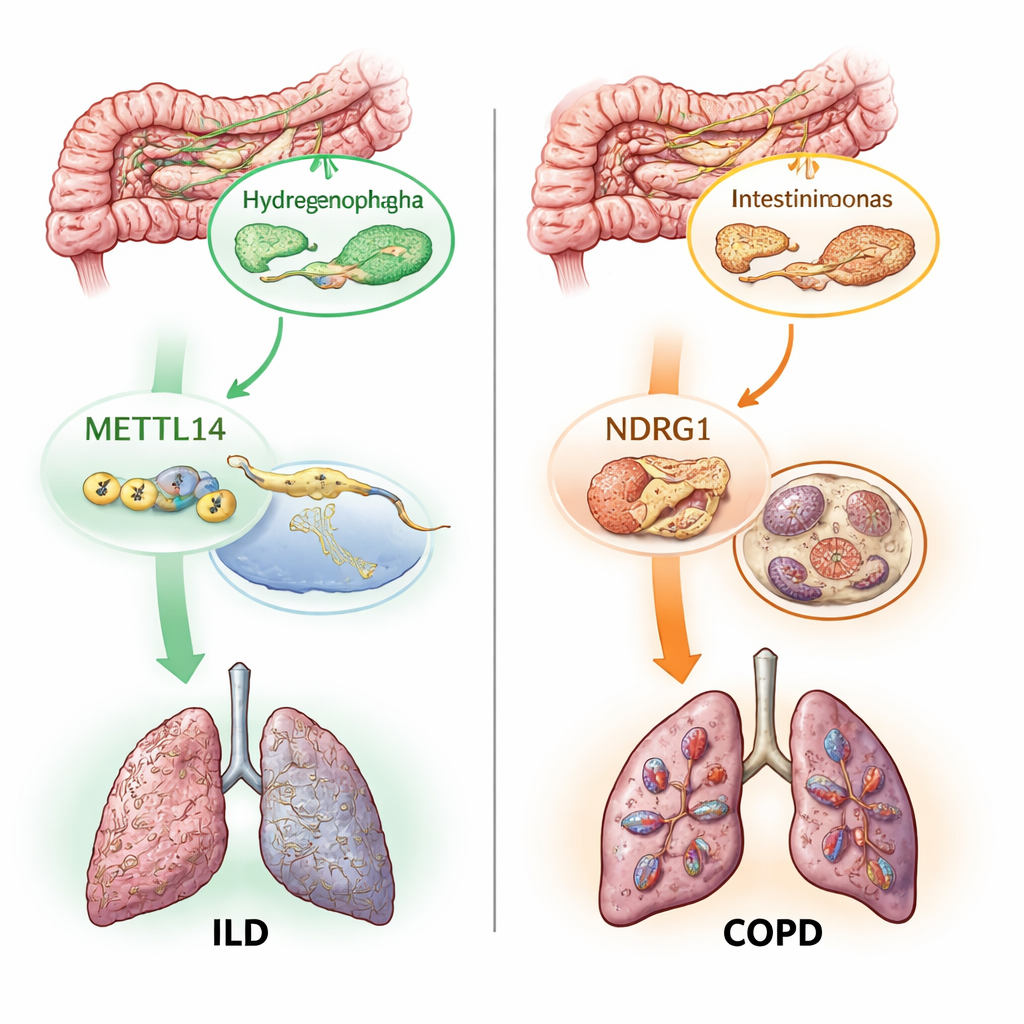
Dos interruptores moleculares: marcas de ARN y muerte celular impulsada por hierro
Más allá de mapear qué microbios importan, los autores preguntaron cómo estos socios microscópicos podrían influir en los tejidos pulmonares. Se centraron en dos procesos moleculares ya sospechosos de contribuir al daño pulmonar. El primero, llamado modificación m6A, es una pequeña etiqueta química añadida al ARN que ajusta cómo se activan o silencian los genes. El segundo, la ferroptosis, es una forma de muerte celular dependiente del hierro impulsada por una oxidación descontrolada de los lípidos en las membranas celulares. Usando proxys genéticos para 19 genes relacionados con m6A y cientos de genes relacionados con la ferroptosis, probaron si las variaciones en estas vías se relacionan causalmente con la enfermedad pulmonar. Encontraron que un gen escritor de m6A, METTL14, se asociaba con menor riesgo de EPI, y varios genes de la ferroptosis, incluido NDRG1, se relacionaban con mayor riesgo de EPOC, EPI y asma.
Conectando los puntos: de microbios a células a enfermedad
La parte más novedosa del trabajo fue trazar cómo encajan estas piezas en cadenas de causa y efecto. Los análisis de mediación estadística sugirieron que parte del efecto protector de METTL14 sobre la EPI opera a través de cambios que induce en un microbio intestinal particular llamado Hydrogenophaga. En otra vía, una bacteria intestinal específica, Intestinimonas massiliensis, pareció influir en el riesgo de EPOC en parte activando NDRG1 y el programa de muerte por ferroptosis. El equipo comprobó luego datos de tejido pulmonar humano y confirmó que tanto METTL14 como NDRG1 se expresan de forma diferente en muestras enfermas frente a sanas. Finalmente, usando mapas genéticos de célula única de células inmunitarias, localizaron el efecto dañino de NDRG1 sobre la EPOC a un subconjunto de células inmunes, un tipo de monocito, lo que sugiere que futuros fármacos dirigidos a este gen podrían necesitar actuar de forma específica en ciertos tipos celulares.
Qué implica esto para tratamientos futuros
Para el público no especializado, el mensaje clave es que la salud pulmonar no depende solo de lo que respiramos, sino también de los microbios que viven en nosotros y de los interruptores moleculares que activan dentro de nuestras células. Este estudio no puede probar cada paso experimentalmente y está limitado principalmente a personas de ascendencia europea, pero ofrece pistas genéticas sólidas de que los microbios intestinales, marcas del ARN como la m6A y la muerte celular impulsada por el hierro conforman una vía conectada que conduce al daño pulmonar crónico. A largo plazo, esta línea de investigación podría inspirar nuevas estrategias que combinen terapias basadas en el microbioma con fármacos dirigidos a METTL14, NDRG1 o la ferroptosis, con el objetivo no solo de aliviar síntomas sino de interrumpir los circuitos biológicos que hacen progresar las enfermedades respiratorias crónicas.
Cita: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
Palabras clave: microbioma intestinal, enfermedad pulmonar crónica, asma y EPOC, epigenética del ARN, vías de muerte celular