Clear Sky Science · es
Asociación del estado mutacional de RAS con resultados clínicos en cáncer colorrectal metastásico tratado con trifluridina/tipiracilo o regorafenib
Por qué este estudio importa a pacientes y familias
El cáncer colorrectal metastásico—cáncer de colon o recto que se ha diseminado—es una de las principales causas de muerte por cáncer en todo el mundo. Cuando los fármacos estándar dejan de funcionar, pacientes y médicos se enfrentan a decisiones difíciles sobre qué probar a continuación. Este estudio plantea una pregunta muy práctica: ¿pueden pruebas genéticas sencillas en el tumor ayudar a emparejar a los pacientes con dos medicamentos de uso extendido en última línea, trifluridina/tipiracilo y regorafenib, para que las personas vivan más tiempo y con mejor calidad de vida?
Mirar los genes para orientar decisiones de tratamiento difíciles
La atención oncológica moderna suele comenzar con el análisis del ADN del tumor. Un conjunto clave de genes, llamado RAS, ayuda a controlar cómo crecen y se dividen las células. Las alteraciones, o mutaciones, en estos genes pueden hacer que las células cancerosas crezcan de forma descontrolada y resistan ciertos fármacos. Los investigadores revisaron historias clínicas de 263 adultos con cáncer colorrectal metastásico tratados en un centro oncológico de Taiwán entre 2018 y 2023. Todos ya habían recibido quimioterapia estándar y terapias dirigidas y luego se les administró trifluridina/tipiracilo solo, trifluridina/tipiracilo más otro fármaco dirigido, o regorafenib. Antes de iniciar estos tratamientos, a cada paciente se le analizaron los genes RAS y se clasificó en uno de tres grupos: RAS normal (tipo salvaje RAS), una mutación común en un punto del gen KRAS (KRAS G12), u otras mutaciones RAS menos frecuentes.
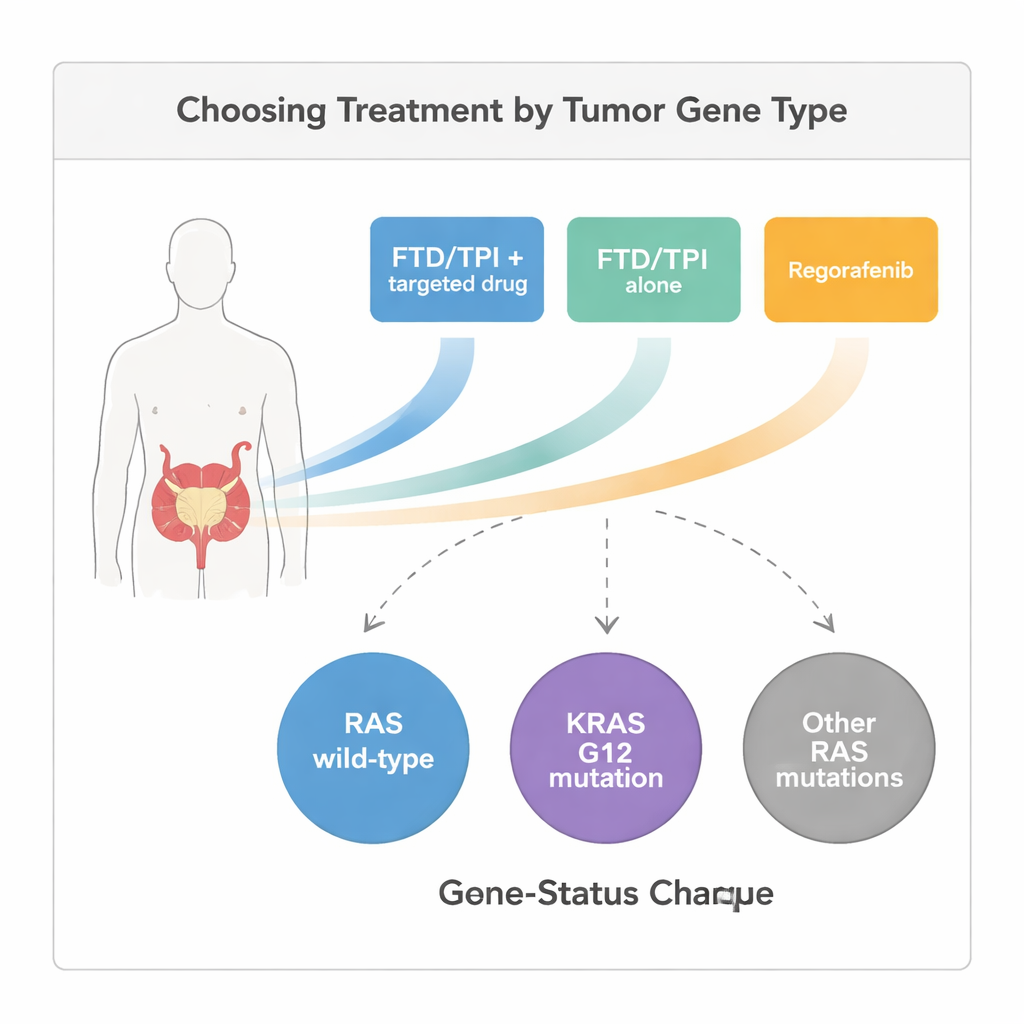
Tres rutas de tratamiento en el mundo real
La trifluridina/tipiracilo es una píldora de quimioterapia, y el regorafenib es una píldora que bloquea varias señales relacionadas con el crecimiento en las células tumorales y los vasos sanguíneos. Algunos pacientes en este estudio recibieron trifluridina/tipiracilo sola, mientras que otros la tomaron en combinación con un fármaco dirigido adicional que bloquea los vasos sanguíneos tumorales o las señales de crecimiento. Como se trató de una revisión del mundo real y no de un ensayo aleatorizado, los médicos eligieron el tratamiento según los efectos secundarios previos de cada paciente, la carga tumoral y su condición general. Los investigadores monitorizaron entonces cuánto tiempo vivieron los pacientes sin que su cáncer empeorara (supervivencia libre de progresión) y cuánto tiempo vivieron en total, así como con qué frecuencia los tumores se redujeron o, al menos, dejaron de crecer.
Las diferencias genéticas condicionan qué fármaco funciona mejor
En todo el conjunto, la combinación de trifluridina/tipiracilo más un fármaco dirigido fue claramente la que mejores resultados ofreció. Los pacientes con esta combinación habitualmente estuvieron alrededor de cinco meses antes de que su enfermedad empeorara y vivieron una mediana de algo más de 15 meses desde el inicio del tratamiento—más que quienes recibieron trifluridina/tipiracilo sola o regorafenib. Los tumores también tendieron a reducirse o estabilizarse con mayor probabilidad con la combinación. Cuando los investigadores examinaron con más detalle los grupos según RAS, emergieron patrones importantes. Para los pacientes cuyos tumores tenían RAS normal o alguna de las mutaciones RAS menos frecuentes, la trifluridina/tipiracilo sola siguió superando al regorafenib en términos de supervivencia. Sin embargo, para los pacientes cuyos tumores presentaban la mutación común KRAS G12, el regorafenib ofreció mejor supervivencia que la trifluridina/tipiracilo sola, aunque el tratamiento combinado seguía siendo el mejor de todos.
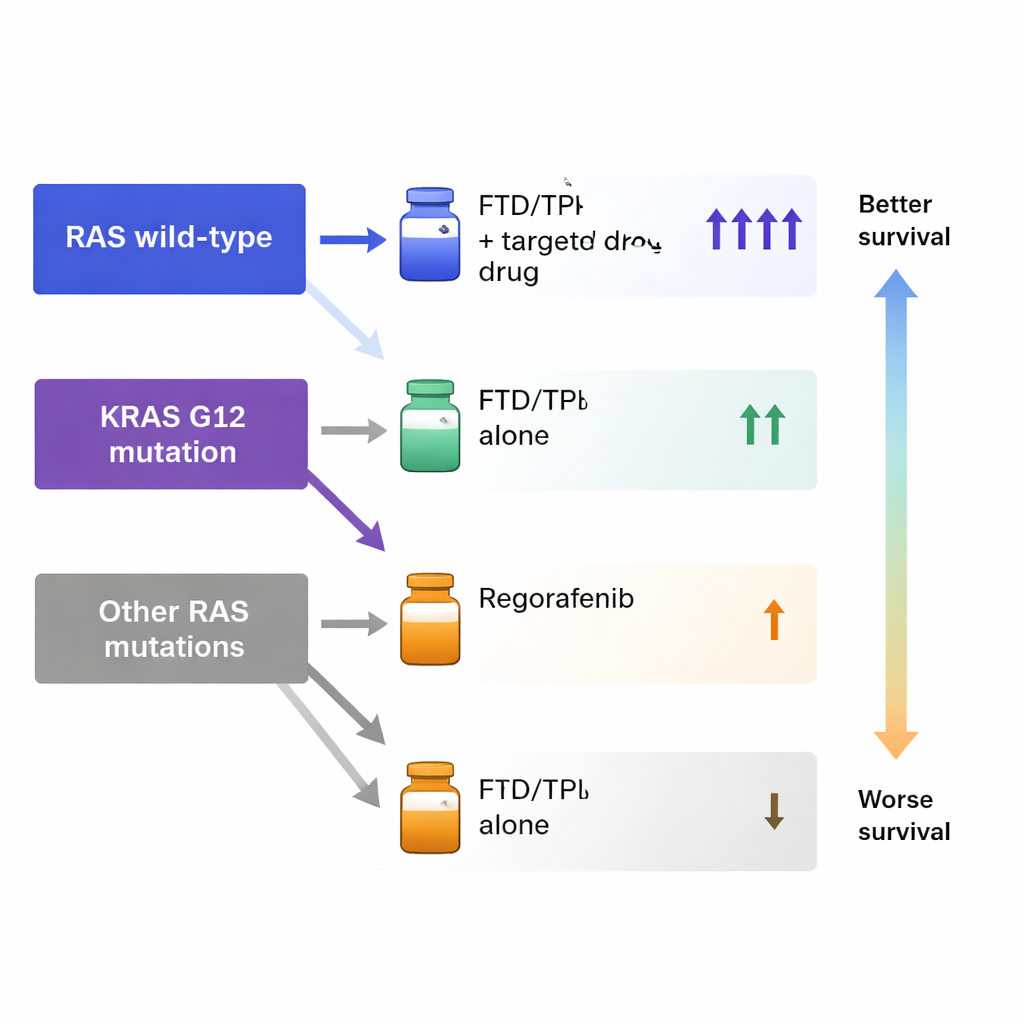
Qué significa esto para la oncología de precisión
Estos hallazgos sugieren que una prueba genética relativamente simple—ya realizada de forma rutinaria en muchos pacientes con cáncer colorrectal—podría ayudar a orientar la elección entre dos difíciles opciones de tratamiento en fase avanzada. En lugar de considerar la trifluridina/tipiracilo y el regorafenib como intercambiables tras el fracaso de la terapia estándar, los médicos podrían favorecer la trifluridina/tipiracilo, especialmente en combinación con un fármaco dirigido, para la mayoría de los pacientes. Para el subgrupo con mutaciones KRAS G12, el regorafenib puede ser la mejor opción como fármaco único si la terapia combinada no es posible. El estudio también sugiere que otras características clínicas, como la estadificación original del cáncer y ciertos marcadores de reparación del ADN, podrían afinar aún más estas decisiones.
Mensaje clave para no especialistas
Para las personas que viven con cáncer colorrectal avanzado, esta investigación ofrece una noticia cautamente esperanzadora: la huella genética de un tumor, en particular las alteraciones en los genes RAS, puede ayudar a indicar el fármaco con mayor probabilidad de ganar tiempo. En este estudio, añadir un fármaco dirigido a la trifluridina/tipiracilo proporcionó la supervivencia más larga para casi todos los pacientes, independientemente de su estado RAS. Entre quienes tenían la mutación específica KRAS G12, el regorafenib pareció una opción más segura que la trifluridina/tipiracilo sola. Dado que se trató de un análisis retrospectivo y de un solo centro, sus resultados deben confirmarse en ensayos aleatorizados más grandes. Aun así, proporciona una hoja de ruta práctica basada en el genoma que los médicos pueden considerar hoy al personalizar el tratamiento de última línea para el cáncer colorrectal metastásico.
Cita: Hsieh, MC., Rau, KM., Liu, KW. et al. Association of RAS mutational status with clinical outcomes in metastatic colorectal cancer treated with trifluridine/tipiracil or regorafenib. Sci Rep 16, 5294 (2026). https://doi.org/10.1038/s41598-026-36509-y
Palabras clave: cáncer colorrectal metastásico, mutación RAS, KRAS G12, trifluridina tipiracilo, regorafenib