Clear Sky Science · es
La fosforilación de NEK7 sobre cortactina modula la capacidad migratoria de células que expresan EML4-ALK V3
Por qué importa el movimiento celular en el cáncer de pulmón
El cáncer se vuelve amenazante cuando las células aprenden a desplazarse. En el cáncer de pulmón no microcítico, algunos tumores se diseminan por el cuerpo más rápido que otros, y un culpable es una proteína de fusión defectuosa llamada EML4-ALK. Una versión concreta, conocida como variante 3 (V3), se asocia con una enfermedad especialmente agresiva y respuestas pobres a fármacos dirigidos. Este estudio plantea una pregunta básica pero vital: ¿qué permite a estas células cancerosas impulsadas por V3 cambiar de forma y moverse con tanta eficacia, y podemos identificar las piezas moleculares que lo hacen posible?
Una variante de cáncer de pulmón hiper-migratoria
Los médicos saben desde hace tiempo que solo una minoría de los cánceres de pulmón llevan la fusión EML4-ALK, pero los pacientes cuyos tumores expresan la forma V3 suelen evolucionar peor que los que tienen otras variantes. Al microscopio, las células que expresan V3 se ven diferentes: en vez de ser compactas y en forma de adoquín, se estiran en formas largas y delgadas con protrusiones extendidas, semejando células en movimiento. Trabajos anteriores mostraron que este comportamiento depende de dos enzimas, NEK9 y NEK7, que actúan como interruptores moleculares en la célula. Sin embargo, los dianas aguas abajo cruciales de esos interruptores —las que remodelan directamente el armazón interno de la célula— no se comprendían bien.
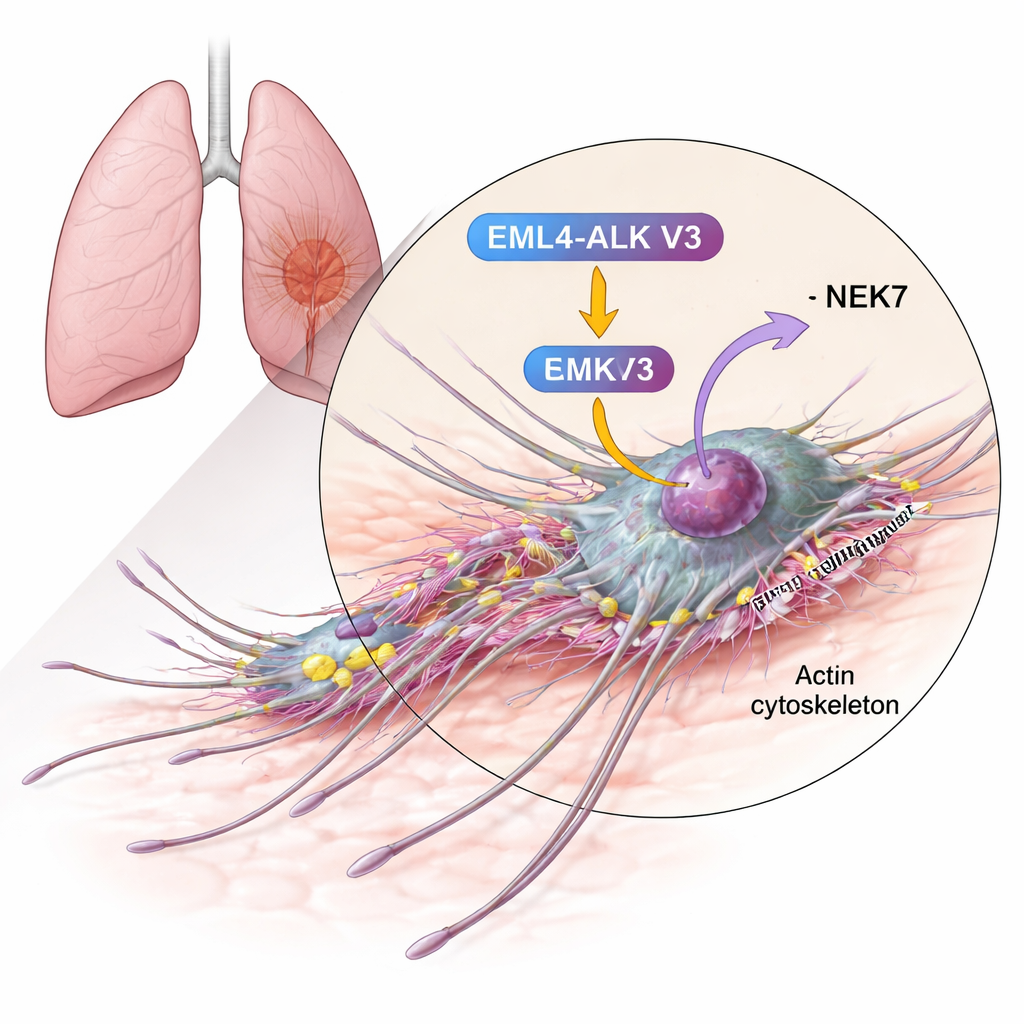
Vinculando una proteína de movimiento con una fusión agresiva
Los autores se centraron en la cortactina, una proteína ya conocida por estar abundante en muchos cánceres invasivos y por contribuir a construir las redes de filamentos de actina que empujan la membrana celular hacia delante. Mediante pruebas bioquímicas, demostraron que la cortactina puede ser modificada químicamente (fosforilada) por NEK6 y, con mayor intensidad, por NEK7. Las enzimas añaden grupos fosfato a residuos de serina específicos dentro de la región de unión a actina de la cortactina —justo el tramo que agarra las fibras de actina y estabiliza redes ramificadas. Cuando NEK7 estaba presente, la cortactina presentaba más grupos fosfato y en más sitios que con NEK6, lo que sugiere que NEK7 es el regulador principal en este contexto.
Apagar la cortactina frena la migración de células cancerosas
Para ver qué hace la cortactina en células vivas, los investigadores la depletaron usando interferencia por ARN en células diseñadas para activar NEK9 o NEK7, o para expresar la propia EML4-ALK V3. En los tres escenarios, las llamativas formas alargadas y mesenquimales colapsaron: las células se volvieron más planas y redondeadas, perdieron sus protrusiones largas y, en su lugar, formaron gruesas y rectas “fibras de tensión” de actina que cruzaban la célula. Varios ensayos de migración —desde cerrar “heridas” artificiales en una capa celular hasta rastrear células individuales y medir el movimiento hacia una señal química— mostraron que sin cortactina, estas células altamente móviles se ralentizaban dramáticamente. Efectos similares se observaron en líneas celulares de cáncer de pulmón establecidas que portan de forma natural EML4-ALK V3, subrayando la relevancia clínica de la vía.
Filamentos finos y puntas afiladas en el frente
Imágenes de alta resolución en células epiteliales bronquiales revelaron un panorama aún más detallado. Las células que expresan EML4-ALK V3 producían muchas extensiones finas, a veces ramificadas, similares a filopodios que salpicaban sus protrusiones. En las puntas y puntos de ramificación de estas estructuras, cortactina, EML4-ALK V3, NEK7 y una forma fosforilada de cortactina se agrupaban juntos. Esta estrecha colocalización sugiere un “sitio de construcción” focalizado donde NEK7 modifica la cortactina para construir y mantener las redes de actina finamente ramificadas que ayudan a dirigir la célula. Cuando se eliminó la cortactina, estas extensiones intrincadas desaparecieron y el crecimiento invasivo desde esferoides tumorales 3D hacia un gel circundante se redujo notablemente.
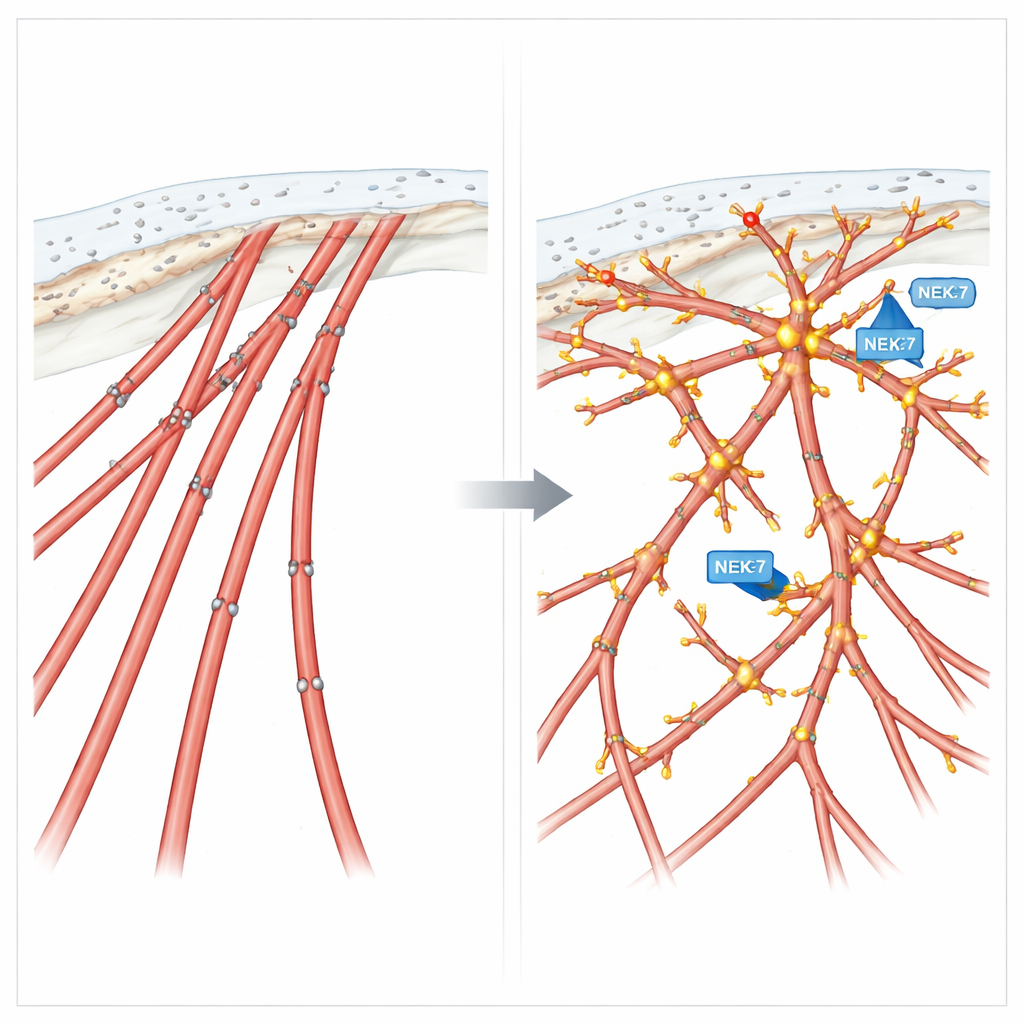
La fosforilación como un regulador de la migración
Para probar cómo estas marcas químicas en la cortactina influyen en el comportamiento, el equipo creó dos versiones diseñadas de la proteína: una forma fosfo-mimética que imita una fosforilación constante en cuatro sitios clave, y una forma fosfo-nula que no puede fosforilarse ahí. Las células que expresaban la versión mimética desarrollaron abundantes extensiones tipo filopodio y mostraron una migración dirigida potenciada, similar a las células con NEK7 activo o EML4-ALK V3. En contraste, las células que expresaban la versión no fosforilable formaron fibras de tensión rígidas, perdieron esas finas extensiones y se desplazaron de forma rápida pero sin rumbo —buenas para vagar, malas para seguir una señal. En cultivos tridimensionales, esta cortactina fosfo-nula impulsó brotes invasivos desorganizados en lugar de guiados con precisión.
Qué significa esto para entender —y atacar— la diseminación
En términos sencillos, el estudio muestra que la agresiva variante de cáncer de pulmón EML4-ALK V3 secuestra un sistema normal de conformación celular. Al activar NEK7, provoca que la cortactina se fosforile en sitios específicos dentro de su región de unión a la actina. Esta modificación afina la función de la cortactina para que pueda construir estructuras de actina finamente ramificadas y extensiones tipo filopodio que sostienen una migración e invasión celular rápida y dirigida. Interrumpir la cortactina o su fosforilación invierte el sistema: las células o apenas se mueven o se desplazan de forma caótica y sin dirección. Estos hallazgos revelan una cadena molecular concreta —desde una fusión que impulsa el cáncer, pasando por NEK7, hasta la cortactina y el citoesqueleto de actina— que ayuda a explicar por qué algunos cánceres de pulmón metastatizan con tanta eficacia, y señalan vías potenciales para ralentizar o desorientar su movimiento.
Cita: Richardson, E.L., Knebel, A., Straatman, K.R. et al. NEK7 phosphorylation of cortactin modulates the migratory capacity of cells expressing EML4-ALK V3. Sci Rep 16, 6407 (2026). https://doi.org/10.1038/s41598-026-36484-4
Palabras clave: cáncer de pulmón no microcítico, EML4-ALK V3, migración celular, cortactina, citosqueleto de actina