Clear Sky Science · es
ATF4 regula la disfunción mitocondrial y la mitofagia, contribuyendo a la apoptosis del endotelio corneal
Por qué la ventana del ojo puede volverse turbia
Nuestras córneas —las claras ventanas frontales del ojo— se mantienen transparentes gracias a una capa delgada y trabajadora de células en su superficie interna. En la distrofia endotelial corneal de Fuchs (FECD), millones de personas pierden lentamente estas células, lo que provoca hinchazón, visión borrosa y, con frecuencia, trasplantes de córnea. Este estudio formula una pregunta básica pero crucial: ¿qué hace que estas células decidan morir, y podría apagar un “interruptor” molecular ayudar a salvarlas?
Una capa celular frágil que mantiene la visión clara
El endotelio corneal es una lámina única de células hexagonales que bombea constantemente el líquido fuera de la córnea para mantenerla clara. En la FECD, estas células se estresan y desaparecen gradualmente, mientras que bultos de material anómalo, llamados guttae, se acumulan en la membrana subyacente. Dado que no existen fármacos aprobados para la FECD y los trasplantes de córnea son el tratamiento principal, los investigadores intentan entender exactamente cómo el estrés dentro de estas células las empuja hacia la muerte. Trabajos anteriores señalaron por separado tensión en dos compartimentos celulares clave —el retículo endoplásmico (la fábrica de plegado de proteínas de la célula) y las mitocondrias (las plantas de energía de la célula)—, pero no estaba claro cómo se comunicaban entre sí estas dos respuestas al estrés.
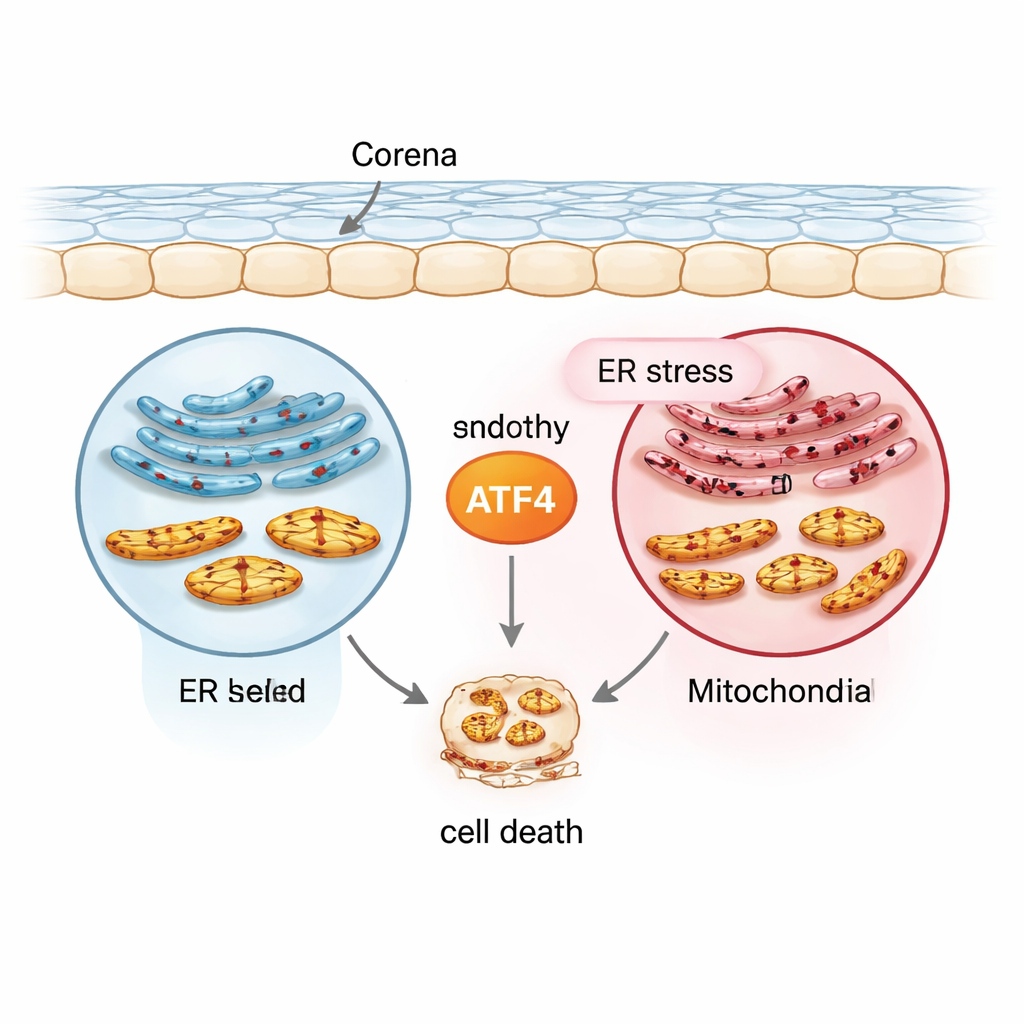
El mensajero del estrés en el centro: ATF4
El equipo se centró en una proteína llamada ATF4, un factor de transcripción que enciende o apaga muchos genes de respuesta al estrés. Usando una línea celular humana normal de endotelio corneal (21T), una línea similar a FECD portadora de la expansión repetida de TCF4 vinculada a la enfermedad (F35T), células endoteliales corneales humanas primarias y modelos de ratón expuestos a radiación ultravioleta A (UVA), crearon una serie de condiciones que imitan el estrés crónico. Indujeron estrés del retículo endoplásmico con un fármaco llamado tunicamicina y midieron luego ATF4 y otros marcadores. En comparación con las células normales, las células tipo FECD partían con niveles más altos de ATF4 y proteínas de estrés relacionadas, y ATF4 aumentó aún más bajo estrés crónico tanto en células cultivadas como en tejidos corneales humanos. Este patrón situó a ATF4 en la encrucijada entre respuestas protectoras tempranas y señales autodestructivas posteriores.
De la falla energética a la muerte programada
A continuación, los investigadores analizaron cómo este estrés afectaba a las mitocondrias. En las células tipo FECD, las mitocondrias produjeron menos ATP, perdieron su potencial eléctrico de membrana y se fragmentaron, pasando de formas largas y en red a muchos fragmentos pequeños. Estos cambios empeoraron cuando el estrés del retículo endoplásmico fue prolongado. Al mismo tiempo, proteínas clásicas de muerte celular —como caspasas activadas y la proteína reparadora de ADN PARP en su forma escindida, pro‑muerte— aumentaron, mientras que proteínas protectoras como Bcl‑2 disminuyeron. En conjunto, estos cambios indican que las células endoteliales corneales estresadas en FECD son empujadas hacia una apoptosis impulsada por mitocondrias, una forma ordenada pero irreversible de suicidio celular programado.
El sistema de limpieza se atasca bajo estrés crónico
Normalmente, las mitocondrias gravemente dañadas se eliminan mediante un proceso de reciclaje llamado mitofagia, en el que son etiquetadas y encerradas en pequeños sacos para su eliminación. El equipo encontró que las moléculas iniciadoras tempranas de la mitofagia (Parkin y LC3) se activaron tanto en células normales como en tipo FECD, especialmente tras el estrés. Pero las proteínas de soporte clave estaban reducidas, y la microscopía electrónica mostró una acumulación de mitocondrias parcialmente digeridas atrapadas en vesículas. Esto sugiere que, si bien el proceso de limpieza se iniciaba, no llegaba a completarse, dejando a las células llenas de centrales defectuosas que alimentan aún más el estrés y la muerte en lugar de la recuperación.
Apagar ATF4 para rescatar células
Para comprobar si ATF4 impulsaba esta espiral, los investigadores emplearon ARN de interferencia pequeño para silenciar parcialmente ATF4 en células endoteliales corneales cultivadas. Bajo el mismo estrés crónico, las células con ATF4 reducido mostraron niveles más bajos de proteínas que promueven la muerte, un potencial de membrana mitocondrial más sano, menos fragmentación y mejor supervivencia en pruebas de viabilidad. Es importante que el número de estructuras de mitofagia atascadas disminuyó, lo que sugiere que reducir ATF4 ayudó a restaurar un equilibrio más eficaz entre daño y limpieza. En ratones diseñados para tener solo una copia funcional del gen ATF4, la exposición a UVA provocó menor activación de una proteína partner pro‑muerte, CHOP, y preservó más células endoteliales con forma normal en comparación con ratones con ATF4 totalmente funcional.
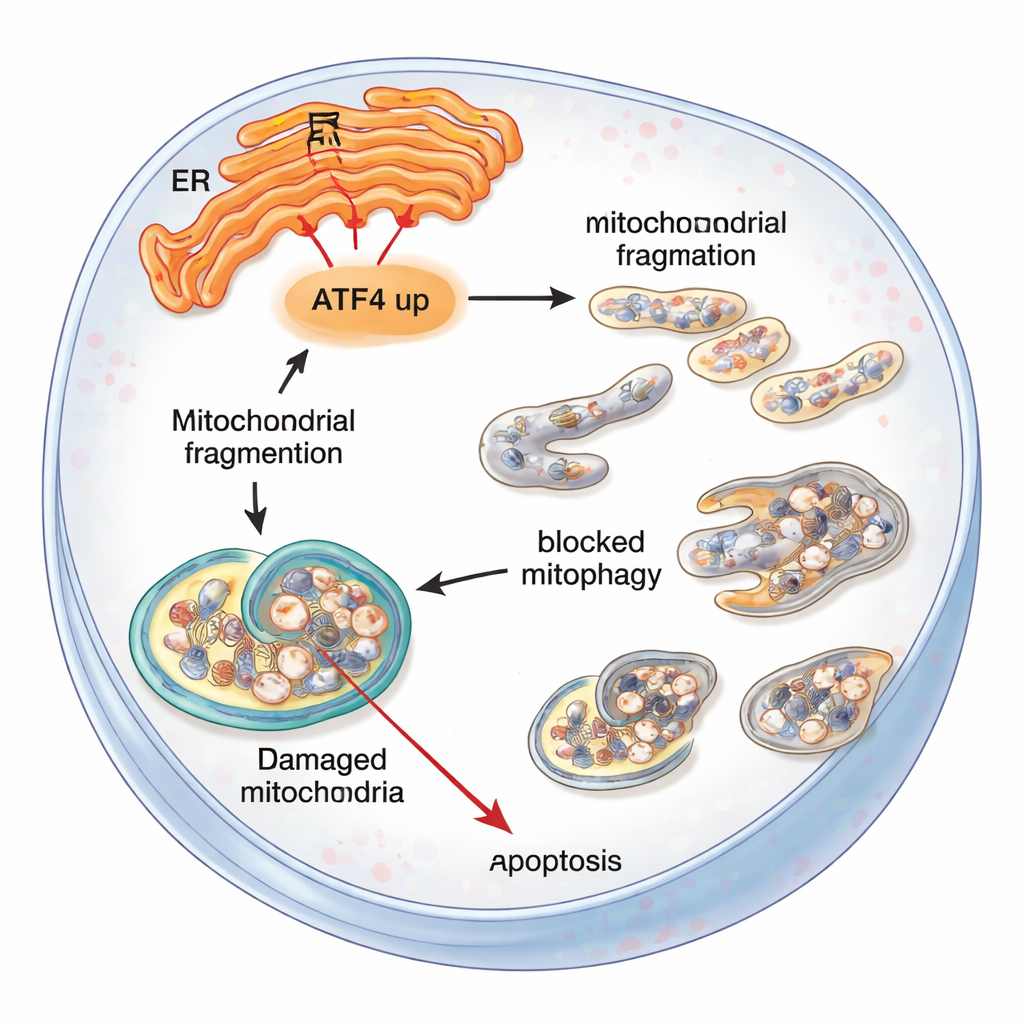
Qué significa esto para las personas con FECD
Para el público no especializado, el mensaje es que un mensajero del estrés, ATF4, puede inclinar a las células endoteliales corneales desde el afrontamiento hacia el colapso. Cuando el estrés del retículo endoplásmico dura, ATF4 contribuye a dañar las mitocondrias, atrasa la maquinaria de limpieza celular y, en última instancia, fomenta que estas células vitales se autodestruyan. Reducir ATF4 —ya sea genéticamente en ratones o con herramientas moleculares dirigidas en células— protege las mitocondrias, mejora la eliminación de desechos y mantiene más células vivas. Aunque este trabajo aún está en etapas de laboratorio y en animales, destaca a ATF4 y las vías de estrés relacionadas como dianas farmacológicas prometedoras que podrían algún día ralentizar o prevenir la progresión de la distrofia de Fuchs y reducir la necesidad de trasplantes de córnea.
Cita: Qureshi, S., Kim, S.Y., Lee, S. et al. ATF4 regulates mitochondrial dysfunction and mitophagy, contributing to corneal endothelial apoptosis. Sci Rep 16, 5960 (2026). https://doi.org/10.1038/s41598-026-36453-x
Palabras clave: Distrofia endotelial corneal de Fuchs, endotelio corneal, estrés mitocondrial, mitofagia, ATF4