Clear Sky Science · es
Un enfoque integrador para identificar nuevas redes de interacción miARN-ARNm en la cardiomiopatía por LMNA
Por qué importan los diminutos reguladores del corazón
La cardiomiopatía dilatada es una afección grave en la que el corazón se dilata y debilita, con frecuencia conduciendo a insuficiencia cardíaca, ritmos peligrosos y hasta muerte súbita. En muchas familias, esta enfermedad es hereditaria, y las alteraciones en un gen llamado LMNA son una causa frecuente. Este estudio plantea una pregunta aparentemente simple con grandes consecuencias: en los corazones dañados por mutaciones en LMNA, ¿qué genes se activan o silencian y qué moléculas de ARN diminutas están moviendo esos interruptores? Al mapear estas conversaciones moleculares en detalle, el trabajo apunta a nuevas formas de predecir, vigilar y quizá algún día tratar esta forma agresiva de enfermedad cardíaca.
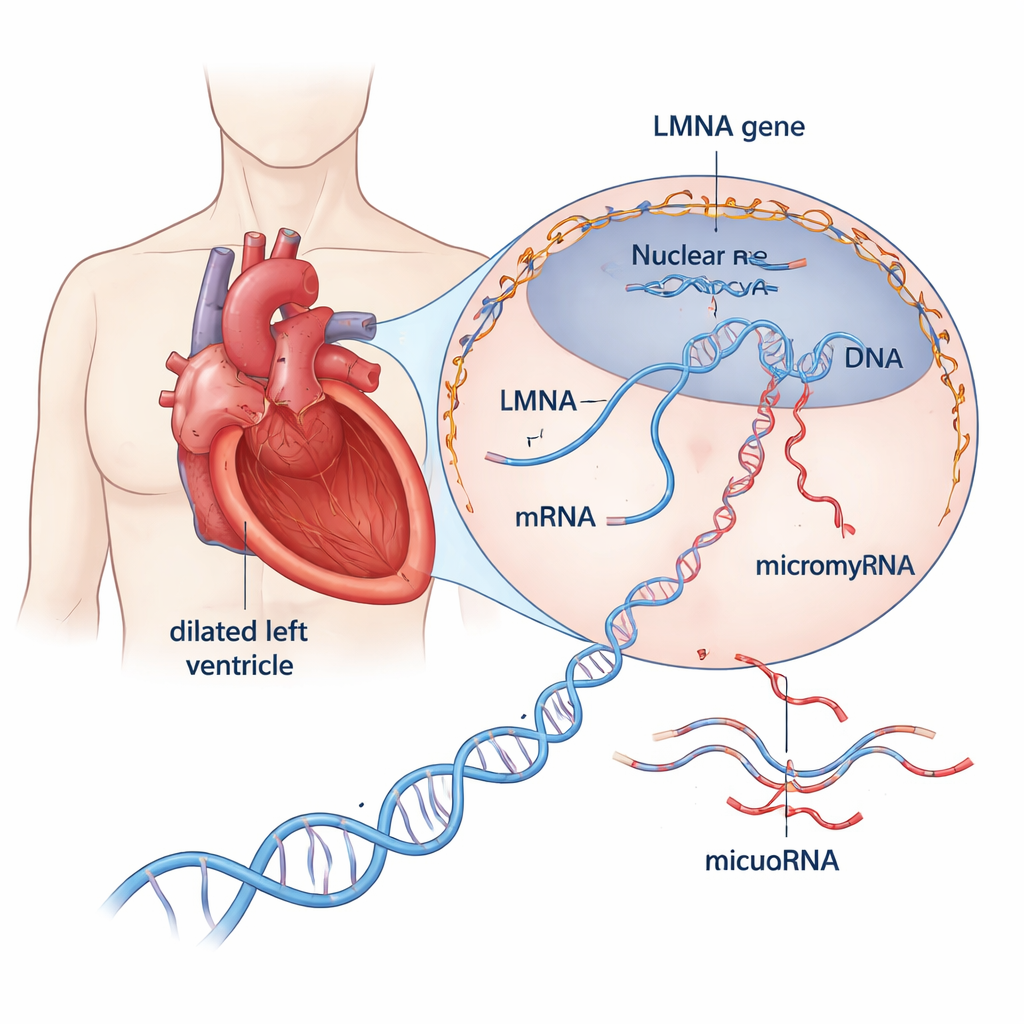
Una mirada más cercana a una enfermedad cardíaca peligrosa
La cardiomiopatía dilatada estira y adelgaza la cámara principal de bombeo del corazón, debilitando su capacidad para impulsar la sangre por el cuerpo. Aproximadamente entre un tercio y la mitad de los casos antes catalogados como “idiopáticos” resultan tener una base genética. Entre los más de 30 genes implicados, LMNA destaca: variantes dañinas en este gen explican aproximadamente el 10 % de los casos hereditarios y se asocian con progresión rápida de la enfermedad, problemas rítmicos tempranos y un alto riesgo de muerte cardíaca súbita. LMNA codifica proteínas estructurales que forman un andamiaje alrededor del ADN de la célula, ayudando a mantener la forma del núcleo e influyendo en qué genes están activos. Sin embargo, no se ha comprendido bien cómo las proteínas LMNA defectuosas empujan al corazón hacia la insuficiencia.
Siguiendo los mensajes dentro de corazones de ratón
Para explorar esto, los investigadores usaron un modelo de ratón portador de una mutación conocida de LMNA (R249W) que desarrolla una forma de cardiomiopatía dilatada similar a la humana. A las 50 semanas de edad —cuando los ratones muestran ventrículos agrandados, función de bombeo reducida y cicatrización fibrótica— el equipo extrajo tejido cardíaco y examinó dos tipos de ARN: ARN mensajero (ARNm), que transporta instrucciones para fabricar proteínas, y microARN (miARN), cadenas cortas no codificantes que afinan la actividad génica bloqueando o degradando ARNm específicos. Mediante secuenciación de alto rendimiento y filtros estadísticos rigurosos, identificaron 2.148 genes cuya actividad cambió en corazones con la mutación y 53 miARNs que aumentaron o disminuyeron en comparación con ratones sanos.
Qué cambia dentro de las células cardíacas enfermas
Al agrupar los genes alterados en vías biológicas, surgieron varios temas. Muchos de los genes cambiados estaban vinculados a cómo se contraen las células del músculo cardíaco, cómo se adhieren entre sí y a su matriz de soporte, cómo viajan las señales eléctricas por el corazón y cómo las células procesan grasas para generar energía. Estos hallazgos encajan bien con el panorama clínico de la enfermedad relacionada con LMNA: tejido rígido y fibrótico; conducción eléctrica perturbada que favorece arritmias; y equilibrio energético deteriorado. Los análisis de vías con bases de datos establecidas confirmaron un enriquecimiento en remodelado de la matriz extracelular, canales iónicos dependientes de voltaje, comunicación tipo sináptica en el corazón y metabolismo de ácidos grasos —lo que sugiere que la mutación en LMNA altera múltiples sistemas interconectados en lugar de un único paso defectuoso.
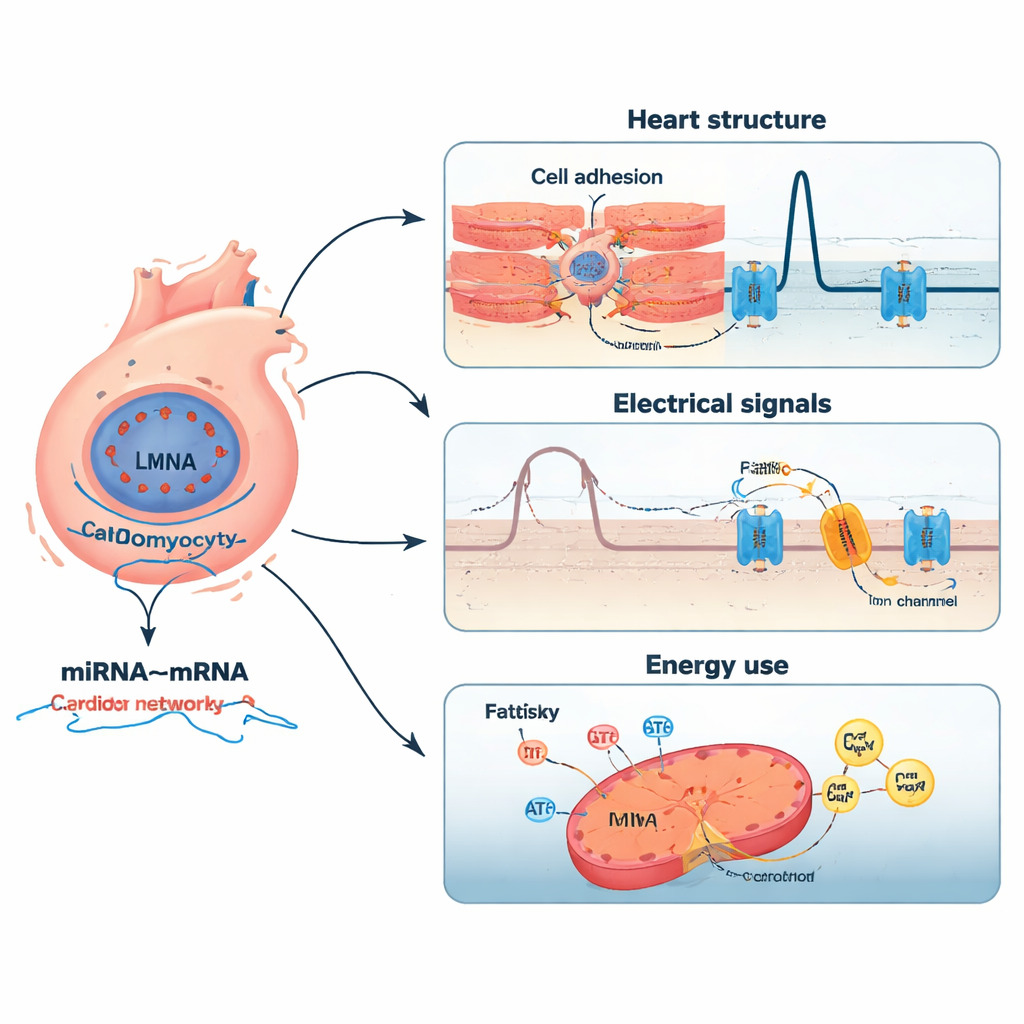
Redes de diminutos interruptores y sus dianas
El estudio fue más allá al emparejar miARNs con sus probables dianas en ARNm. Utilizando análisis de correlación y comprobaciones cruzadas contra grandes bases de datos de interacciones validadas experimentalmente, los autores ensamblaron una red de alta confianza de 2.197 pares miARN–ARNm que involucraban 12 miARNs clave. Algunos miARNs estaban más activos y parecían atenuar genes críticos para el desarrollo cardíaco, el manejo del calcio y las respuestas al estrés oxidativo. Otros estaban menos activos, potencialmente liberando los frenos sobre genes implicados en adhesión celular, inflamación y remodelado del andamiaje estructural del corazón. Por ejemplo, un miARN (miR-183-5p) se vinculó a un receptor en la vía de señalización Wnt, que influye en la comunicación célula a célula, mientras que otro (miR-3473a) se conectó a un canal de liberación de calcio central para el ritmo cardíaco. Juntas, estas redes muestran cómo cambios sutiles en reguladores de ARN diminutos pueden amplificar el impacto de una mutación en LMNA.
De los mapas moleculares a futuras terapias
Para quienes no son especialistas, la conclusión es que este estudio ofrece un mapa detallado de cómo una mutación en LMNA remodela el cableado interno del corazón a nivel del control génico. En vez de un único “gen malo”, la enfermedad refleja una cascada de mensajes alterados —muchos orquestados por miARNs— que afectan la estructura cardíaca, la estabilidad eléctrica y el uso de energía. Aunque el trabajo se realizó en ratones y se apoya en gran medida en análisis computacionales, destaca pares específicos miARN–gen como candidatas prometedoras para futuros biomarcadores en sangre o terapias dirigidas. A largo plazo, ajustar estos diminutos interruptores de ARN podría ayudar a los médicos a predecir mejor quién tiene mayor riesgo, monitorizar la progresión de la enfermedad con más precisión y diseñar tratamientos más personalizados para las familias afectadas por la cardiomiopatía relacionada con LMNA.
Cita: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
Palabras clave: cardiomiopatía dilatada, gen LMNA, microARN, regulación génica, insuficiencia cardíaca