Clear Sky Science · es
Segmentación de trombosis venosa profunda consciente de la privacidad mediante un marco de aprendizaje federado multimodelo con el algoritmo de promediado federado
Por qué importan los coágulos y la privacidad de los datos
Los coágulos que se forman en las venas profundas de las piernas, conocidos como trombosis venosa profunda (TVP), pueden desplazarse silenciosamente hasta los pulmones y provocar emergencias potencialmente mortales. Las tomografías computarizadas (TC) pueden revelar estos coágulos, pero convertir miles de imágenes en escala de grises en detecciones automáticas fiables es una tarea difícil para los ordenadores. Al mismo tiempo, los hospitales son comprensiblemente cautelosos a la hora de compartir datos sensibles de los pacientes. Este estudio explora cómo varios hospitales pueden colaborar para entrenar un potente sistema de inteligencia artificial (IA) para detectar coágulos sin necesidad de agrupar o exponer nunca sus exploraciones de pacientes en bruto.
Compartir cerebros, no cuerpos
El núcleo del trabajo es una técnica llamada aprendizaje federado, que permite a varias instituciones entrenar modelos de IA de forma colaborativa manteniendo sus datos localmente. En lugar de enviar las imágenes de TC a un servidor central, cada hospital entrena su propio modelo local con sus propias exploraciones. Solo se envían al servidor central los parámetros aprendidos por el modelo, esencialmente lo que ha "aprendido" sobre el reconocimiento de coágulos. Allí, un enfoque llamado promediado federado combina estos distintos conjuntos de parámetros en un único modelo global mejorado, que luego se envía de vuelta a todos los hospitales. De este modo, cada sitio se beneficia de la experiencia colectiva de todos los participantes, mientras que ninguna imagen de paciente abandona su institución de origen. 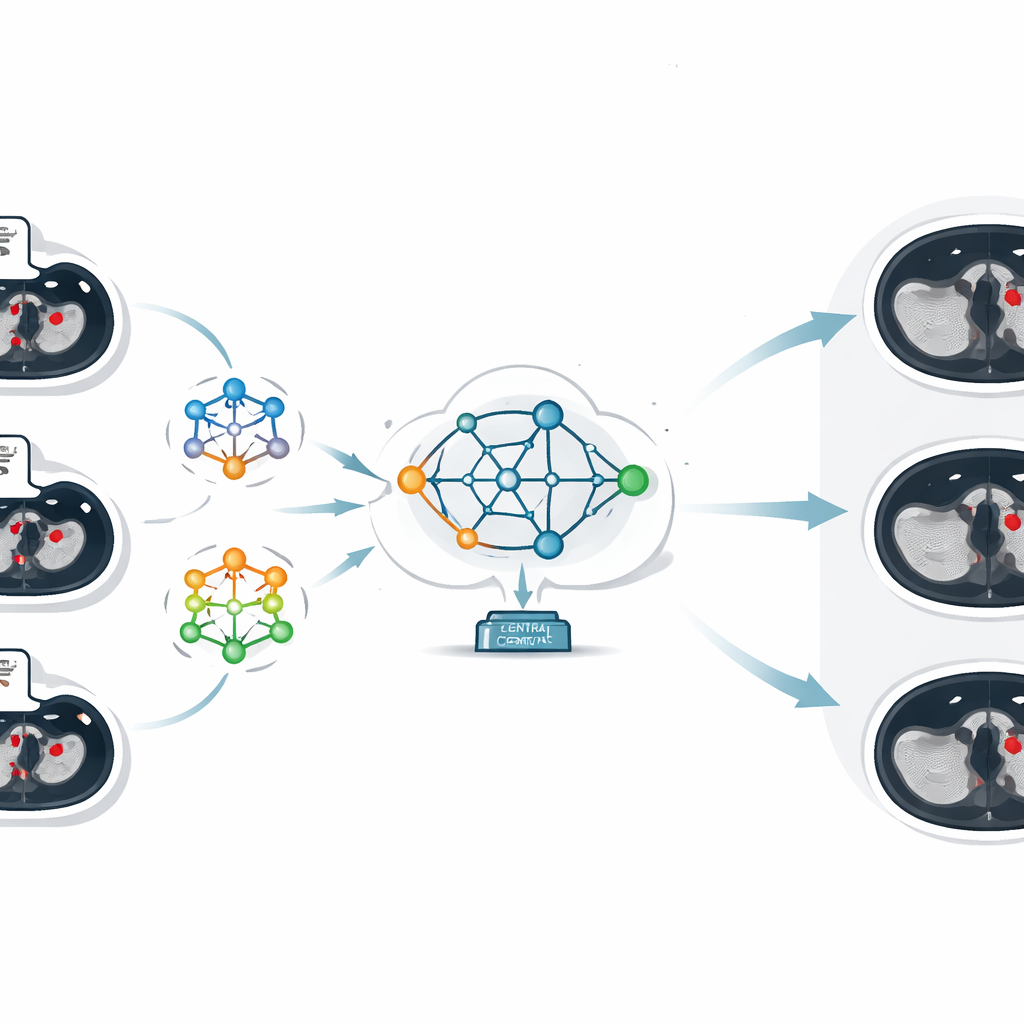
Muchos estilos de IA observando las mismas venas
Una innovación clave de este estudio es que los investigadores no se basaron en un único tipo de red neuronal. Reunieron siete diseños de modelo diferentes, cada uno con ventaja para ver distintos aspectos de las imágenes TC. Los modelos más simples, como redes convolucionales básicas y modelos secuenciales, son más rápidos y fáciles de ejecutar en hardware limitado. Arquitecturas más avanzadas, incluidas U‑Net, VGG‑19 y dos redes personalizadas con bloques residuales, inception, de atención y de procesamiento multiescala, son mejores trazando fronteras finas de los vasos, detectando coágulos pequeños y manejando imágenes ruidosas. Permitir que cada hospital utilice el modelo que mejor se adapta a sus datos y capacidad de cómputo hace que el sistema refleje la realidad desordenada de los entornos clínicos reales en lugar de suponer que todos los centros son idénticos.
Aprender de datos desiguales e imperfectos
En medicina, los datos de un hospital rara vez se parecen exactamente a los de otro. Los escáneres, los protocolos de imagen y las poblaciones de pacientes difieren, por lo que el estudio trabajó deliberadamente con datos "no IID" —colecciones desiguales y no idénticamente distribuidas. Esto normalmente hace que el entrenamiento sea más inestable. Aquí, los autores abrazaron esa diversidad y mostraron que agregar conocimiento procedente de múltiples modelos estructuralmente distintos en realidad mejoraba la capacidad de generalización del sistema global. Realizaron tres fases experimentales: primero con tres clientes, luego cinco y finalmente siete, usando conjuntos de datos de 1.000, 2.000 y 3.000 imágenes TC. En cada paso siguieron no solo con qué frecuencia el modelo global segmentaba correctamente los coágulos, sino también cuánta comunicación se necesitó, cuánto tiempo tardó el entrenamiento, cuán diferentes eran los datos de cada cliente y qué tan efectivas eran las protecciones de privacidad.
Mejor detección de coágulos, a un precio computacional
En todas las fases, el modelo global combinado superó de forma consistente a cualquier modelo local individual. A medida que aumentó el número de imágenes y entraron en la federación modelos más sofisticados, la precisión de segmentación subió de aproximadamente un 91 % a más del 96 %, y una medida de calidad equilibrada llamada puntuación F1 ascendió de alrededor de 0,89 a 0,95. Al mismo tiempo, una medida de pérdida centrada en el error se redujo a más de la mitad, señalando contornos de coágulos más limpios y fiables. Estas mejoras no fueron gratuitas: la comunicación entre clientes y servidor pasó de unas decenas de megabytes a varios gigabytes, y el tiempo medio de entrenamiento aumentó de segundos a muchas horas a medida que maduraba la arquitectura. No obstante, el sistema mantuvo una fuerte garantía formal de privacidad, indicando que las actualizaciones compartidas filtran muy poca información sobre cualquier paciente individual. 
Qué significa esto para pacientes y hospitales
Para un lector no especializado, la conclusión es que este trabajo demuestra cómo los hospitales pueden enseñar a una IA compartida a detectar coágulos peligrosos con mayor precisión sin ceder el control de sus datos sensibles. Al combinar varios diseños de modelos complementarios y agregar con cuidado lo que cada uno aprende, los autores construyen un sistema de segmentación de coágulos que es a la vez potente y respetuoso con la privacidad. Aunque el enfoque requiere recursos computacionales y ancho de banda de red considerables, apunta a un futuro en el que los centros médicos colaboren de forma rutinaria en herramientas diagnósticas más inteligentes, mejorando la atención de pacientes en riesgo de TVP y condiciones relacionadas mientras mantienen sus exploraciones personales protegidas detrás de los muros institucionales.
Cita: B, P.L., S, V. Privacy-aware deep vein thrombosis segmentation using a multi-model federated learning framework with the federated averaging algorithm. Sci Rep 16, 11333 (2026). https://doi.org/10.1038/s41598-026-36432-2
Palabras clave: trombosis venosa profunda, aprendizaje federado, segmentación de imágenes médicas, IA que preserva la privacidad, imágenes por TC