Clear Sky Science · es
Actividad antitumoral de QAL333 y modelado predictivo: análisis integrado transcriptómico-bioinformático revela citotoxicidad selectiva y determinantes de sensibilidad
Por qué importa este nuevo candidato farmacológico
Los fármacos contra el cáncer suelen funcionar bien en algunos pacientes pero fracasan en otros, en gran parte porque los tumores difieren en su cableado interno. Este estudio presenta un compuesto de nuevo diseño, QAL333, que parece atacar con mayor fuerza ciertos cánceres colorrectales mientras respeta a muchas células normales. Igualmente importante, los investigadores muestran cómo los patrones de actividad génica en las células tumorales podrían ayudar a predecir quién es más probable que se beneficie, apuntando a estrategias de tratamiento más precisas y personalizadas.
Un golpe dirigido a tipos tumorales específicos
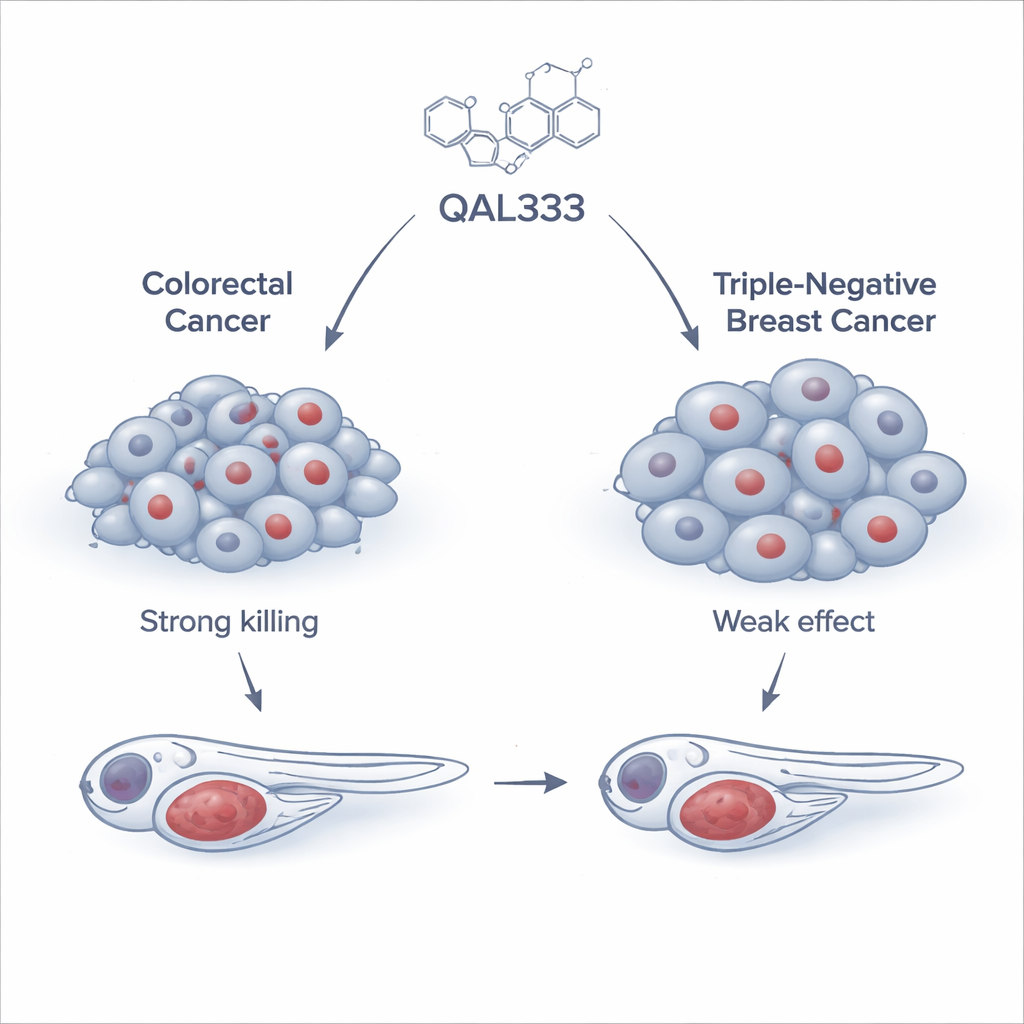
El equipo comenzó probando QAL333, una molécula sintética relacionada con una familia de compuestos ya conocida por dañar células cancerosas, en un amplio panel de 15 líneas celulares humanas tumorales y tres líneas no cancerosas. Encontraron que las células de cáncer colorrectal, en especial una línea llamada SW620, eran muy sensibles, con el fármaco matándolas a dosis relativamente bajas. En contraste, las células de cáncer de mama triple negativas fueron mucho más resistentes y requirieron dosis más de diez veces superiores, difíciles de alcanzar de forma segura. Curiosamente, no todas las células no cancerosas reaccionaron igual: algunas eran sensibles, pero otras, como una línea celular renal de uso extendido, resultaron sorprendentemente resistentes. Este patrón mostró que los efectos de QAL333 dependen más de la biología interna de la célula que de si se etiqueta como “cancerosa” o “normal”.
Probando el fármaco en organismos vivos
Para ver si los prometedores resultados en cultivo celular se mantenían en un organismo vivo, los investigadores recurrieron al pez cebra, un pez pequeño y transparente ampliamente usado para modelar enfermedades humanas. Implantaron células humanas tumorales etiquetadas con fluorescencia en embriones de pez cebra y los trataron con QAL333. En peces que portaban células de cáncer colorrectal, el fármaco frenó claramente el crecimiento tumoral, aproximándose al efecto de una combinación de quimioterapia estándar utilizada en la clínica. En contraste, los tumores formados por las células de cáncer de mama triple negativo respondieron apenas, aunque un fármaco común contra el cáncer de mama, el paclitaxel, funcionó bien en el mismo modelo. Estas pruebas in vivo reforzaron que la fortaleza de QAL333 reside en un subconjunto de tumores y no en todos los cánceres.
Mirando dentro de las células para ver cómo actúa QAL333
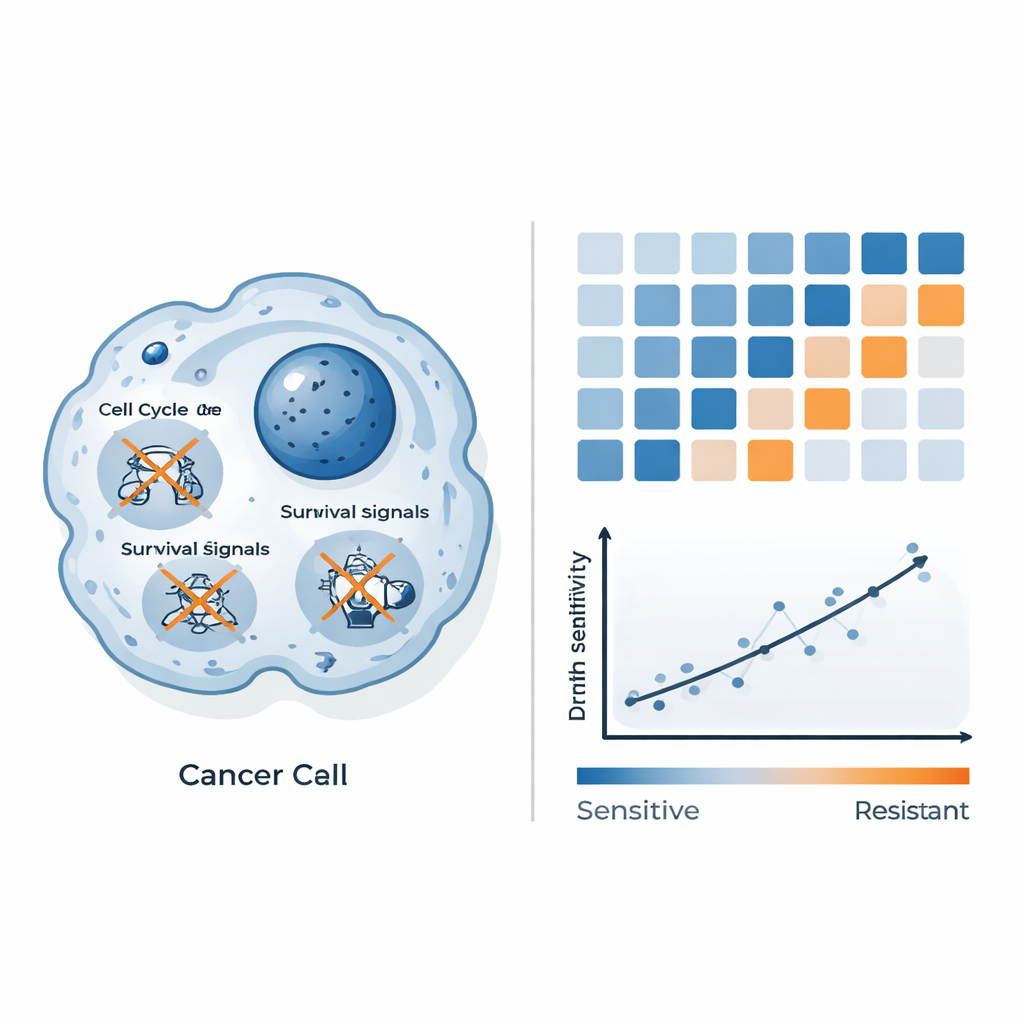
Para entender por qué algunas células mueren y otras resisten, los científicos midieron cómo cambiaron los niveles de actividad de miles de genes tras el tratamiento con QAL333. En las células colorrectales sensibles, genes clave que impulsan el ciclo de división y el crecimiento celular se apagaron, y se atenuaron vías principales de supervivencia. También se alteraron señales vinculadas al estrés oxidativo y a una forma de muerte celular distinta de la apoptosis clásica, lo que sugiere que QAL333 sobrecarga sistemas ya frágiles encargados de gestionar el daño dentro de estas células. Las células resistentes de cáncer de mama, por el contrario, activaron programas de estrés e inflamación controlados por factores como NF-κB, conocidos por ayudar a las células a afrontar condiciones perjudiciales. Esta comparación lado a lado dibujó una imagen de QAL333 abrumando defensas débiles en algunas células, mientras que otras montan una contrarrespuesta eficaz.
Usar patrones génicos para predecir quién responderá
Más allá de catalogar cambios génicos, los investigadores se preguntaron si estos patrones podían convertirse en una herramienta práctica de predicción. Combinaron datos de actividad génica basal del panel de líneas celulares con su sensibilidad medida al fármaco y usaron aprendizaje automático para buscar las señales más informativas. En lugar de confiar en genes individuales, agruparon genes en vías biológicas y crearon una “puntuación de vía” combinada construida a partir de tres sistemas: cómo las células procesan energía y sustancias químicas (vías metabólicas), cómo organizan su entorno (proteoglucanos y estructuras relacionadas en el cáncer) y cómo se organiza su citoesqueleto. Esta puntuación compuesta se correlacionó fuertemente con la dosis de QAL333 necesaria para matar cada línea celular: puntuaciones más bajas se alinearon con mayor sensibilidad y puntuaciones más altas con resistencia. En otras palabras, la afinación de estas redes dentro de un tumor puede pronosticar qué tan bien funcionará QAL333.
Pistas inesperadas de efectos biológicos más amplios
Aunque el foco principal fue el cáncer, QAL333 también mostró capacidad para interrumpir el “quorum sensing”, un sistema de comunicación que las bacterias usan para coordinar comportamientos como la formación de biopelículas. A dosis muy bajas, el compuesto redujo la formación de biopelículas por una bacteria asociada a enfermedades de las encías y atenuó ciertas señales inflamatorias en células inmunitarias. Los autores tratan estos hallazgos como tempranos y exploratorios, pero sugieren que QAL333 o moléculas relacionadas podrían algún día tener usos más allá de la terapia contra el cáncer, por ejemplo en infecciones en las que comunidades bacterianas son difíciles de erradicar.
Qué podría significar esto para futuros pacientes
En conjunto, el estudio posiciona a QAL333 como un candidato farmacológico selectivo que golpea tumores colorrectales vulnerables mientras respeta muchos otros tipos celulares, y lo acompaña de una hoja de ruta para predecir qué tumores probablemente responderán. Si se confirma en modelos animales más avanzados y, eventualmente, en pacientes, una sencilla prueba de expresión génica podría ayudar a los médicos a decidir cuándo QAL333 es una buena opción, alineándose con el objetivo más amplio de adaptar el tratamiento del cáncer al cableado de cada tumor. Al mismo tiempo, el trabajo subraya que incluso los fármacos prometedores tienen límites: los cánceres de mama y otros tumores resistentes pueden requerir combinaciones inteligentes o estrategias completamente diferentes.
Cita: Kim, H.H., Im, S., Kim, J. et al. QAL333’s antitumor activity and predictive modeling: integrated transcriptomic-bioinformatic analysis reveals selective cytotoxicity and sensitivity determinants. Sci Rep 16, 5648 (2026). https://doi.org/10.1038/s41598-026-36430-4
Palabras clave: cáncer colorrectal, terapia dirigida, expresión génica, modelado de sensibilidad a fármacos, xenoinjerto en pez cebra