Clear Sky Science · es
De modelos QSAR in silico a ensayos MTT in vitro: validación experimental de nuevos candidatos uPAR para cáncer de mama triple negativo (TNBC) y cáncer de piel
Por qué importa esta investigación
Cánceres como el de mama triple‑negativo y ciertos cánceres de piel son notoriamente difíciles de tratar porque se diseminan con rapidez y a menudo resisten las terapias estándar. Este estudio explora un objetivo prometedor en la superficie de las células tumorales —denominado uPAR— y muestra cómo la combinación de diseño de fármacos por ordenador con experimentos de laboratorio puede descubrir nuevos candidatos a fármaco que podrían frenar o detener la progresión de estos tumores agresivos.
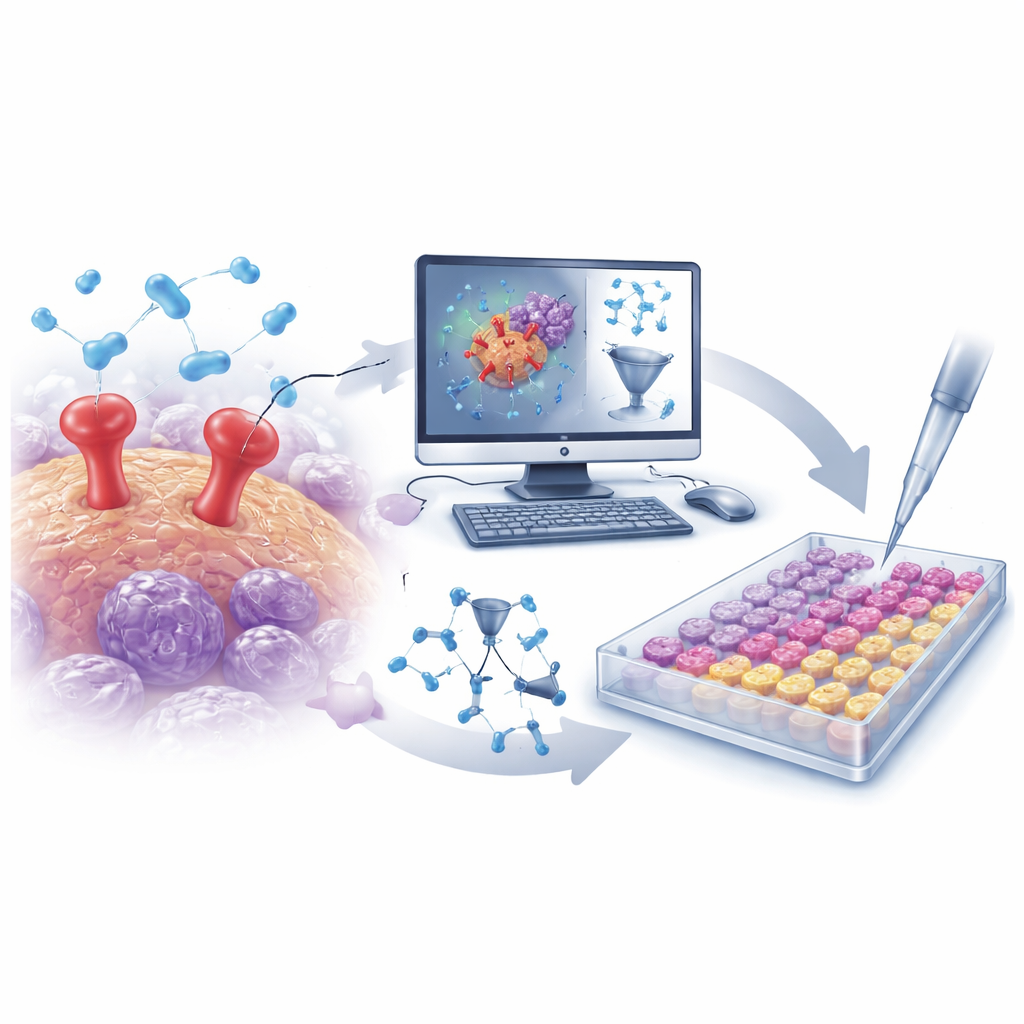
Una puerta que ayuda a la diseminación del cáncer
Para que un tumor se vuelva letal, sus células deben liberarse del sitio original, degradar el tejido circundante, entrar en el torrente sanguíneo y colonizar órganos distantes. uPAR es un colaborador clave en este proceso. Se encuentra en la superficie de la célula cancerosa y actúa con proteínas asociadas para activar enzimas que disuelven la estructura de soporte circundante, facilitando el movimiento e invasión celular. uPAR se encuentra en niveles especialmente altos en células de cáncer de mama triple‑negativo y en ciertos cánceres de piel, y su abundancia se asocia con crecimiento más rápido, mayor invasividad y peores resultados clínicos. Por ello, uPAR es un objetivo atractivo —aunque hasta ahora poco explotado— para fármacos antitumorales.
Minería de grandes datos químicos con algoritmos inteligentes
Los investigadores comenzaron reuniendo una amplia colección de más de 500 moléculas conocidas que bloquean uPAR procedentes de una base de datos pública. La estructura de cada molécula se tradujo en miles de descriptores numéricos que capturan características como tamaño, forma, distribución de carga y flexibilidad. Con estos datos, el equipo construyó un modelo de relación cuantitativa estructura‑actividad (QSAR), un tipo de herramienta matemática que aprende qué rasgos estructurales tienden a convertir una molécula en un inhibitor más potente de uPAR. Tras una validación cuidadosa para evitar sobreajuste, el modelo mostró un alto poder predictivo sobre compuestos no vistos, destacando varias características clave que potenciaban o debilitaban el bloqueo de uPAR. Estos conocimientos guiaron la búsqueda de nuevas moléculas mejor diseñadas.
De cribados virtuales a tubos de ensayo reales
Armados con el modelo QSAR entrenado, el equipo cribó virtualmente una biblioteca focalizada de alrededor de 30.000 moléculas dirigidas a proteasas. El modelo redujo rápidamente este vasto conjunto a un pequeño grupo de inhibidores de uPAR probables. En paralelo, se usaron simulaciones de acoplamiento (docking) por ordenador para evaluar cómo encajaba cada candidato en el sitio de unión de uPAR, y simulaciones de dinámica molecular probaron si estos complejos acoplados se mantenían estables a lo largo del tiempo. De esta campaña in silico combinada surgieron dos moléculas destacadas: D685‑0061, señalada por el modelo QSAR como altamente potente, y C878‑1660, resaltada por docking y simulación por formar interacciones especialmente estables con uPAR.
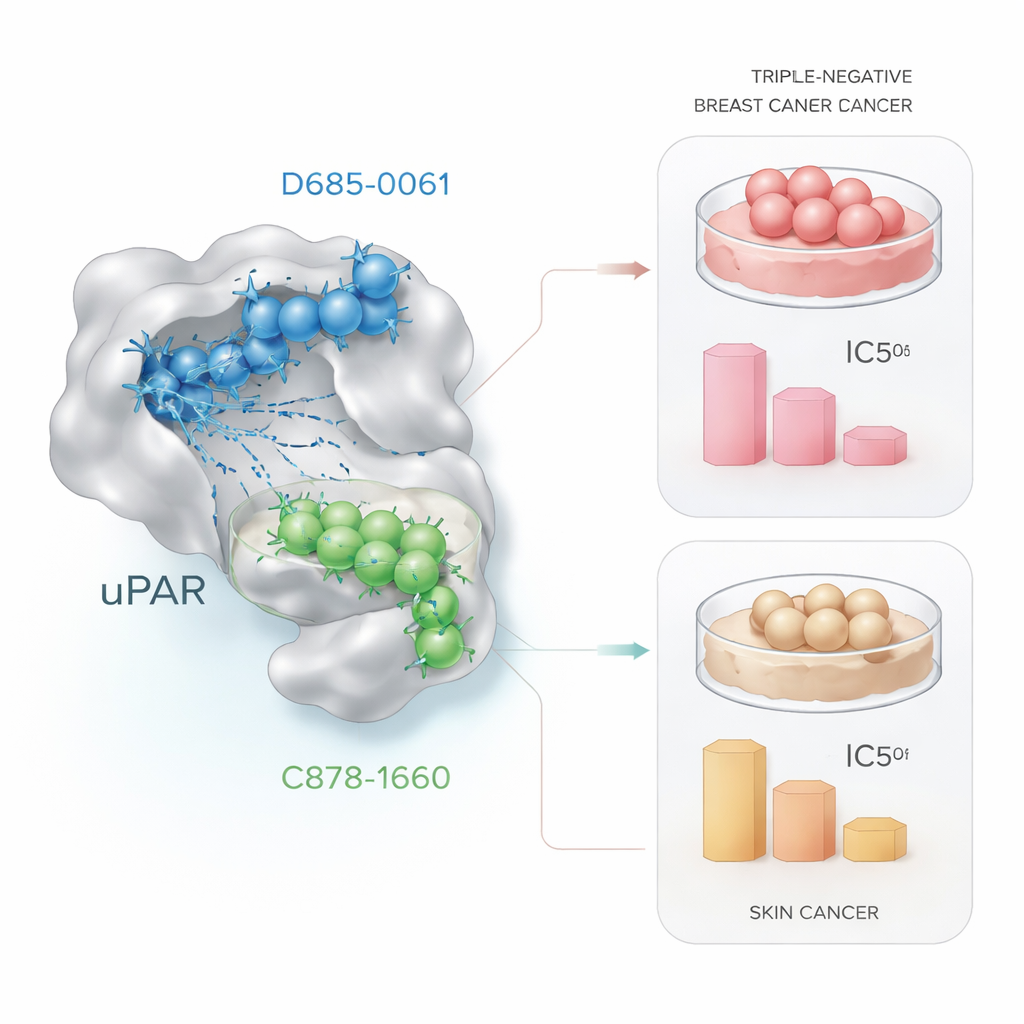
Poniendo a prueba los candidatos en células cancerosas
La promesa computacional solo tiene sentido si se traduce en efectos biológicos reales. Para comprobarlo, los investigadores expusieron células tumorales vivas a dosis crecientes de las dos moléculas líderes y midieron la supervivencia celular usando un método de laboratorio estándar llamado ensayo MTT. En células de cáncer de mama triple‑negativo (MDA‑MB‑231), D685‑0061 mató células con mayor eficacia, reduciendo la viabilidad a la mitad alrededor de 21 micromoles, mientras que C878‑1660 requirió aproximadamente cuatro veces esa concentración. Al microscopio, las células tratadas con D685‑0061 mostraron signos claros de muerte celular programada, como redondeamiento, desprendimiento de la superficie y fragmentación. En contraste, en células de cáncer de piel (A431), C878‑1660 fue el más potente, alcanzando el 50% de mortalidad celular alrededor de 19 micromoles frente a unos 28 micromoles para D685‑0061, también con daño visible dependiente de la dosis.
Qué implica esto para tratamientos futuros contra el cáncer
Este trabajo no entrega un fármaco nuevo de forma inmediata, pero sí aporta dos puntos de partida prometedores y, igual de importante, un plan eficaz para encontrar más. Al vincular modelado de big data, simulaciones 3D y experimentos celulares cuidadosos, el estudio muestra que uPAR puede ser dirigido de forma selectiva con pequeñas moléculas que dañan células agresivas de cáncer de mama y de piel. D685‑0061 y C878‑1660 ahora sirven como compuestos líderes que los químicos pueden optimizar para aumentar potencia, mejorar seguridad y optimizar su farmacocinética. A más largo plazo, fármacos desarrollados con este enfoque podrían ayudar a bloquear la diseminación de cánceres impulsados por uPAR, convirtiendo algunos de los tumores más peligrosos de hoy en enfermedades más manejables.
Cita: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
Palabras clave: inhibidores de uPAR, cáncer de mama triple negativo, cáncer de piel, diseño de fármacos asistido por ordenador, ensayo de viabilidad celular MTT