Clear Sky Science · es
Un estudio por teoría del funcional de la densidad sobre la adsorción de ciclofosfamida y purinethol en un marco covalente triazínico (CTF-2) para aplicaciones de administración de fármacos
Por qué importa una quimioterapia más inteligente
Los fármacos quimioterápicos salvan vidas, pero a menudo actúan como un foco que lo ilumina todo en vez de un haz dirigido: atacan las células sanas junto con las cancerosas. Esto puede provocar efectos secundarios graves, desde fatiga e infecciones hasta daño orgánico. El estudio que se presenta aquí explora un material ultrafino y altamente poroso llamado marco covalente triazínico (CTF-2) como una “esponja inteligente” que puede transportar dos fármacos anticancerígenos de uso prolongado—ciclofosfamida y purinethol—de forma más segura y eficiente hasta donde se necesitan, y luego liberarlos en condiciones similares a las tumorales.
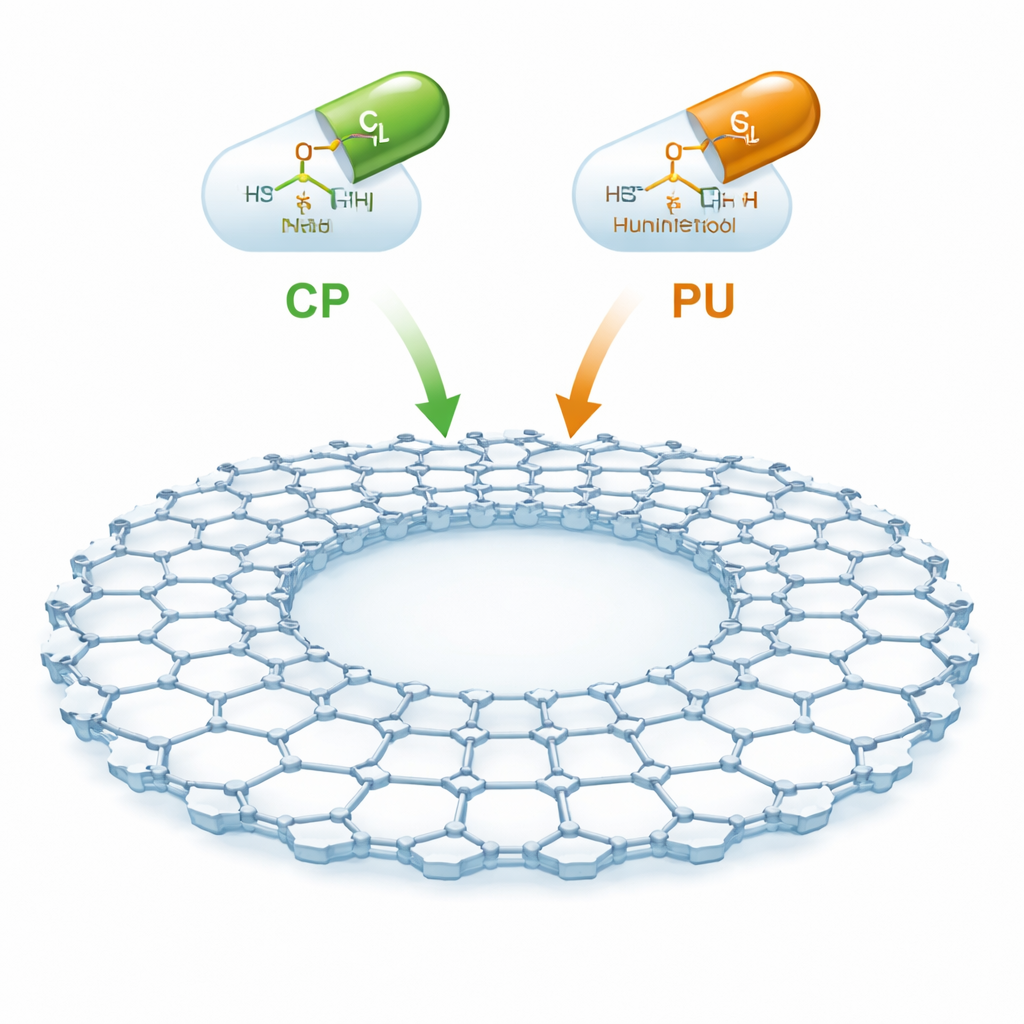
Una nueva clase de esponja molecular
El CTF-2 es un material sintético formado por anillos de carbono y nitrógeno unidos en una red plana y en lámina con una gran cavidad central y mucho espacio abierto. Por ser delgado, estable y poroso, ofrece una enorme área superficial interna para atrapar moléculas de fármaco. Los autores se centraron en dos medicamentos oncológicos importantes: la ciclofosfamida, ampliamente usada para cánceres hematológicos y tumores sólidos, y el purinethol (también llamado mercaptopurina), empleado contra las leucemias y algunas enfermedades inflamatorias intestinales. La idea es anclar estos fármacos suavemente sobre la superficie del CTF-2 para que puedan circular por el torrente sanguíneo y liberarse de forma más selectiva, reduciendo el daño a los tejidos sanos.
Explorar lo invisible con experimentos por ordenador
En lugar de trabajar en un laboratorio húmedo, el equipo usó cálculos computacionales avanzados a nivel cuántico (teoría del funcional de la densidad y métodos relacionados) para preguntar con qué fuerza se adheriría cada fármaco al CTF-2 y qué mantiene unidos a los complejos. Optimizaron las geometrías del CTF-2 más cada fármaco, midieron las distancias entre átomos en los puntos de contacto y calcularon cuánta energía se gana cuando un fármaco se adhiere al entramado. Para la ciclofosfamida, la energía de adsorción calculada fue de alrededor de −1,04 electronvoltios, algo más fuerte que los −0,82 electronvoltios hallados para el purinethol. Estos valores, que se mantienen claramente favorables incluso tras corregir artefactos técnicos y simular el agua como disolvente, indican que ambos fármacos se unen con suficiente firmeza para cargarse pero no tan fuertemente como para impedir su liberación posterior.
Fuerzas suaves que realizan un trabajo importante
El estudio muestra que el “pegamento” entre los fármacos y el CTF-2 no es un enlace químico duro sino una red de fuerzas no covalentes y suaves. Mediante análisis especializados de la densidad electrónica—esencialmente mapas de dónde residen los electrones compartidos—los investigadores encontraron que predominan las atracciones de van der Waals (las mismas fuerzas débiles que permiten a las geckos trepar paredes) y las interacciones electrostáticas moderadas. Estas interacciones ocurren a distancias cortas pero no enlazantes entre átomos de hidrógeno, nitrógeno, oxígeno, azufre y carbono presentes en los fármacos y en el entramado. Cálculos adicionales que descomponen la atracción total en distintos componentes confirmaron que las fuerzas electrostáticas y de dispersión (van der Waals) proporcionan la mayor parte del tirón estabilizador, mientras que las fuerzas repulsivas evitan que el fármaco se hunda demasiado o se una de forma irreversible.
Señales de carga estable y liberación modulable
El equipo también examinó cómo se redistribuyen los electrones cuando los fármacos se aposentan sobre el CTF-2 y cómo esto modifica propiedades eléctricas básicas. Observaron transferencias de carga pequeñas pero claras entre cada fármaco y el entramado y un ligero estrechamiento de la brecha energética que separa los estados electrónicos ocupados de los vacíos. Esto implica que la reactividad y la conductividad del material se ajustan sutilmente al cargarse, una característica útil para futuras aplicaciones de detección o teranóstica. De forma crucial, al simular el entorno más ácido que se encuentra cerca de los tumores añadiendo protones extra, la unión calculada se debilitó y las distancias de contacto aumentaron. En términos sencillos, las simulaciones sugieren que el CTF-2 puede retener los fármacos en condiciones normales similares a las sanguíneas, pero tenderá a liberarlos más fácilmente en entornos tumorales ácidos—justo el comportamiento deseado para una entrega dirigida.
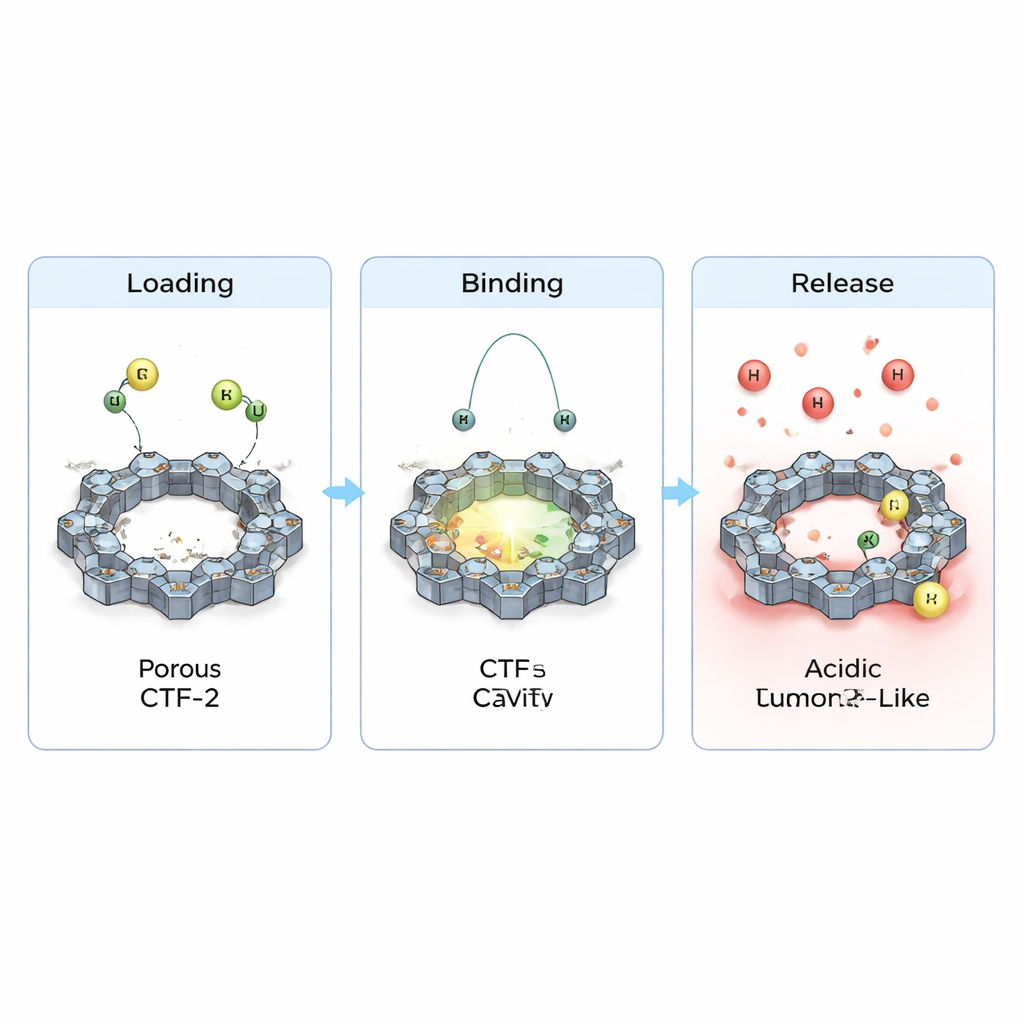
Qué significa esto para futuros tratamientos contra el cáncer
En conjunto, estos cálculos presentan al CTF-2 como un transportador prometedor para la ciclofosfamida y el purinethol: puede cargarlos en su superficie porosa de forma estable, protegerlos durante la circulación y luego liberarlos cuando la química local cambia alrededor de un tumor. Aunque el trabajo es teórico y necesitará confirmación experimental, sugiere que marcos finamente diseñados y ricos en nitrógeno como el CTF-2 podrían ayudar a transformar fármacos quimioterápicos antiguos pero efectivos en medicinas más inteligentes—entregando dosis potentes donde más se necesitan y reduciendo el daño colateral a las células sanas.
Cita: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
Palabras clave: nanotransportador, administración de fármacos, quimioterapia contra el cáncer, marco covalente triazínico, modelado computacional