Clear Sky Science · es
Un marco interactivo en cascada de aprendizaje profundo con refinamiento experto para una segmentación precisa de subregiones estriatales
Por qué importa cartografiar regiones cerebrales minúsculas
El estriado, una estructura pequeña y profunda del cerebro, desempeña un papel central en el movimiento y la motivación y se ve fuertemente afectada en trastornos como la enfermedad de Parkinson. Los médicos suelen usar exploraciones PET y RM para medir cambios químicos en esta zona, pero el estriado se divide en muchas subregiones diminutas que son difíciles de ver y delinear con precisión. Este artículo presenta un nuevo método asistido por ordenador, llamado StriaSeg‑iARM, que ayuda a los especialistas a trazar estos límites con mayor precisión y eficiencia, incluso en personas cuyos cerebros están alterados por la edad o la enfermedad.
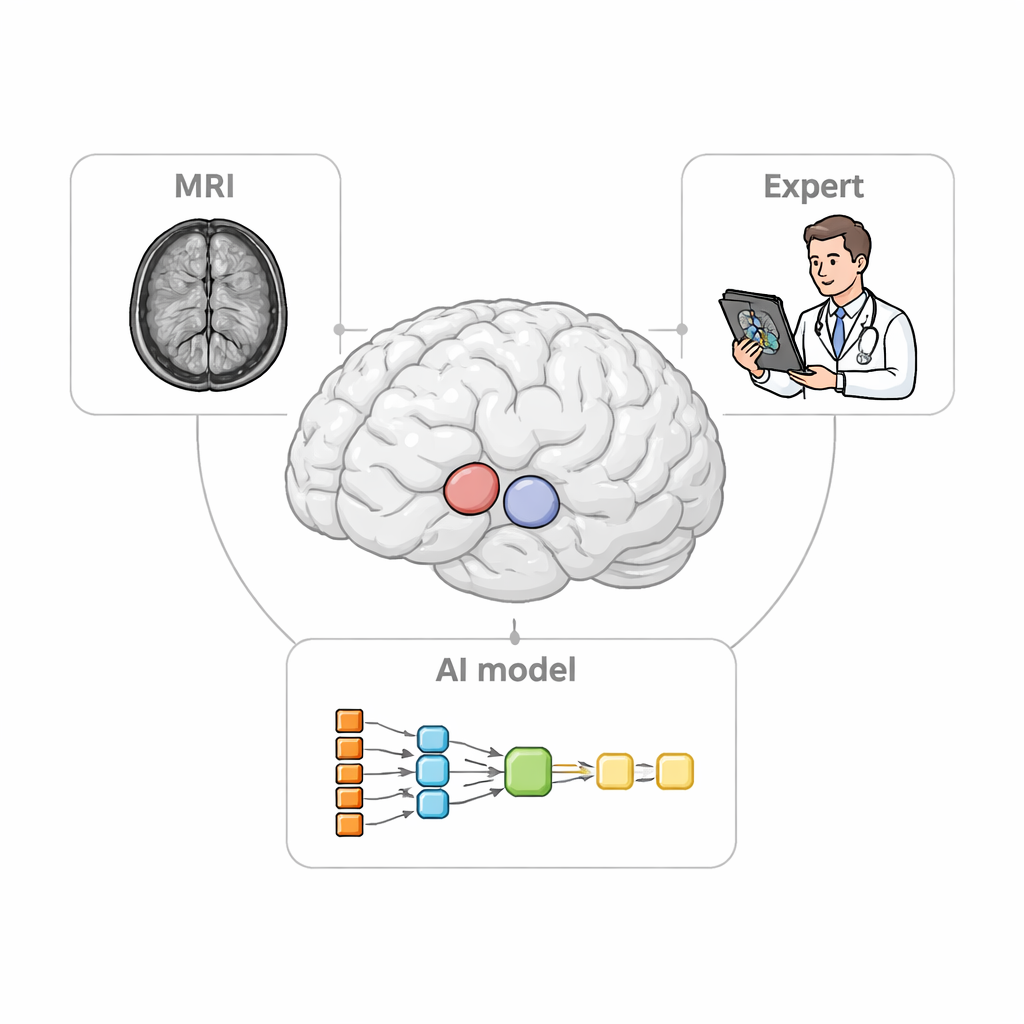
El problema clínico a la vista
Cuando los neurólogos evalúan condiciones como la enfermedad de Parkinson, se apoyan en escáneres PET para seguir cómo varían las señales relacionadas con la dopamina en distintas partes del estriado. Para hacerlo correctamente, deben primero definir pequeñas “regiones de interés” tridimensionales en la RM, que actúan como vasos medidores para los datos PET. Delinear manualmente estas regiones es una tarea lenta y tediosa y puede variar entre expertos. El software existente solo puede localizar automáticamente las estructuras más grandes y a menudo tiene dificultades en pacientes cuyos cerebros están encogidos o distorsionados, una situación común en enfermedad neurodegenerativa avanzada. Estas limitaciones pueden difuminar el patrón real de daño y debilitar la utilidad del uso de la imagen como herramienta diagnóstica.
Un asistente más inteligente en dos pasos
Los investigadores diseñaron StriaSeg‑iARM como un sistema de aprendizaje profundo en dos etapas que trabaja directamente en el espacio cerebral de cada persona en lugar de forzar la exploración a un molde estándar. En la primera etapa, el programa localiza el estriado global en una RM tridimensional. En la segunda etapa, divide esta estructura en 12 subregiones anatómicas definidas en ambos lados del cerebro. Entre estas dos etapas yace la innovación clave: un paso interactivo en el que un experto puede comprobar rápidamente y, si es necesario, corregir el contorno grosero producido por la primera etapa antes de ejecutar la subdivisión más fina. Este enfoque combina la rapidez de la automatización con el criterio de un observador humano entrenado.
Entrenamiento y pruebas en cerebros del mundo real
Para enseñar al sistema qué buscar, el equipo reunió cientos de exploraciones RM de varios hospitales y tipos de escáner, y creó delineados manuales cuidadosos de las 12 subregiones estriatales. Luego probaron el modelo en dos conjuntos de datos externos que incluían tanto RM como PET relacionados con la dopamina: uno de pacientes con Parkinson en fases relativamente tempranas y voluntarios sanos, y otro de un grupo clínico mayor y más afectado, con encogimiento cerebral marcado y diagnósticos mixtos. En estos casos desafiantes, StriaSeg‑iARM igualó de forma consistente los trazados manuales de expertos mejor que los métodos basados en atlas tradicionales y un modelo de aprendizaje profundo de una sola etapa, con mayor solapamiento, contornos más precisos y medidas de volumen estables.
Mediciones más nítidas para exploraciones químicas cerebrales
Puesto que el objetivo final es cuantificar las señales PET, los autores también examinaron cómo los distintos métodos de segmentación afectaban las lecturas PET. Usando una medida estándar de la unión del trazador en cada subregión, compararon los resultados automáticos con los basados en delineados manuales. El método por atlas tendía a subestimar la unión, especialmente en pacientes con cambios más severos, mientras que el modelo básico de aprendizaje profundo aún mostraba sesgos notables en algunas regiones. En contraste, los modelos en cascada —especialmente cuando se usaba el paso interactivo de corrección— produjeron valores PET que seguían de cerca la referencia experta, con sesgo y dispersión mínimos. El equipo mostró además que una puntuación simple de incertidumbre de la primera etapa puede señalar alrededor de una cuarta parte de los casos más difíciles en los que el refinamiento experto es realmente necesario, manteniendo el resto totalmente automático.
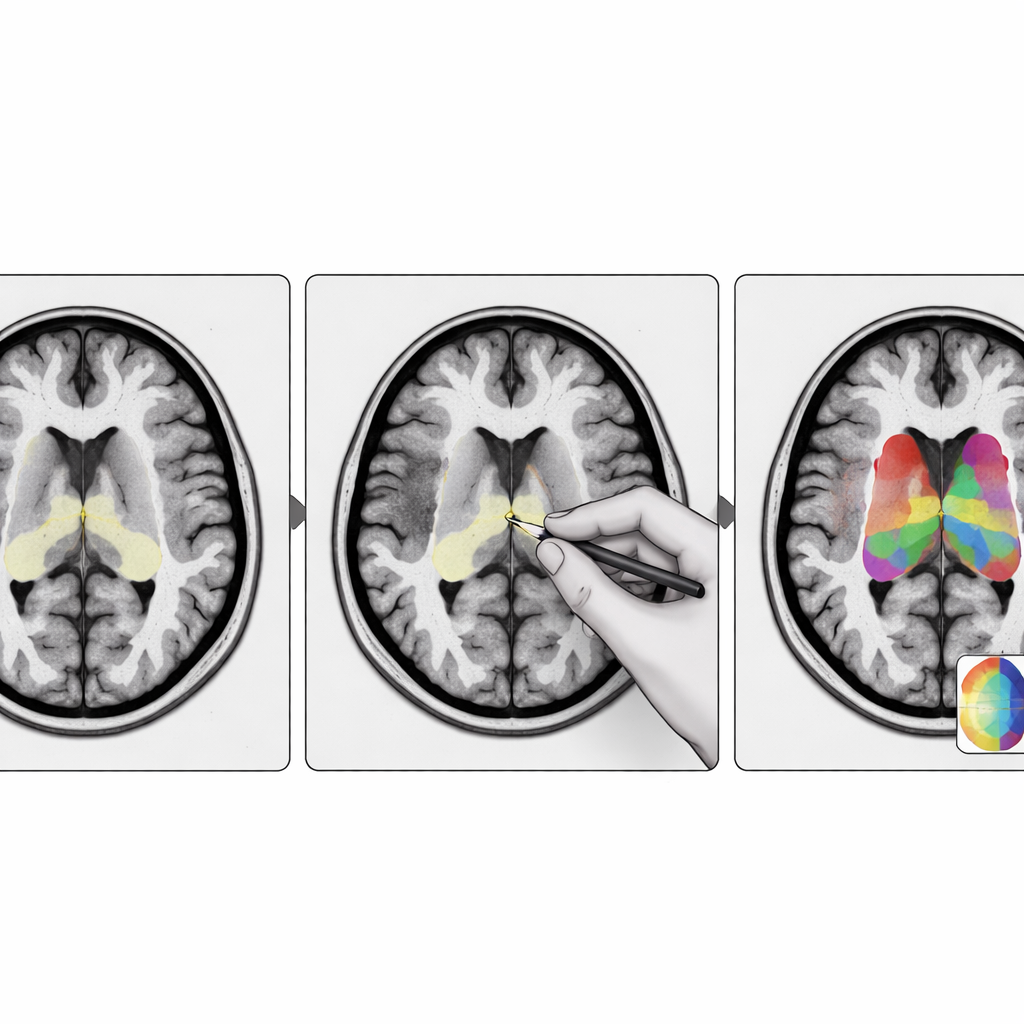
Qué significa esto para pacientes y clínicos
Para los no especialistas, la conclusión es que mapas digitales mejores de pequeñas regiones cerebrales pueden hacer que las exploraciones químicas del cerebro sean más fiables. StriaSeg‑iARM ofrece un marco flexible en el que un modelo de aprendizaje profundo realiza la mayor parte del trabajo, pero los especialistas aún pueden intervenir para corregir los casos complejos sin necesidad de reentrenar el sistema. Esta combinación de automatización y supervisión experta mejora la precisión de las mediciones usadas para diagnosticar y seguir trastornos como la enfermedad de Parkinson, y podría adaptarse a otros órganos y enfermedades donde estructuras pequeñas y difíciles de ver contienen pistas vitales.
Cita: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
Palabras clave: imagenología de la enfermedad de Parkinson, segmentación del estriado, aprendizaje profundo en radiología, PET y RM cerebral, biomarcadores neurodegenerativos