Clear Sky Science · es
Una cepa de Staphylococcus capitis que produce dos bacteriocinas, capidermicina y micrococcina P1, muestra actividad antimicrobiana de amplio espectro
Por qué las bacterias diminutas de la piel importan frente a las amenazas de supergérmenes
Las infecciones resistentes a los antibióticos están aumentando en todo el mundo y los médicos se están quedando sin fármacos fiables. Una idea prometedora es reclutar a nuestros propios microbios "buenos" para que ayuden a combatir a los patógenos. Este estudio se centra en una bacteria cutánea común, Staphylococcus capitis, y muestra que una cepa particular, denominada HBC3, produce de forma natural dos moléculas antimicrobianas potentes. Juntas, estas moléculas pueden abatir patógenos peligrosos de hospitales, incluido el Staphylococcus aureus resistente a meticilina (MRSA), lo que sugiere que las bacterias amistosas de la piel podrían convertirse en herramientas futuras para combatir infecciones.
Un residente de la piel con poder oculto
S. capitis vive normalmente de forma silenciosa en nuestra piel, especialmente en el cuero cabelludo, y suele ser inofensiva. Los investigadores cribaron 18 cepas de S. capitis recogidas de las fosas nasales de personas para ver si alguna podía inhibir MRSA, una causa importante de infecciones difíciles de tratar. Una cepa, HBC3, destacó. En pruebas de laboratorio, suprimió con fuerza una amplia variedad de bacterias Gram positivas, incluido MRSA, enterococos resistentes a la vancomicina (VRE), Streptococcus pyogenes, Listeria monocytogenes y especies de Bacillus y Clostridium que pueden causar enfermedades graves. Cabe señalar que no mostró efecto sobre varias bacterias Gram negativas comunes como Escherichia coli y Klebsiella pneumoniae, lo que sugiere una acción focalizada pero potente en lugar de una matanza indiscriminada. 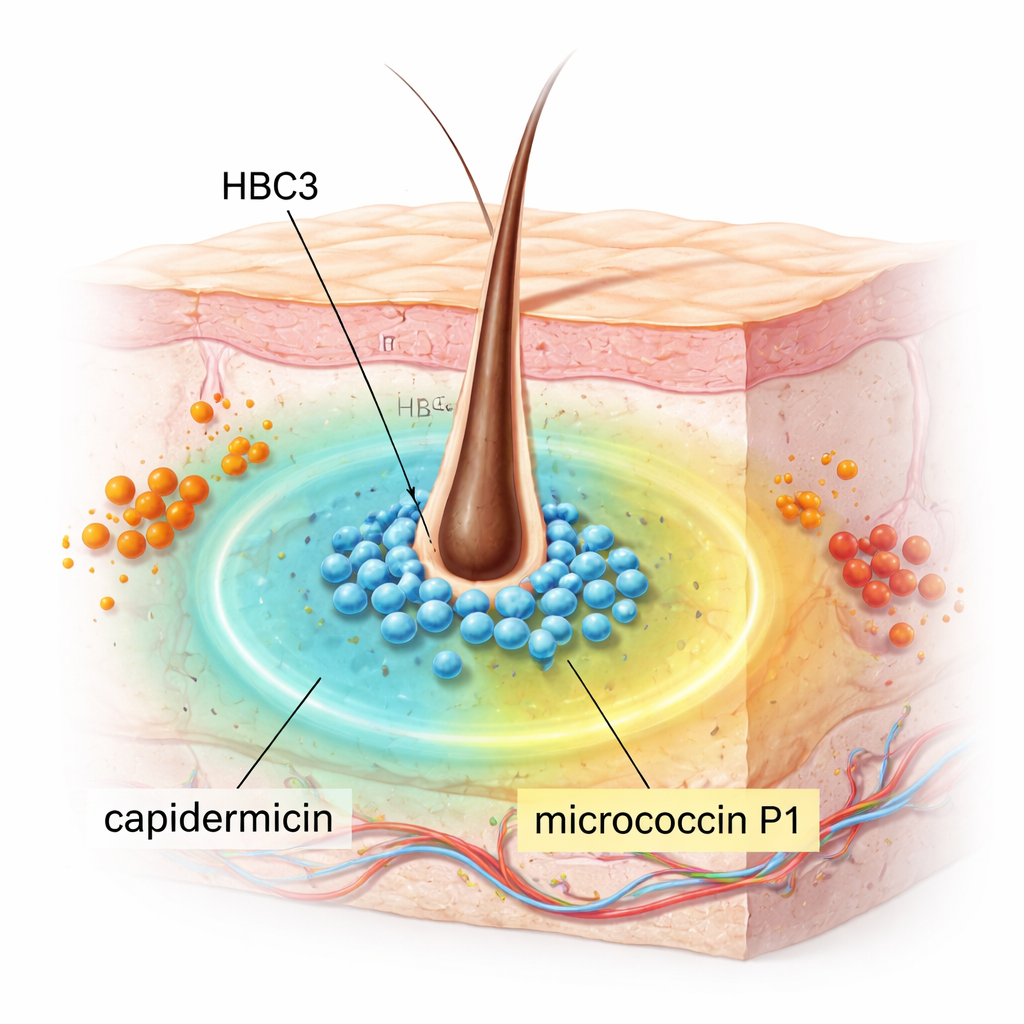
Dos antibióticos naturales en un solo “mini-cromosoma” genético
Para descubrir cómo HBC3 ejerce este potente efecto antimicrobiano, el equipo decodificó su genoma completo. Identificaron un pequeño elemento de ADN circular, un plásmido llamado pHBC3_1, que contiene las instrucciones completas para fabricar dos bacteriocinas diferentes: péptidos naturales similares a antibióticos producidos por bacterias. Una es la capidermicina, un pequeño péptido cargado positivamente ya observado en otras cepas de S. capitis. La otra es la micrococcina P1 (MP1), una tiopeptida que bloquea la síntesis proteica en las bacterias diana y que no se había reportado antes en S. capitis. Cuando se eliminó este plásmido de HBC3, la cepa perdió completamente su actividad antibacterial, lo que confirma que estos genes son esenciales para sus capacidades defensivas.
Dianas diferentes, objetivo compartido
Al purificar cada bacteriocina por separado, los científicos evaluaron su capacidad para inhibir diversos microbios. MP1 mostró una actividad amplia y potente contra muchos cocos Gram positivos, incluido MRSA y enterococos, a bajas concentraciones. La capidermicina, en contraste, fue más eficaz contra bacilos Gram positivos como Bacillus coagulans y Listeria, pero tuvo un efecto débil o nulo sobre estafilococos en las condiciones empleadas aquí. Cuando el equipo combinó ambos péptidos contra B. coagulans observaron un efecto aditivo: dosis más bajas en conjunto lograron una inhibición del crecimiento más fuerte que cualquiera de los dos por separado. Esta orientación complementaria permite a HBC3 suprimir una gama más amplia de rivales desplegando dos armas moleculares distintas ajustadas a diferentes formas bacterianas y superficies celulares. 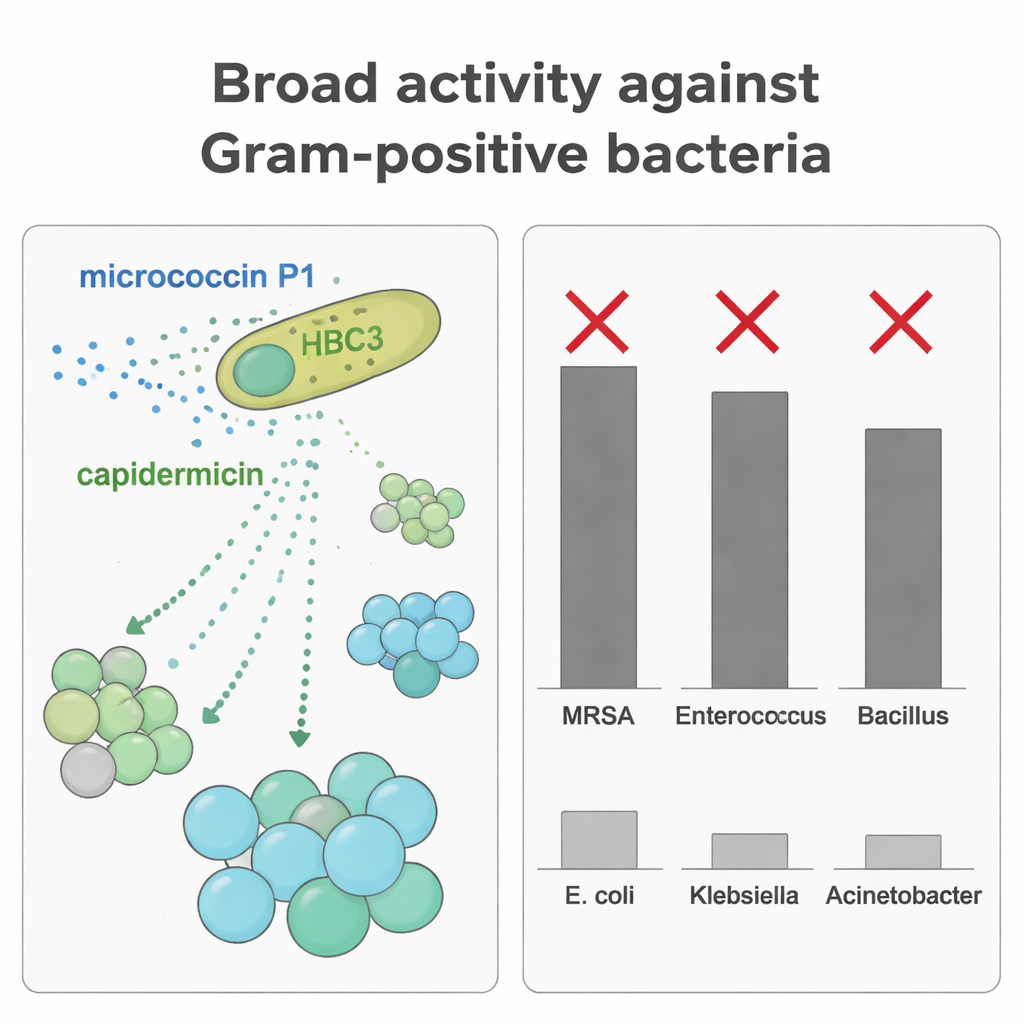
Ganar espacio en vecindarios microbianos concurridos
Para imitar la competencia en la vida real, los investigadores co-cultivaron HBC3 con MRSA, VRE y B. coagulans en las mismas placas. La cepa HBC3 normal eliminó casi por completo estos patógenos de las comunidades mixtas, mientras que una versión sin el plásmido les permitió prosperar. Comparaciones genéticas sugieren que el plásmido con las dos bacteriocinas probablemente surgió de fusiones y reorganizaciones pasadas de plásmidos separados, facilitadas por elementos de ADN móvil que pueden mover grupos de genes entre bacterias. Este plásmido compuesto confiere a HBC3 una ventaja clara en entornos concurridos como la piel o las mucosas, donde muchos microbios compiten por nutrientes y espacio.
¿De aliado cutáneo a probiótico del futuro?
El estudio concluye que S. capitis HBC3 está equipado con la rara combinación de dos bacteriocinas distintas en un mismo plásmido, lo que le permite inhibir con fuerza a múltiples patógenos Gram positivos clínicamente importantes, incluidas cepas resistentes a antibióticos. Dado que la propia HBC3 no pertenece a una línea de alto riesgo conocida y no porta genes de resistencia a fármacos detectables, podría ser candidata para desarrollarse como probiótico dirigido o agente de descolonización —diseñado, por ejemplo, para reducir selectivamente S. aureus en la piel o en la nariz mientras preserva vecinos más benignos. Antes de que tales aplicaciones sean realidad, será necesario evaluar con cuidado la seguridad, la eficacia en animales y humanos y los impactos a largo plazo sobre la microbiota normal, pero el trabajo pone de relieve cómo nuestros propios microbios pueden ayudar a contrarrestar la crisis continua de los supergérmenes.
Cita: Ohdan, K., Suzuki, Y., Kawada-Matsuo, M. et al. Staphylococcus capitis strain producing dual bacteriocins, capidermicin and micrococcin P1, shows broad-spectrum antimicrobial activity. Sci Rep 16, 6835 (2026). https://doi.org/10.1038/s41598-026-36393-6
Palabras clave: bacteriocinas, Staphylococcus capitis, micrococcina P1, capidermicina, resistencia a antibióticos