Clear Sky Science · es
Implementación del enfoque de cribado virtual de alto rendimiento (HTVS) para la identificación de nuevos inhibidores de la lactato deshidrogenasa (LDH) con propiedades anticancerígenas
Por qué esta investigación importa para el tratamiento del cáncer
Las células cancerosas a menudo reprograman su producción de energía, y ese cambio puede explotarse para diseñar fármacos más inteligentes y selectivos. Este estudio explora una enzima metabólica clave llamada lactato deshidrogenasa (LDH), que ayuda a los tumores a prosperar en condiciones adversas y a resistir el tratamiento. Mediante cribado computacional avanzado y pruebas de laboratorio, los investigadores identificaron dos nuevas pequeñas moléculas que bloquean la LDH y muestran efectos anticancerígenos prometedores en líneas celulares de cáncer de próstata.
El extraño metabolismo de las células cancerosas
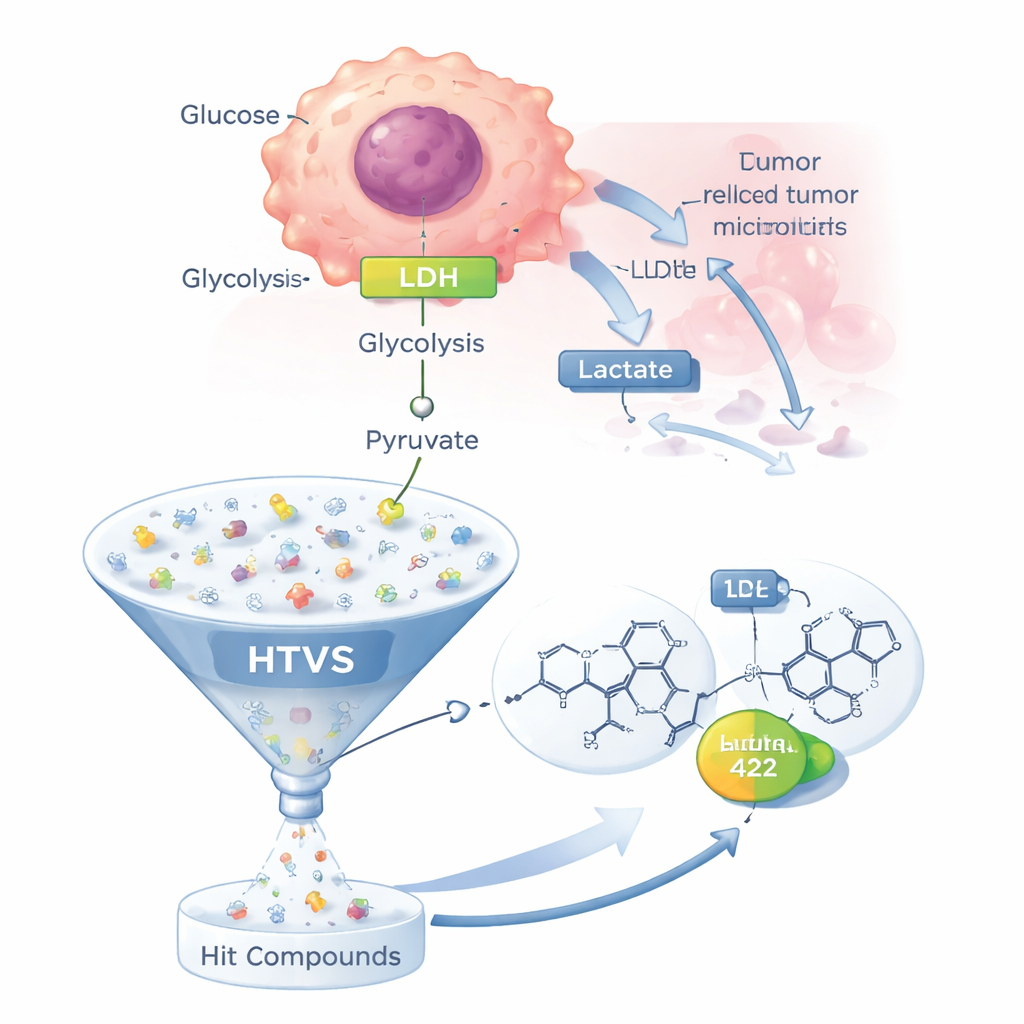
La mayoría de las células sanas usan el oxígeno de manera eficiente en sus mitocondrias para generar energía. Sin embargo, muchas células cancerosas dependen en gran medida de una vía menos eficiente llamada glucólisis, incluso cuando el oxígeno es abundante —un fenómeno conocido como el efecto Warburg. En esta vía abreviada, la glucosa se descompone hasta piruvato, que luego es convertido en lactato por la LDH en lugar de ser enviado a las mitocondrias. El lactato se expulsa de la célula, acidificando el entorno tumoral, lo que ayuda a las células cancerosas a eludir la muerte celular, debilitar el ataque inmune e incluso reducir la eficacia de muchos fármacos quimioterápicos. Dado que la LDH se sitúa en el corazón de este metabolismo alterado y aún no existe un fármaco aprobado dirigido a la LDH, se ha convertido en un objetivo prioritario para nuevas terapias anticancerígenas.
Usar ordenadores para filtrar medio millón de moléculas
En lugar de probar posibles fármacos uno por uno en el laboratorio, el equipo empleó una estrategia de cribado virtual de alto rendimiento (HTVS). Comenzaron con 28 moléculas que bloquean la LDH ya reportadas en la literatura científica y a partir de ellas derivaron un "farmacóforo": un patrón tridimensional abstracto de rasgos que cualquier buen inhibidor de la LDH probablemente comparta. Aplicaron este modelo a una biblioteca comercial de aproximadamente 500.000 moléculas con características de fármacos, buscando qué candidatos coincidían con los rasgos esenciales. Aproximadamente 110.000 moléculas superaron este primer filtro, y una selección adicional basada en reglas estándar de "afinidad a fármaco" redujo la lista a 2.337 candidatos más realistas para el acoplamiento (docking) con la enzima LDH.
Acercándose a los mejores ligandos
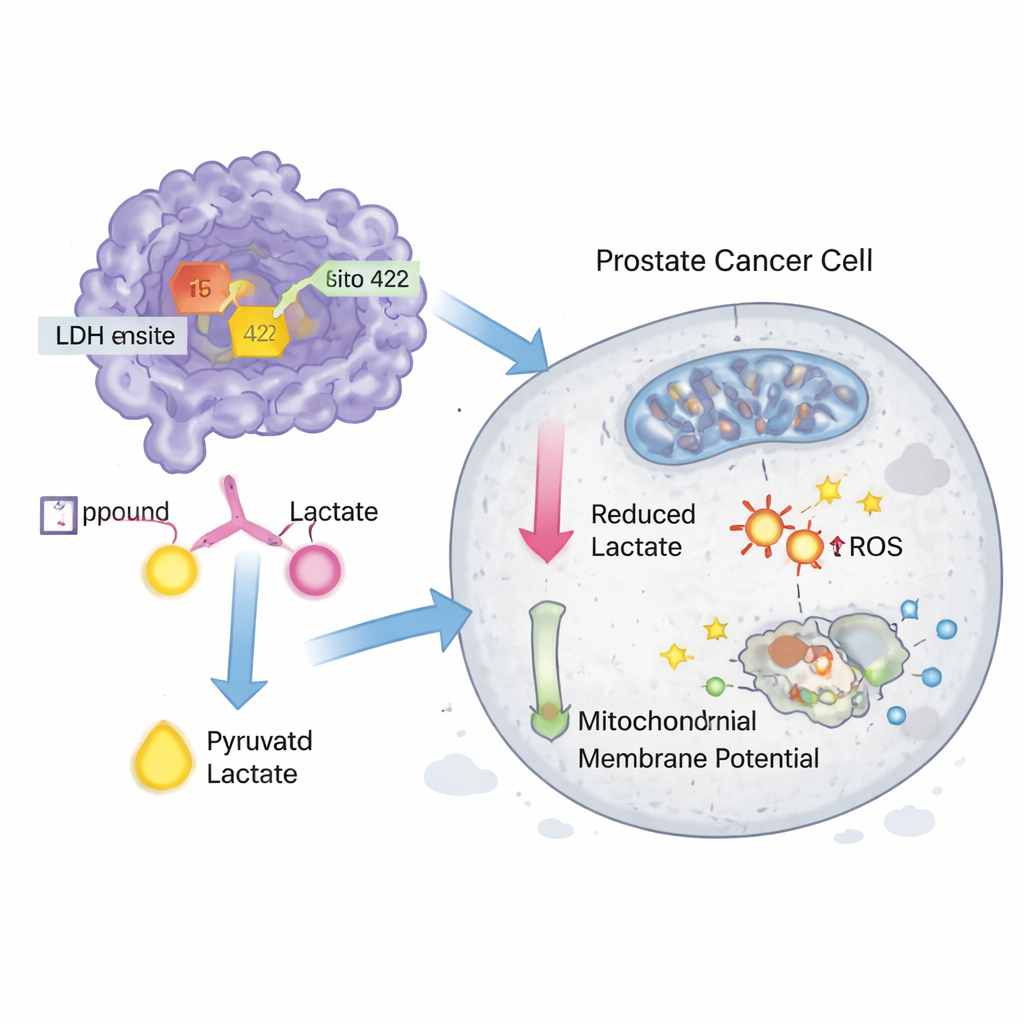
El siguiente paso fue estimar con qué fuerza estos candidatos podrían encajar en el sitio activo de la LDH. Usando varios niveles de acoplamiento computacional, los investigadores calcularon cómo podría interactuar cada molécula con aminoácidos específicos dentro del bolsillo enzimático. Este proceso por etapas redujo progresivamente el conjunto desde miles de candidatos hasta solo 59 moléculas prometedoras, y luego a cinco claros "hits" con una afinidad predicha especialmente alta. Dos de ellas, denominadas compuestos 15 y 422, destacaron porque simulaciones de dinámica molecular basadas en ordenador sugirieron que forman complejos inusualmente estables con la LDH a lo largo del tiempo, manteniendo contactos clave con residuos críticos en el sitio activo mientras preservan una estructura proteica razonable en general.
Del cribado a células cancerosas reales
Para comprobar si estos hits tenían efecto en sistemas vivos, los científicos compraron los compuestos 15 y 422 y los probaron en líneas celulares de cáncer de próstata DU-145 y PC-3. Ambas moléculas inhibieron la actividad de la LDH en células a concentraciones nanomolares y también ralentizaron directamente la actividad de una LDH purificada, aunque fueron algo menos potentes que un inhibidor experimental conocido llamado GNE‑140. En ensayos de crecimiento, los compuestos redujeron la supervivencia de las células cancerosas a dosis bajas en micromolar, acercándose nuevamente al rendimiento de GNE‑140. Experimentos adicionales mostraron que los tratamientos aumentaron ligeramente el estrés oxidativo, alteraron el potencial de membrana mitocondrial —un signo de compromiso de las fábricas de energía— y desencadenaron la muerte celular programada (apoptosis) en células DU‑145, siendo el compuesto 15 el más activo de los dos.
Qué podría significar esto para futuros fármacos contra el cáncer
Si bien estas moléculas no son medicamentos listos para usar, proporcionan puntos de partida valiosos para el diseño de fármacos. Tanto los compuestos 15 como 422 presentan propiedades químicas que sugieren mejor solubilidad, permeabilidad y una mayor "afinidad a fármaco" en general que algunos inhibidores de LDH existentes, lo que los convierte en candidatos atractivos para una mayor optimización. El estudio demuestra cómo el cribado informático a gran escala, orientado por características estructurales conocidas, puede descubrir nuevos inhibidores de LDH que debilitan a las células cancerosas privándolas de su suministro energético alterado. Con trabajos futuros para refinar sus estructuras, probar la unión directa con mayor rigor y estudiar su comportamiento en modelos animales, estos compuestos podrían contribuir a una nueva clase de agentes anticancerígenos que ataquen a los tumores a través de sus vulnerabilidades metabólicas únicas.
Cita: Huang, Y., Benni, S., Yadav, U.P. et al. Deploying the high-throughput virtual screening (HTVS) approach for the identification of new lactate dehydrogenase (LDH) inhibitors with anticancer assets. Sci Rep 16, 5921 (2026). https://doi.org/10.1038/s41598-026-36385-6
Palabras clave: inhibidores de la lactato deshidrogenasa, metabolismo del cáncer, cribado virtual, cáncer de próstata, descubrimiento de fármacos anticancerígenos