Clear Sky Science · es
La regulación a la baja de CDC25C suprime el crecimiento del CHC mediante autophagia y apoptosis inducidas por estrés mitocondrial
Por qué importa este estudio sobre cáncer de hígado
El cáncer de hígado es uno de los más letales en todo el mundo y muchos pacientes se diagnostican demasiado tarde para que la cirugía o los tratamientos convencionales funcionen bien. Este estudio explora un único “interruptor” celular, una proteína llamada CDC25C, que parece impulsar el crecimiento del cáncer de hígado mientras resulta menos crítica para las células hepáticas sanas. Al bajar la actividad de este interruptor, los investigadores observaron que podían estresar y, en última instancia, eliminar las células cancerosas mediante los propios sistemas de autolimpieza y autodestrucción de la célula, lo que apunta a una estrategia terapéutica prometedora y más selectiva.
Un interruptor de crecimiento dentro de los tumores hepáticos
Toda célula debe decidir cuándo dividirse y cuándo detenerse. CDC25C es una de las proteínas clave que empujan a las células a través del ciclo de división. En el cáncer de hígado, este interruptor a menudo queda atascado en la posición de “encendido”, ayudando a los tumores a crecer y diseminarse. El equipo utilizó células de cáncer de hígado de ratón y células hepáticas normales de ratón, así como ratones portadores de tumores, para reducir artificialmente los niveles de CDC25C. Confirmaron, mediante pruebas genéticas y de proteína estándar, que CDC25C se redujo notablemente en su grupo experimental en comparación con los controles, estableciendo un modelo sólido para estudiar qué ocurre cuando este interruptor de crecimiento se atenúa.
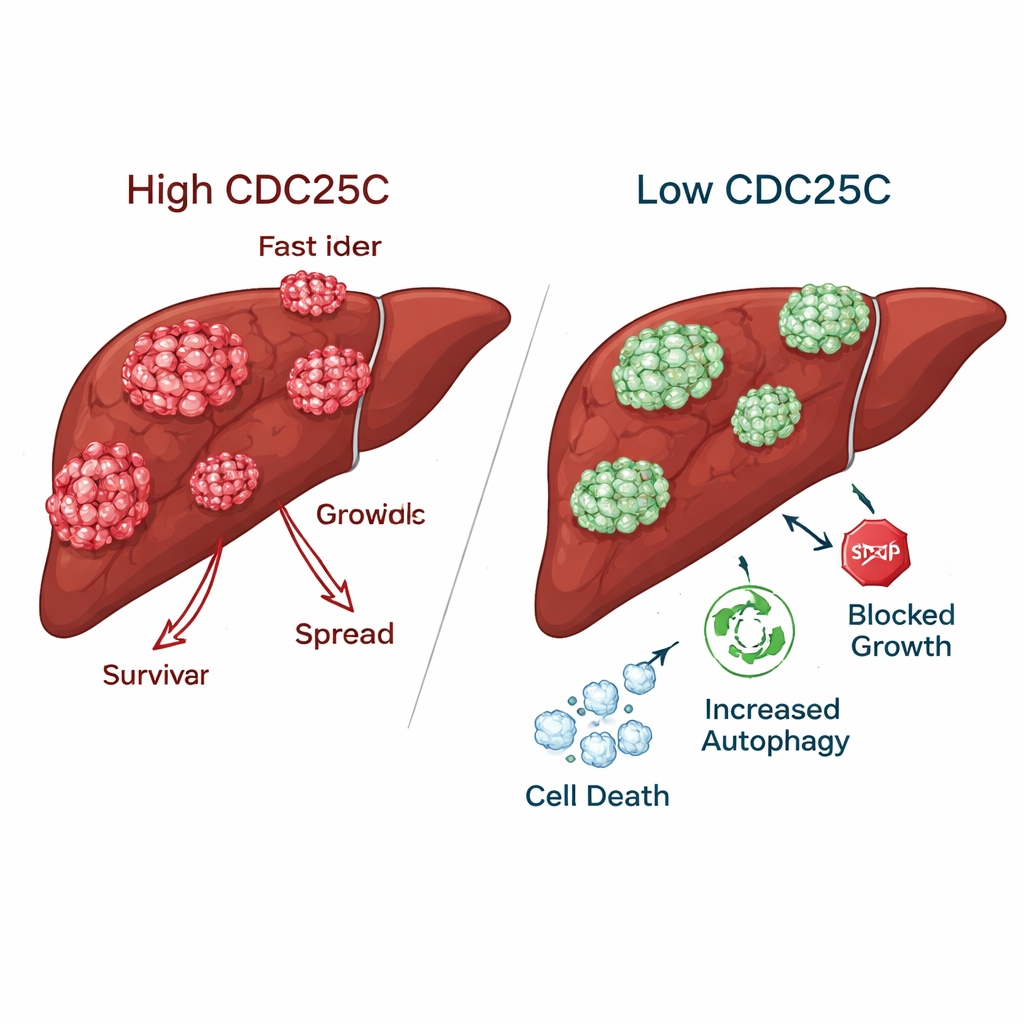
Frenar el cáncer mientras se preservan las células hepáticas sanas
Cuando CDC25C se redujo en las células de cáncer hepático, los tumores perdieron muchas de sus características agresivas. Las células cancerosas formaron muchas menos colonias, migraron más despacio a través de “heridas” artificiales y tuvieron menor capacidad para atravesar e invadir barreras en pruebas de laboratorio. En contraste, las células hepáticas normales mostraron incluso un mejor crecimiento y movimiento cuando CDC25C se redujo, lo que sugiere que el tejido sano puede tolerar o incluso beneficiarse de la inhibición de CDC25C. En ratones, los tumores diseñados con reducción de CDC25C mostraron niveles más bajos de esta proteína en mediciones tanto de gen como de proteína, confirmando que el mismo efecto ocurrió en animales vivos.
Estrés de las centrales energéticas y el equipo de limpieza celular
Al mirar dentro de las células con microscopios electrónicos, los investigadores observaron que las células cancerosas con baja CDC25C contenían mitocondrias hinchadas y dañadas —las pequeñas centrales energéticas de la célula— junto con estructuras en forma de burbuja llamadas autofagosomas que señalan la activación del sistema interno de reciclaje celular, la autofagia. Luego midieron signos clave de estrés mitocondrial: los niveles de calcio y las especies reactivas de oxígeno (ROS), ambos elevados en las células cancerosas tras la reducción de CDC25C. Los marcadores de la respuesta al estrés mitocondrial, incluidas proteínas ayudantes como HSP60 y dos enzimas mitocondriales de “control de calidad”, también aumentaron, al igual que CHOP, un factor relacionado con el estrés que enlaza los problemas mitocondriales con respuestas celulares más amplias. De forma llamativa, estas señales de estrés se movieron en la dirección opuesta en las células hepáticas normales, reforzando la idea de que las células cancerosas y las sanas responden de forma muy diferente a la pérdida de CDC25C.
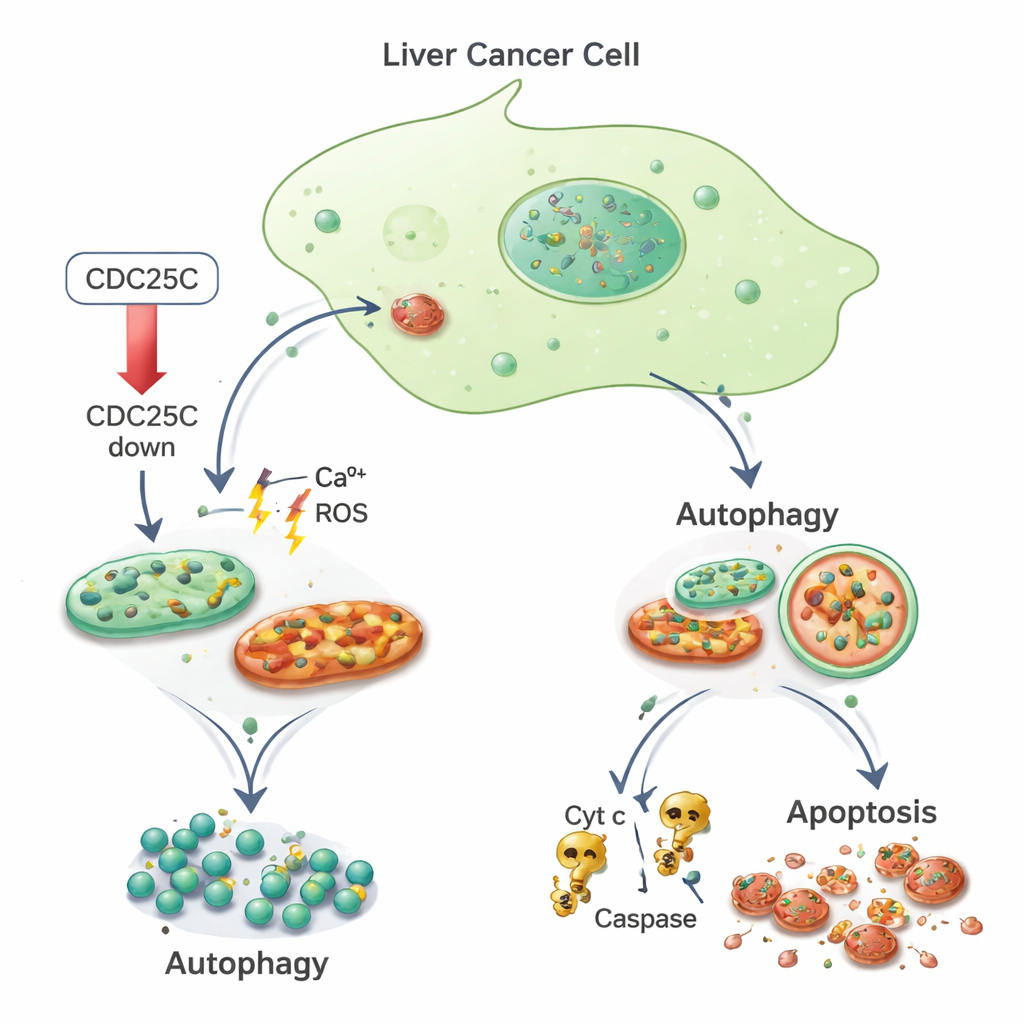
Del estrés a la autodestrucción y la muerte celular
El equipo preguntó a continuación cómo estaban afrontando estas células cancerosas estresadas. Encontraron que los marcadores de autofagia aumentaron tanto en las células cancerosas como en las células hepáticas normales cuando CDC25C se redujo. Proteínas como LC3 y p62, que reflejan la formación y actividad de autofagosomas, se incrementaron, lo que indica que las células activaron su maquinaria de limpieza. Al mismo tiempo, solo en las células cancerosas, el daño mitocondrial parece empujar a las células más allá de la reparación y hacia la muerte programada. Usando colorantes fluorescentes y citometría de flujo, los investigadores observaron más células cancerosas con núcleos fragmentados y fuertemente teñidos —un sello de la apoptosis— y una reducción del potencial de membrana mitocondrial. También hallaron niveles aumentados de citocromo c y de las enzimas caspasa-3 y caspasa-9, componentes clásicos de la vía de muerte mediada por mitocondrias. Por el contrario, las células hepáticas normales mostraron menos apoptosis bajo las mismas condiciones de reducción de CDC25C.
Qué podría significar esto para tratamientos futuros
Para un lector general, el mensaje clave es que bajar CDC25C parece afectar a las células de cáncer de hígado en su punto débil: sobrecargar sus centrales energéticas, llevar sus sistemas de reciclaje al límite y, finalmente, desencadenar una autodestrucción ordenada —mientras que en su mayoría se preservan las células hepáticas normales. Los autores concluyen que CDC25C es más que un simple interruptor de crecimiento; también moldea cómo las células manejan el estrés, la limpieza y la muerte. Dado que las células cancerosas dependen en gran medida de CDC25C y responden a su pérdida con un estrés mitocondrial fatal y apoptosis, fármacos que apunten a esta proteína, o a las vías de estrés que ella regula, podrían algún día ofrecer una forma más selectiva de tratar el cáncer de hígado con menos daño para el tejido hepático sano.
Cita: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
Palabras clave: carcinoma hepatocelular, CDC25C, estrés mitocondrial, autofagia, apoptosis