Clear Sky Science · es
TET1 suprime la progresión del carcinoma hepatocelular modulando las vías de señalización PI3K/Akt
Por qué una enzima hepática importa para el cáncer
El cáncer primario de hígado, especialmente un tipo llamado carcinoma hepatocelular, es uno de los cánceres más letales a nivel mundial. Muchos pacientes se diagnostican demasiado tarde para una cirugía curativa, y los fármacos disponibles solo benefician a una fracción de ellos. Este estudio explora una molécula llamada TET1, una enzima que edita marcas químicas en el ADN, para plantear una pregunta sencilla pero vital: ¿favorece TET1 el crecimiento de los tumores hepáticos y podría convertirse en un nuevo objetivo terapéutico?
Un editor oculto en nuestro ADN
Nuestros genes no están controlados solo por el código del ADN, sino también por marcas químicas que activan o desactivan genes. Una marca común es la metilación del ADN, que actúa como un regulador de intensidad de la actividad génica. TET1 forma parte de una familia de enzimas que borran o remodelan estas marcas, ayudando a las células a responder al entorno y a mantener su función normal. Cuando este sistema falla, las células pueden derivar hacia estados patológicos, incluido el cáncer. Investigaciones anteriores mostraron que TET1 puede tanto frenar como acelerar el crecimiento tumoral según el tejido, pero su papel exacto en el cáncer hepático humano seguía siendo poco claro y objeto de debate.
Los niveles de TET1 se disparan en los tumores hepáticos
Para averiguar qué hace TET1 en el cáncer de hígado, los investigadores recurrieron primero a grandes bases de datos públicas de expresión génica y luego a muestras de pacientes. En varios tipos de cáncer, los niveles de TET1 fueron inusualmente altos en diversos tumores, incluido el de hígado. Centrándose en los tumores hepáticos, compararon tejido tumoral con hígado no canceroso cercano del mismo paciente. En ocho pares emparejados, la proteína TET1 fue consistentemente más alta en el tumor. Conjuntos de datos públicos de cientos de pacientes contaron la misma historia a nivel de ARN: los cánceres de hígado tenían más TET1 que los hígados sanos o los hígados con solo fibrosis. Los pacientes cuyos tumores mostraban niveles elevados de TET1 tendían a presentar enfermedad más avanzada y una supervivencia global y libre de enfermedad más corta, lo que sugiere que TET1 se asocia tanto con la agresividad tumoral como con un pronóstico peor.
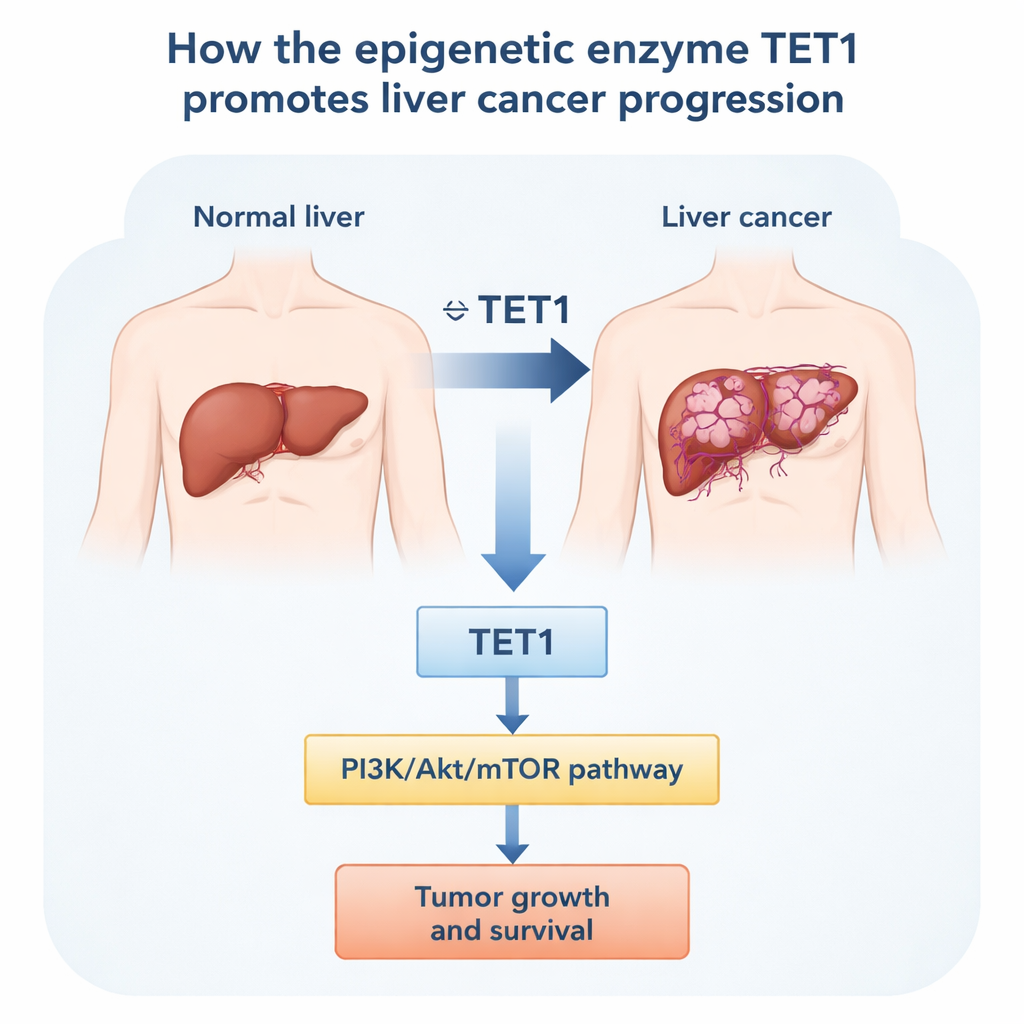
Reducir TET1 frena las células tumorales
A continuación, el equipo investigó qué ocurre cuando se disminuye TET1 dentro de células de carcinoma hepatocelular cultivadas en el laboratorio. Utilizando pequeños fragmentos de ARN para silenciar el gen TET1, redujeron drásticamente los niveles de TET1 en varias líneas celulares humanas de cáncer de hígado, incluidas las que presentan alteraciones asociadas al virus de la hepatitis B. Una vez suprimido TET1, las células se dividieron más lentamente, formaron menos colonias y mostraron signos claros de estrés. Experimentos por citometría de flujo revelaron que más células quedaban bloqueadas en la fase temprana “G1” del ciclo celular, en lugar de avanzar hacia la división. Al mismo tiempo, la fracción de células que experimentaban muerte programada, o apoptosis, aumentó notablemente. Estos efectos se observaron tanto en líneas típicas de cáncer hepático como en una línea positiva para VHB, indicando que TET1 ayuda a sostener la supervivencia y el crecimiento continuo en distintos contextos de cáncer de hígado.
Una vía de crecimiento bajo el control de TET1
Para desvelar cómo ejerce TET1 esta influencia, los investigadores analizaron qué genes cambiaban entre células hepáticas normales y células tumorales. Miles de genes eran distintos, y muchos de ellos se agruparon en circuitos conocidos de crecimiento y supervivencia. Una vía destacó: PI3K/Akt/mTOR, una cadena de señalización central que muchos cánceres utilizan para aumentar el metabolismo, resistir la muerte celular y eludir terapias. Los análisis de bases de datos mostraron que los niveles de TET1 aumentaban junto con componentes centrales de esta vía y disminuían en oposición a PTEN, un freno natural de la actividad PI3K/Akt. Cuando TET1 fue silenciado en células de cáncer hepático, las formas activadas, “fosforiladas”, de PI3K, Akt y especialmente mTOR se redujeron. El tratamiento de las células con un inhibidor químico que bloquea la actividad de la familia TET también redujo la fosforilación de Akt y mTOR. Estos resultados sugieren que la actividad enzimática de TET1 —su capacidad para remodelar las marcas del ADN— alimenta la cascada PI3K/Akt/mTOR, inclinando la balanza hacia el crecimiento y la supervivencia en lugar de la contención.
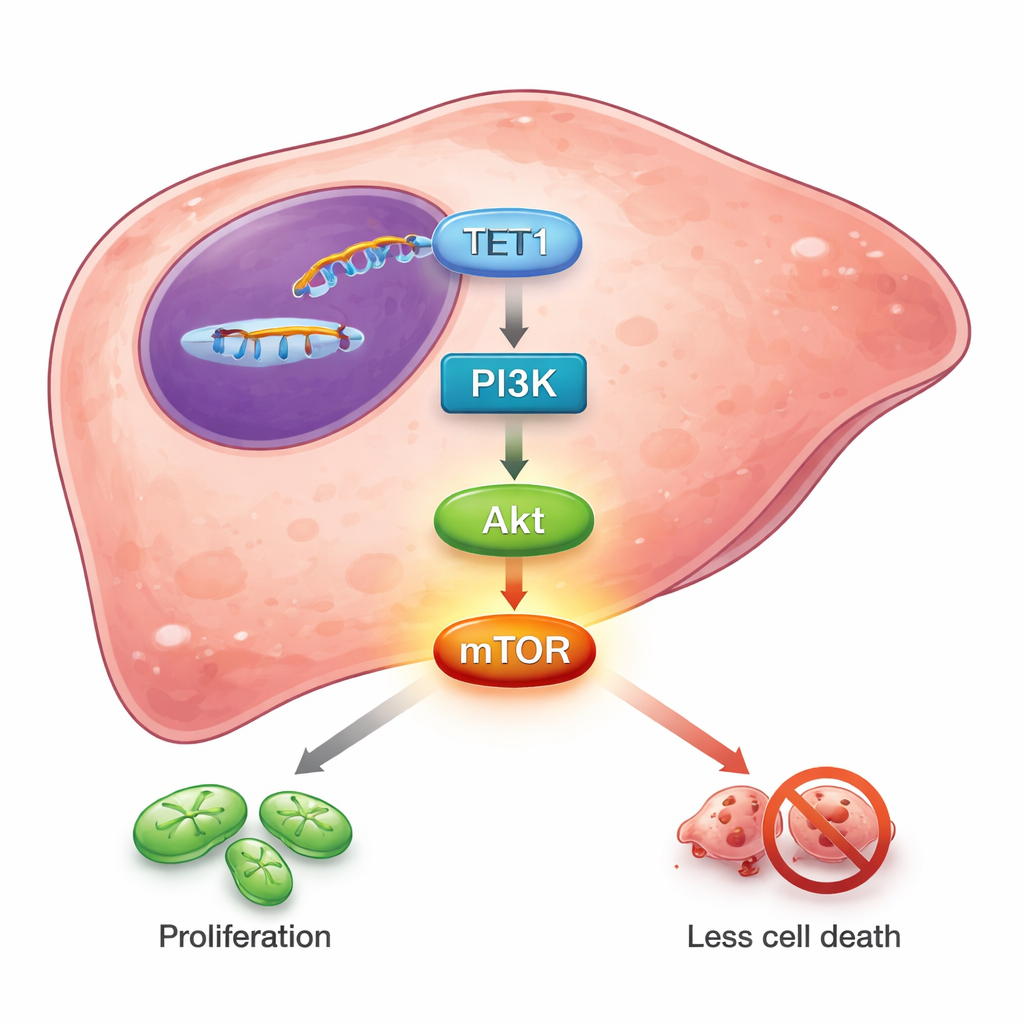
Del hallazgo molecular a posibles tratamientos
En conjunto, este trabajo describe a TET1 como un aliado clave de los tumores hepáticos más que como un guardián contra ellos. Un TET1 alto ayuda a las células de cáncer de hígado a proliferar y evitar la muerte, en parte manteniendo activada la vía PI3K/Akt/mTOR. En los pacientes, un mayor TET1 en los tumores va de la mano con enfermedad más avanzada y peores resultados. Para el lector general, el mensaje es que una enzima que edita discretamente las marcas químicas del ADN puede influir de forma decisiva en si las células de cáncer hepático sobreviven o mueren. Diseñar fármacos que inhiban TET1, o combinar estos fármacos con terapias dirigidas a PI3K/Akt, podría permitir en el futuro cortar una línea de apoyo crucial para los tumores hepáticos y mejorar la supervivencia de las personas con esta enfermedad tan desafiante.
Cita: Qi, S., Chen, M., Ding, Z. et al. TET1 suppresses hepatocellular carcinoma progression by modulating the PI3K/Akt signaling pathways. Sci Rep 16, 5791 (2026). https://doi.org/10.1038/s41598-026-36334-3
Palabras clave: cáncer de hígado, TET1, epigenética, PI3K Akt mTOR, carcinoma hepatocelular