Clear Sky Science · es
Reutilización de dapagliflozina mediante nanogeles poliméricos para la terapia del cáncer colorrectal
Por qué un fármaco para la diabetes podría ayudar a combatir el cáncer de colon
El cáncer colorrectal es una de las principales causas de mortalidad relacionada con el cáncer en todo el mundo, y muchos pacientes siguen recayendo a pesar de la cirugía y la quimioterapia. Este estudio explora un aliado inesperado contra esta enfermedad: la dapagliflozina, una pastilla habitual para la diabetes tipo 2. Al encapsular este fármaco en diminutas partículas blandas que se convierten en un gel suave en el estómago, los investigadores buscan entregar más cantidad al intestino grueso —donde crecen los tumores de colon— manteniendo al mismo tiempo una dosis oral similar a las tabletas existentes.
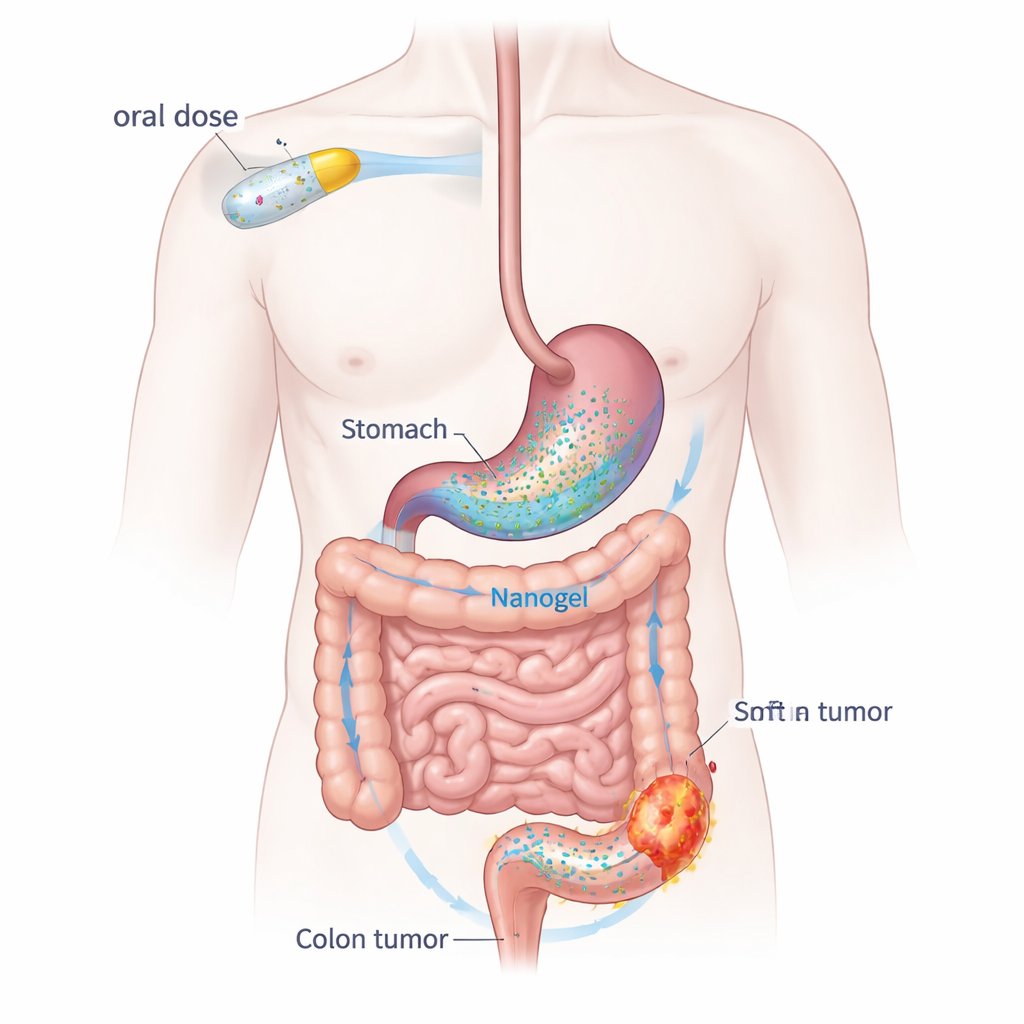
Convertir una pastilla cotidiana en una carga dirigida al cáncer
La dapagliflozina suele actuar en los riñones para reducir la glucosa en sangre, pero también atenúa la inflamación y ralentiza el crecimiento celular, dos procesos de los que dependen los cánceres. Sin embargo, por sí sola la droga se disuelve mal en agua y se elimina del organismo con rapidez. Para superar esto, el equipo construyó un sistema de liberación tipo “nanogel” usando dos polímeros similares a alimentos: alginato sódico, extraído de algas, y alcohol polivinílico, un espesante biocompatible de uso general. El fármaco queda atrapado dentro de nanopartículas de aproximadamente una diezmilésima de milímetro de ancho. Cuando estas partículas se encuentran con el ácido del estómago, se asientan y se entrelazan formando una masa hidrogelificada y blanda que perdura, liberando luego gradualmente el fármaco a medida que avanza hacia el colon.
Hacer el fármaco más soluble y más lento en desaparecer
Los científicos optimizaron primero cómo se fabricaban las partículas, ajustando la proporción de los dos polímeros para que las nanopartículas permanecieran pequeñas, con tamaño uniforme y estables en líquido. Confirmaron que el fármaco estaba bien integrado en la red polimérica y que se transformaba parcialmente de una forma cristalina a otra más amorfa, que por lo general se disuelve mejor. En líquidos de prueba que imitan los fluidos gástricos e intestinales, la formulación en nanogel aumentó la solubilidad aparente de la dapagliflozina en aproximadamente 1,7–1,8 veces en comparación con el fármaco en crudo. Al monitorizar la rapidez con la que el fármaco se liberaba, el nanogel mostró un perfil de liberación suave y sostenida durante varias horas, en lugar de la liberación rápida observada con el fármaco simple. Una receta en particular, denominada F2, formó un gel compacto y resistente que se mantuvo unido al menos dos horas en condiciones ácidas mientras liberaba el medicamento de forma constante.
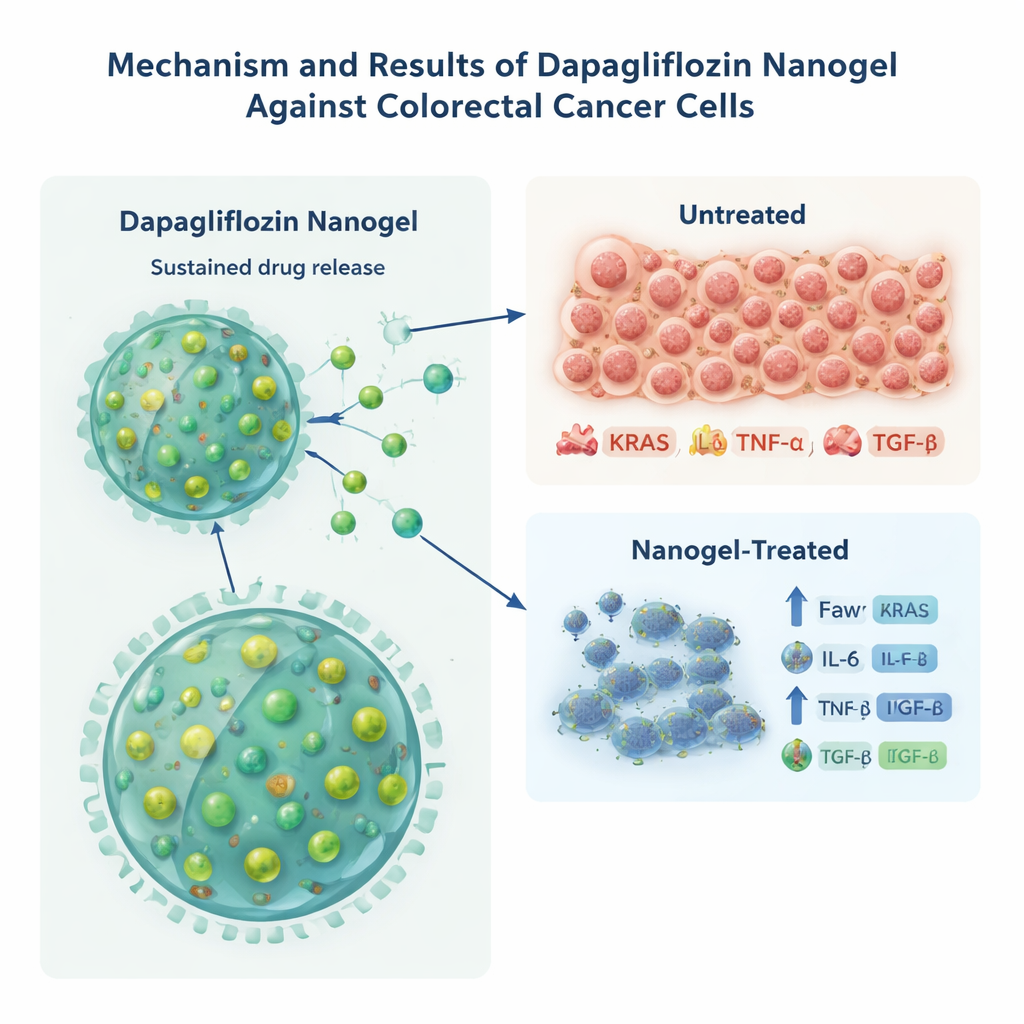
Someter a las células cancerosas a estrés en el laboratorio
Para comprobar si esta nueva forma de dapagliflozina podía realmente dañar las células cancerosas, el equipo la probó en células de cáncer colorrectal HCT-116 cultivadas en placas de laboratorio. En comparación con la misma cantidad de fármaco libre, la versión en nanogel mató las células cancerosas a concentraciones más bajas, reduciendo la dosis necesaria para disminuir a la mitad el crecimiento celular en aproximadamente un tercio. Los investigadores analizaron luego moléculas vinculadas con un comportamiento tumoral agresivo y la inflamación crónica, incluyendo KRAS (una proteína clave que impulsa el cáncer) y las proteínas de señalización IL-6, TNF-α y TGF-β. Las células tratadas con el nanogel cargado de fármaco mostraron niveles mucho más bajos de todos estos marcadores que las tratadas con el fármaco libre o con partículas vacías, lo que sugiere que la exposición sostenida proporcionada por las nanopartículas redujo más eficazmente las señales relacionadas con el cáncer y la inflamación. Dado que la línea celular ya porta una mutación fija en KRAS, los autores advierten que esta disminución de la proteína KRAS podría reflejar respuestas al estrés más que una corrección genética directa, pero aun así respalda un impacto biológico contundente.
Cambiar la manera en que el organismo maneja el medicamento
El equipo pasó después a estudios en animales, administrando a ratas ya fuera una suspensión simple de polvo de dapagliflozina o el nanogel optimizado, ambos por vía oral y a la misma dosis. En el grupo tratado con nanogel, los niveles máximos del fármaco en sangre aparecieron más tarde y fueron menores, pero el fármaco permaneció en circulación por más tiempo. La exposición total (medida como área bajo la curva) aumentó modestamente en torno a un 7%, y la semivida aparente se duplicó aproximadamente. Estos cambios significan que el organismo experimenta una dosis más suave y prolongada a lo largo del tiempo en lugar de un pico pronunciado y una caída rápida. Ese comportamiento coincide con lo que los investigadores diseñaron para el gel: retener el fármaco en el intestino, liberarlo lentamente y, potencialmente, mantener niveles más elevados bañando el intestino inferior y el colon donde surgen los tumores.
Qué podría significar esto para la atención oncológica futura
En términos cotidianos, este estudio toma un fármaco para la diabetes bien conocido y le suministra un nuevo “traje de entrega” para que llegue mejor y permanezca cerca de los tumores de colon. El nanogel facilita la disolución del fármaco, ralentiza su salida del tubo digestivo y parece hacerlo más tóxico para las células de cáncer colorrectal mientras reduce señales clave de inflamación y crecimiento. En ratas, amplía de forma suave la presencia del fármaco en la sangre sin aumentar de manera drástica la dosis total. El trabajo aún está en una fase temprana —limitado a una línea celular y a pruebas animales de corto plazo— y todavía no ha demostrado reducción tumoral directa en animales vivos ni en personas. Aun así, sienta una base detallada para reutilizar la dapagliflozina como parte de futuros tratamientos contra el cáncer colorrectal, usando nanogeles orales inteligentes para convertir una pastilla familiar en una herramienta anticancerígena más dirigida.
Cita: Abdullah, S., Thiab, S., Altamimi, A.A. et al. A repurposing Dapagliflozin via polymeric nanogels for colorectal cancer therapy. Sci Rep 16, 5625 (2026). https://doi.org/10.1038/s41598-026-36232-8
Palabras clave: cáncer colorrectal, reutilización de fármacos, nanopartículas, administración oral de fármacos, dapagliflozina