Clear Sky Science · es
Vigilancia genómica nacional de aislamientos de Klebsiella pneumoniae resistentes a carbapenémicos y colistina en sangre en Tailandia (2020–2024)
Aumento de infecciones sanguíneas mortales
Los hospitales de todo el mundo se enfrentan a una tendencia inquietante: bacterias comunes que antes cedían ante nuestros antibióticos más potentes se están volviendo casi imposibles de tratar. Este estudio se centra en Klebsiella pneumoniae, un microbio que puede invadir el torrente sanguíneo y causar infecciones potencialmente mortales, y sigue cómo ha evolucionado en Tailandia para resistir incluso los fármacos de último recurso. Comprender dónde se están propagando estos supermicrobios y cómo eluden los medicamentos es crucial para proteger a los pacientes, orientar las decisiones clínicas y diseñar políticas de salud pública.
Rastreando un supermicrobio hospitalario a lo largo de una nación
Los investigadores analizaron 227 muestras de Klebsiella pneumoniae tomadas de la sangre de pacientes en hospitales de Tailandia entre 2020 y 2024. Estas muestras procedían de una red de vigilancia nacional que recoge rutinariamente datos sobre infecciones resistentes a fármacos. Las pruebas de laboratorio mostraron que más del 93 % de estos aislamientos sanguíneos eran resistentes a los carbapenémicos, una poderosa clase de antibióticos que suele emplearse cuando fallan otros fármacos. Preocupantemente, casi un tercio de las cepas resistentes a carbapenémicos también eran resistentes a la colistina, una de las últimas opciones que emplean los médicos cuando nada más funciona. Al combinar las pruebas de sensibilidad habituales con secuenciación genómica completa, el equipo pudo ver no solo qué fármacos fallaban, sino también qué artimañas genéticas usaban las bacterias para sobrevivir.
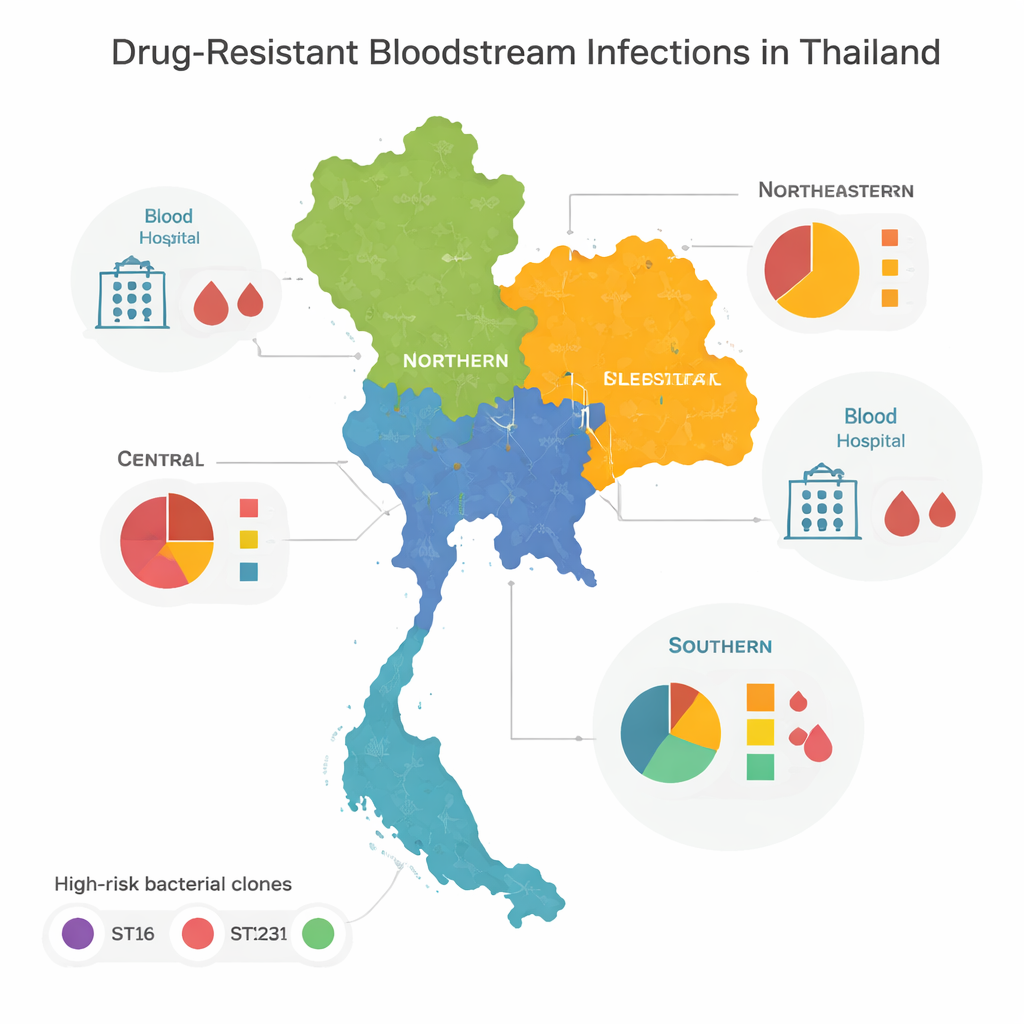
Clones de alto riesgo y patrones regionales
Cuando el equipo comparó los genomas, descubrió que la mayoría de las bacterias resistentes pertenecían a unas pocas familias “de alto riesgo”, o clones, conocidos a nivel mundial por causar brotes hospitalarios. Tres en particular —denominados ST16, ST147 y ST231— dominaron en las zonas central, norte y noreste de Tailandia. Estos clones se habían propagado ampliamente entre regiones, lo que sugiere movimientos frecuentes de pacientes, personal o bacterias entre hospitales. El sur del país presentaba un panorama distinto: en lugar de estar dominado por unos pocos tipos, albergaba una gran variedad de linajes bacterianos, muchos observados solo una vez. Esta diversidad apunta a una mezcla más compleja de brotes locales, fuentes ambientales y movimiento transfronterizo, en vez de uno o dos clones descontrolados.
Cómo las bacterias burlan a los antibióticos
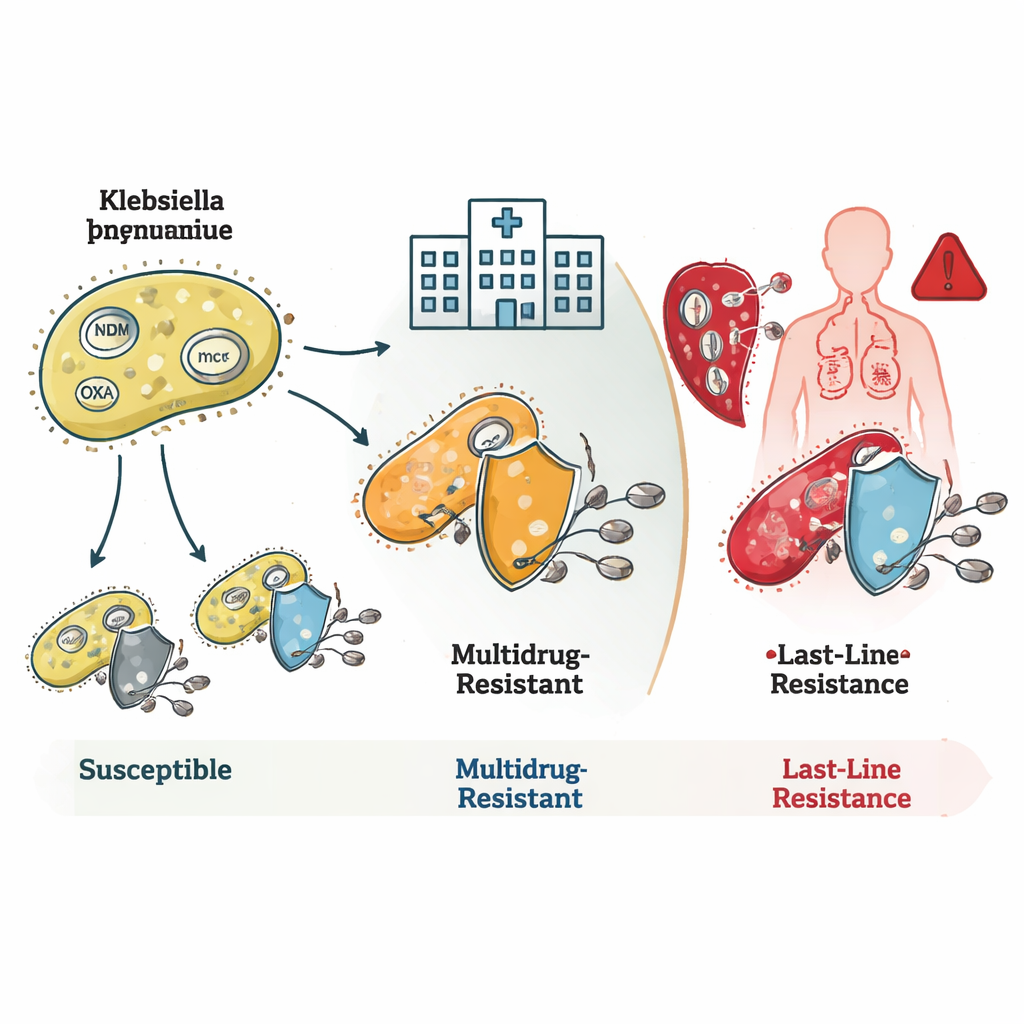
El estudio reveló cómo estas bacterias combinan múltiples mecanismos de resistencia. Muchas cepas ST16 y ST231 llevaban genes conocidos como blaNDM y blaOXA, que producen enzimas que degradan los antibióticos carbapenémicos antes de que puedan actuar. Algunas también presentaban alteraciones en su membrana externa que reducen la entrada de fármacos, combinándose para crear una resistencia de muy alto nivel. Las cepas ST231 con frecuencia llevaban además un gen, rmtF1, que bloquea a un grupo importante de antibióticos llamados aminoglucósidos, estrechando aún más las opciones terapéuticas. ST147 destacó por su flexibilidad genética: mezclaba y combinaba distintos genes de resistencia y plásmidos —anillos de ADN pequeños y móviles—, convirtiéndolo en un potencial centro para la difusión de rasgos de resistencia a otras bacterias.
Fracasos de último recurso y peligros ocultos
El hallazgo más alarmante concernió a la resistencia a la colistina, un fármaco que los médicos reservan para situaciones desesperadas. Algunas familias bacterianas poco frecuentes portaban genes mcr, que pueden saltar entre especies mediante plásmidos y causar directamente resistencia a la colistina. Otras, especialmente dentro del clon ST16, eran resistentes a la colistina a pesar de carecer de genes o mutaciones de resistencia conocidos. Esto sugiere que los científicos aún no han mapeado por completo todas las formas en que las bacterias pueden neutralizar este fármaco de último recurso. El equipo también identificó cepas hipervirulentas —bacterias especialmente eficaces para causar enfermedad grave—, incluyendo un linaje que combinaba alta virulencia con resistencia a todos los carbapenémicos probados, una mezcla particularmente peligrosa.
Por qué importa la vigilancia genómica
Para entender cómo los cambios genéticos se traducían en fallos terapéuticos reales, los investigadores usaron modelos estadísticos para vincular genes de resistencia específicos con los resultados de las pruebas de laboratorio. Genes como blaNDM-1 y sus parientes mostraron asociaciones extremadamente fuertes con la resistencia a carbapenémicos, confirmando su papel central en provocar el fracaso del tratamiento. Sin embargo, para la colistina, la mayoría de las bacterias resistentes no presentaban marcadores de resistencia reconocidos, lo que apunta a mecanismos ocultos que aún deben descubrirse. Los autores sostienen que el uso rutinario de la secuenciación genómica completa en la vigilancia hospitalaria puede actuar como un radar de alerta temprana, detectando clones emergentes de alto riesgo, rastreando su movimiento a través de regiones y fronteras, y guiando respuestas rápidas de control de infecciones.
Qué significa esto para pacientes y políticas
Para el público general, el mensaje es directo pero claro: algunas infecciones sanguíneas en Tailandia están ahora causadas por bacterias que resisten casi todos los fármacos disponibles, y unas pocas familias peligrosas de estos microbios se están expandiendo ampliamente. Al mismo tiempo, el estudio muestra que con las herramientas adecuadas —muestreo nacional, análisis genético y compartición rápida de datos— los sistemas de salud pueden anticipar estas amenazas y adaptarse. Ampliar la vigilancia genómica, desarrollar pruebas moleculares rápidas y reforzar el control de infecciones podrían ayudar a frenar el avance de estos supermicrobios y ganar tiempo para desarrollar nuevos tratamientos y vacunas.
Cita: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
Palabras clave: resistencia a antimicrobianos, Klebsiella pneumoniae, infección de la sangre, vigilancia genómica, atención sanitaria en Tailandia