Clear Sky Science · es
ARNs largos no codificantes con expresión aberrante en la diferenciación de células madre mesenquimales derivadas de tejido adiposo hacia células tipo núcleo pulposo
Por qué importa el dolor de espalda y el ARN oculto
El dolor lumbar es una de las principales causas por las que las personas faltan al trabajo o consultan a un médico, y uno de los culpables es el deterioro lento de los cojines blandos entre las vértebras, conocidos como discos intervertebrales. En el interior de cada disco hay un núcleo gelatinoso llamado núcleo pulposo, que depende de una población saludable de células especializadas para mantenerse elástico y bien hidratado. A medida que estas células se pierden o envejecen, el disco se deshidrata, colapsa y puede desencadenar dolor crónico. Los científicos exploran si las células madre —células versátiles capaces de convertirse en distintos tejidos— podrían guiarse para reemplazar estas células discales desgastadas. Este estudio plantea una pregunta sorprendentemente básica: ¿qué señales genéticas “silenciosas” se activan cuando se induce a las células madre a convertirse en nuevas células discales, y cómo podrían aprovecharse esas señales para mejorar futuras terapias?
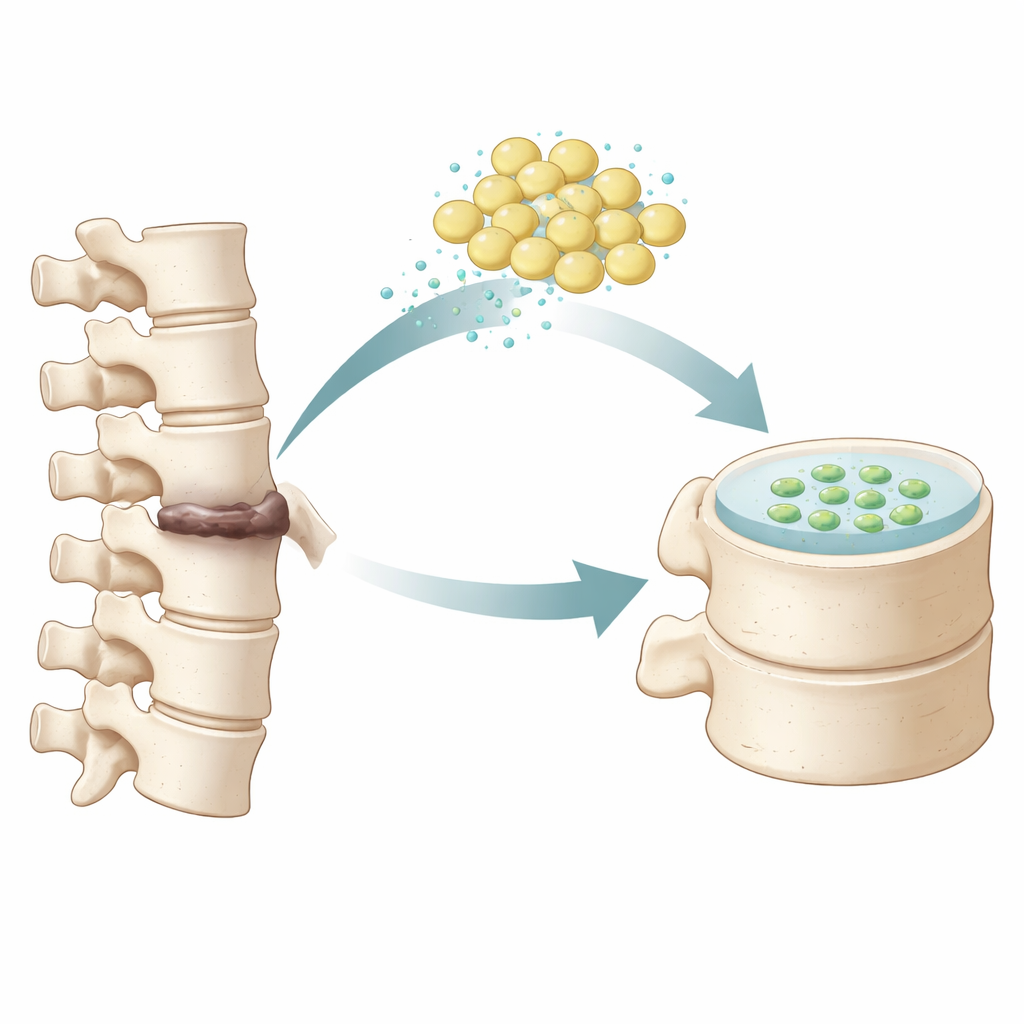
De tejido adiposo a la reparación del disco
Los investigadores se centraron en células madre mesenquimales humanas derivadas del tejido adiposo, que se obtienen de la grasa corporal y son relativamente fáciles de conseguir. En el laboratorio, cultivaron estas células en pequeños pellets tridimensionales y las expusieron a una mezcla cuidadosamente seleccionada de factores de crecimiento que trabajos previos habían mostrado que pueden empujar a las células hacia una identidad similar a la del núcleo pulposo. Durante varias semanas, el equipo observó los pellets con tinciones microscópicas estándar y marcadores fluorescentes. Las células tratadas empezaron a parecerse y comportarse más como las células del núcleo gelatinoso de un disco sano, produciendo componentes característicos del tejido discal como colágeno y agrecano, y activando genes clave asociados con la identidad del núcleo pulposo.
Escuchando el “ruido de fondo” celular
Más allá de los genes codificantes de proteínas conocidos, las células también producen ARN largos no codificantes: fragmentos de ARN que no generan proteínas pero que pueden orientar sutilmente qué genes se activan o se silencian. Estas moléculas están emergiendo como directores importantes en la orquesta de la diferenciación celular. Mediante secuenciación de ARN de alto rendimiento, el equipo midió tanto los ARN mensajeros tradicionales como los ARN largos no codificantes en células madre sometidas a diferenciación tipo discal, y los comparó con células control no diferenciadas. Encontraron una remodelación extensa del paisaje genético: 500 ARN largos no codificantes y 601 ARN mensajeros cambiaron sus niveles de actividad, con algunos aumentando en abundancia y otros disminuyendo a medida que las células se desplazaban hacia un estado similar al del núcleo pulposo.
Vías clave y reguladores maestros
Para dar sentido a esta larga lista de moléculas alteradas, los científicos emplearon herramientas bioinformáticas que agrupan genes según sus funciones en la célula. Muchos de los genes modificados estaban relacionados con la construcción y organización de la matriz extracelular —la red de colágeno, azúcares y otras moléculas que confiere propiedades amortiguadoras al tejido discal. El análisis de vías destacó la ruta de señalización PI3K–Akt y los sistemas que gobiernan el esqueleto interno de la célula como particularmente activos durante la diferenciación, lo que sugiere que estos circuitos ayudan a impulsar la transformación de células madre derivadas de grasa a células tipo disco. Al construir redes de interacción, el equipo identificó un conjunto de ARN largos no codificantes, incluidos MALAT1, MEG3, GAS5, ZNF331 y ARN vinculados a JARID2, que parecen situarse en el centro de la comunicación entre ARNs regulatorios, ARN mensajeros y microARNs. Estos hubs pueden actuar como interruptores maestros que controlan la eficiencia con la que las células madre se comprometen con un destino tipo disco.
Pistas para mejorar las terapias con células madre
La degeneración del disco intervertebral presenta un entorno especialmente hostil —ácido, con bajo oxígeno y rico en moléculas inflamatorias— que puede frustrar a las células madre trasplantadas. Al mapear qué ARNs y vías cambian durante la conversión exitosa en laboratorio de células madre derivadas de grasa a células similares al núcleo pulposo, este estudio ofrece un catálogo de objetivos moleculares que podrían ajustarse para aumentar la supervivencia y el rendimiento de las células terapéuticas en pacientes reales. Aunque el trabajo se realizó in vitro y con un número limitado de muestras, sienta las bases para experimentos futuros que podrían, por ejemplo, modificar ARNs largos no codificantes específicos o vías de señalización para mejorar la regeneración del disco.
Qué significa esto para las personas con dolor de espalda
Para las personas que viven con dolor lumbar crónico, estos hallazgos no cambiarán el tratamiento de forma inmediata, pero ayudan a completar una pieza crucial que faltaba: cómo las células madre aprenden a convertirse en el tipo exacto de células discales necesarias para la reparación. El estudio muestra que esta transformación está guiada no solo por genes bien conocidos, sino también por una compleja red de ARN largos no codificantes y vías de señalización que moldean el comportamiento celular. Al descifrar esta capa oculta de control, los científicos avanzan hacia el diseño de terapias con células madre más inteligentes que puedan resistir mejor el entorno hostil de un disco dañado y reconstruir de forma más fiable su núcleo amortiguador, ofreciendo potencialmente un alivio más duradero en el futuro.
Cita: Zhu, J., Jin, L., Jin, K. et al. Aberrantly expressed long noncoding RNAs in adipose-derived mesenchymal stem cells differentiation to nucleus pulposus-like cells. Sci Rep 16, 8029 (2026). https://doi.org/10.1038/s41598-026-36219-5
Palabras clave: degeneración del disco intervertebral, terapia con células madre, células del núcleo pulposo, ARN largo no codificante, secuenciación de ARN