Clear Sky Science · es
Pigmentos distiril-BODIPY sustituidos con piridinio y bromo para terapia fotodinámica dirigida a las mitocondrias
Iluminando las células cancerosas desde el interior
La terapia fotodinámica es un tratamiento contra el cáncer que utiliza fármacos especiales activados por la luz para matar células tumorales preservando en gran medida el tejido sano. Este estudio explora una nueva familia de colorantes fluorescentes diseñados para localizarse en las centrales energéticas de la célula —las mitocondrias— y, al ser iluminados con luz rojo‑profunda, generar especies reactivas de oxígeno que pueden destruir células cancerosas. El trabajo muestra tanto las promesas como las limitaciones de diseñar ese tipo de colorantes a nivel molecular.
¿Por qué atacar las centrales energéticas de la célula?
Las mitocondrias son fundamentales para la producción de energía y contribuyen a decidir si una célula sobrevive o muere. Las células cancerosas tienden a tener una membrana mitocondrial más polarizada que las células normales, lo que hace que atraigan con mucha más fuerza moléculas con carga positiva. Los investigadores aprovecharon esto uniendo un grupo piridinio cargado positivamente a un andamiaje de colorante fluorescente bien conocido, llamado BODIPY. Este diseño ayuda a dirigir los colorantes hacia las mitocondrias, donde las reacciones químicas desencadenadas por la luz pueden infligir el máximo daño a las células cancerosas mientras se limita el daño en otras partes.
Diseñando colorantes activados por luz más inteligentes
El equipo creó tres colorantes estrechamente relacionados, denominados PyBHI, PyBMI y PyBBrI, que difieren principalmente en cuántos átomos de bromo contienen (ninguno, uno o dos). Todos comparten una estructura larga y extendida que desplaza su absorción y emisión hacia la región del infrarrojo cercano —una ventana útil donde la luz puede penetrar más profundamente en el tejido. En teoría, estos colorantes podrían usar dos vías internas diferentes para alcanzar un estado excitado “triplete” que produce oxígeno singlete reactivo: una impulsada por los pesados átomos de bromo y otra por un desplazamiento temporal de carga eléctrica dentro de la molécula. 
Cuando la teoría se encuentra con la realidad experimental
A pesar del diseño elegante, las pruebas detalladas mostraron que los colorantes no generaban oxígeno singlete con la eficiencia esperada. Usando sondas químicas que pierden su color al reaccionar con oxígeno singlete, los investigadores midieron rendimientos de generación de oxígeno muy bajos para los tres colorantes, con solo una mejora modesta al añadir más átomos de bromo. Experimentos con láser ultrarrápido revelaron la razón: tras la absorción de luz, los colorantes entran rápidamente en estados con desplazamiento de carga que mayoritariamente se relajan de forma inocua como calor en lugar de convertirse en el estado triplete deseado. En las versiones bromadas, los átomos pesados aún abren una vía al estado triplete, pero esta ruta es mucho más lenta que la pérdida de energía competidora, lo que limita la eficiencia global.
Dirigiéndose a las mitocondrias tumorales en células vivas
La historia cambia en un entorno biológico. En cultivos de células humanas de mama (MCF‑7) y cervicales (HeLa), las tres moléculas mostraron por microscopía confocal una fuerte acumulación en mitocondrias, colocalizándose con un tinte mitocondrial estándar. Las pruebas de toxicidad en la oscuridad indicaron que los colorantes son en gran medida inofensivos sin luz. Sin embargo, bajo irradiación con luz roja, el colorante dibromado PyBBrI causó una muerte sustancial de células cancerosas, con dosis en el rango de nanomolar bajo que reducían la viabilidad celular a la mitad. Los otros dos colorantes fueron mucho menos efectivos. 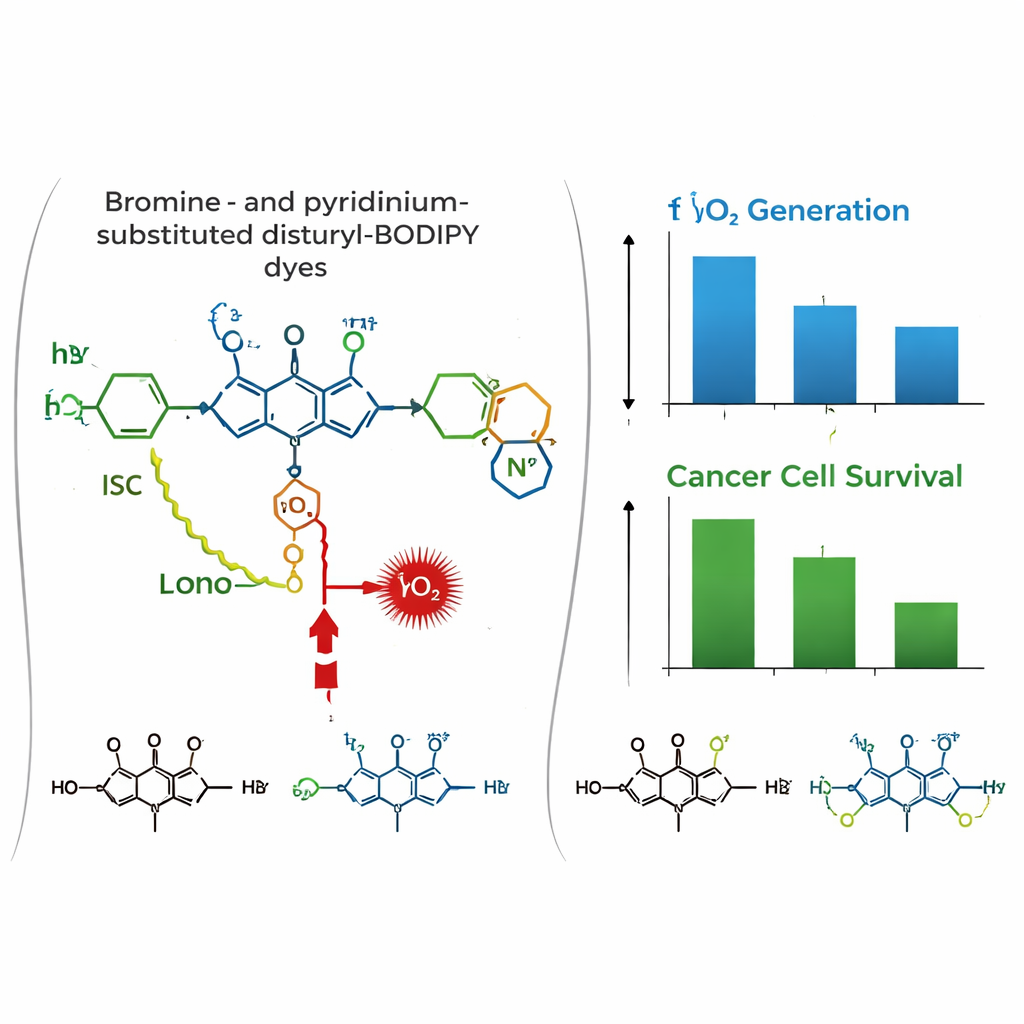
Qué significa esto para futuras terapias contra el cáncer
Para un público no especializado, el mensaje clave es que pequeños ajustes químicos pueden cambiar drásticamente el comportamiento de fármacos activados por la luz, y que su rendimiento en células reales puede ser mejor —o peor— de lo predicho por mediciones básicas. En este caso, el colorante más modificado, PyBBrI, mostró solo una producción modesta de oxígeno reactivo en tubo de ensayo pero resultó altamente potente contra células cancerosas una vez que alcanzó sus mitocondrias. El trabajo subraya tanto la importancia de dirigir los fármacos a estructuras vulnerables dentro de las células cancerosas como la complejidad de predecir la eficiencia fotodinámica. Señala el camino hacia terapias de nueva generación dirigidas a mitocondrias que usan luz en el infrarrojo cercano para “activar” selectivamente la química letal exactamente donde se necesita.
Cita: Kim, C., Badon, I.W., Jo, J. et al. Pyridinium- and bromine-substituted distyryl-BODIPY dyes for mitochondria-targeted photodynamic therapy. Sci Rep 16, 6789 (2026). https://doi.org/10.1038/s41598-026-36213-x
Palabras clave: terapia fotodinámica, colorantes dirigidos a mitocondrias, BODIPY, oxígeno singlete, células cancerosas