Clear Sky Science · es
La radiación γ induce alteraciones subcelulares específicas por región de marcadores de esclerosis lateral amiotrófica y demencia frontotemporal en el cerebro de porcinos
Por qué importan las dosis pequeñas de radiación y los cerebros de cerdo
La mayoría de nosotros pensamos en la radiación como algo puramente dañino, sobre todo para el cerebro. Pero nuestro entorno está lleno de niveles bajos de radiación procedentes de exploraciones médicas, vuelos y el medio ambiente. Al mismo tiempo, los científicos aún intentan dilucidar qué provoca la esclerosis lateral amiotrófica (ELA), la enfermedad mortal que paralizó al jugador de béisbol Lou Gehrig, y su pariente cercano, la demencia frontotemporal (DFT), que ataca el comportamiento y la personalidad. Este estudio plantea una pregunta sorprendentemente esperanzadora: ¿podría una única dosis moderada de radiación gamma remodelar sutilmente la química cerebral de maneras que no sean únicamente perjudiciales y, tal vez, incluso protectoras frente a los cambios moleculares asociados a la ELA y la DFT?
Una mirada más cercana a las señales de alerta de la ELA en el cerebro
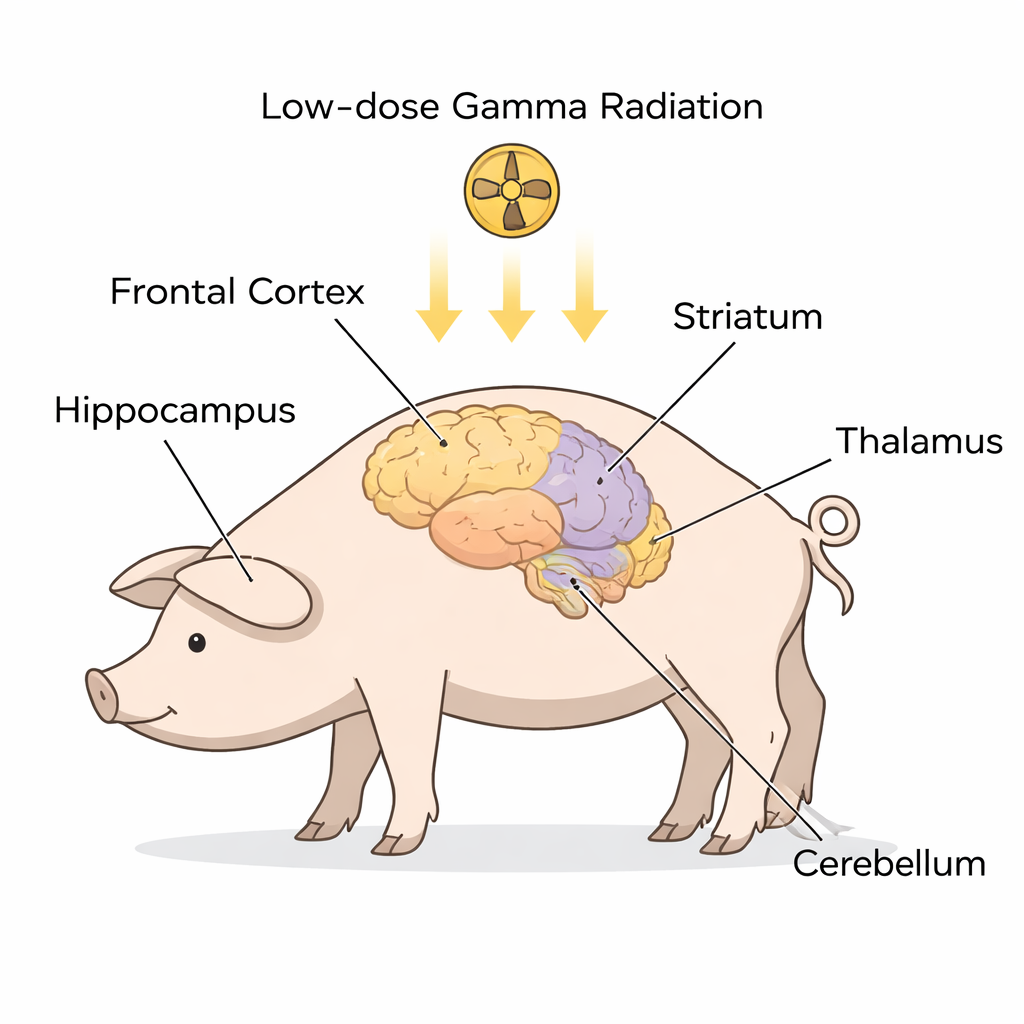
En lugar de examinar a pacientes que ya tenían ELA, los investigadores trabajaron con minipuerros de Göttingen sanos, cuyos cerebros son anatómicamente similares a los nuestros. Nueve animales recibieron una exposición única de cuerpo entero a radiación gamma de baja dosis, mientras que seis fueron anestesiados pero no irradiados y sirvieron como controles. Aproximadamente un mes después, los científicos disecaron cinco regiones cerebrales clave a menudo implicadas en la ELA y la DFT: la corteza frontal, el hipocampo, el cuerpo estriado, el tálamo/hipotálamo y el cerebelo. En cada región separaron el contenido celular en dos compartimentos principales: el citoplasma (el fluido interior de la célula) y el núcleo (el compartimento que alberga el ADN). Mediante una técnica llamada Western blot, midieron los niveles de varias proteínas fuertemente vinculadas a la ELA y a la ELA‑DFT, incluidas SOD1, FUS, C9orf72, STMN2, ubiquitina, TDP‑43 y una forma modificada llamada TDP‑43 fosforilada.
La radiación deja algunos marcadores sin cambios — y otros desplazados
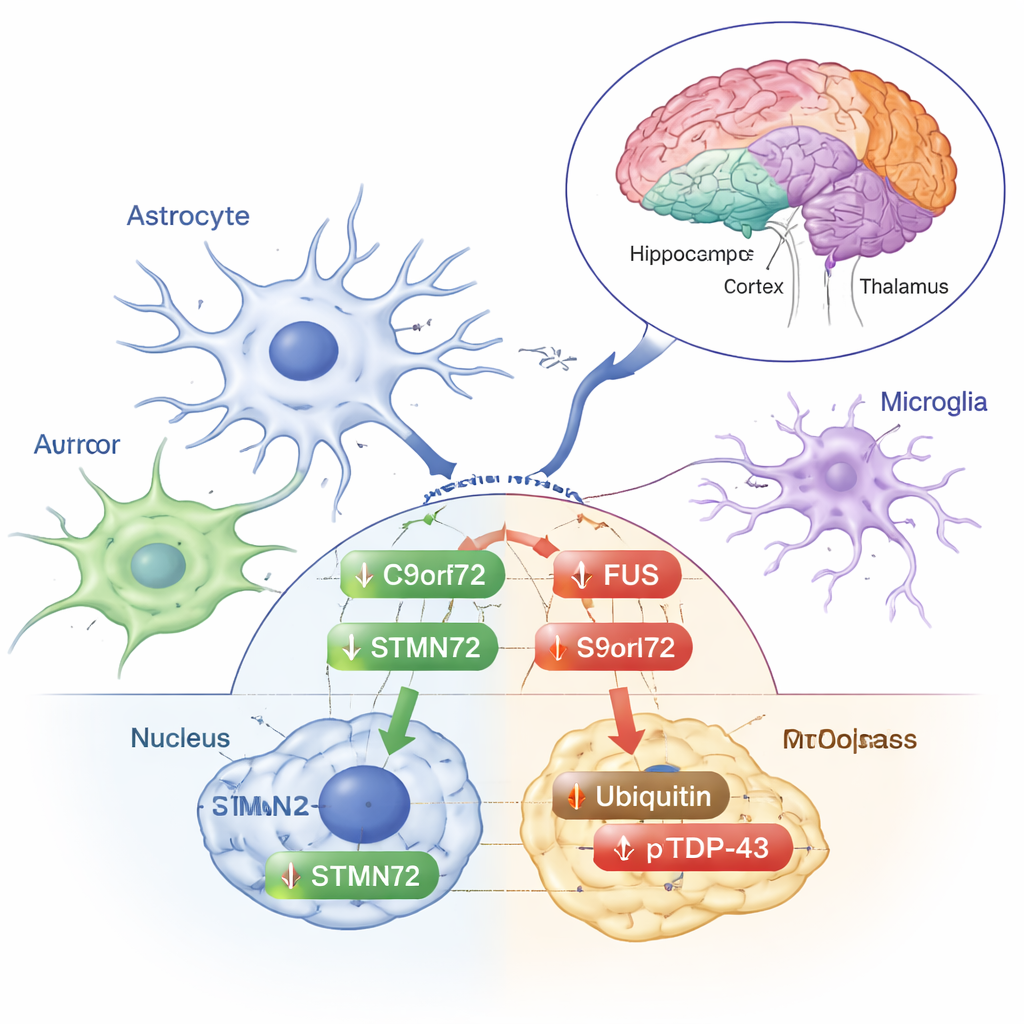
Un hallazgo tranquilizador fue que los niveles totales de SOD1, una proteína cuyas mutaciones provocan algunos casos hereditarios de ELA, no cambiaron en ninguna región tras la radiación. Del mismo modo, las formas principales de TDP‑43 —la proteína que con más frecuencia se encuentra en los agregados cerebrales relacionados con la ELA— permanecieron estables tanto en el núcleo como en el citoplasma en todas las regiones. Pero no todo fue estático. El equipo observó cambios específicos por región y por compartimento en varias otras proteínas. Por ejemplo, FUS, una proteína que normalmente reside en el núcleo pero que puede comportarse mal y agregarse en la ELA, disminuyó en el citoplasma del tálamo/hipotálamo tras la radiación, mientras que sus niveles nucleares aumentaron en la corteza frontal y descendieron en el hipocampo. La proteína vinculada a la ELA C9orf72 no presentó cambios en el fluido celular pero mostró una caída en los núcleos hipocámpicos. STMN2, una proteína importante para mantener las fibras nerviosas, también se redujo en los núcleos del hipocampo, lo que sugiere una respuesta coordinada entre estas dos moléculas en esa región relacionada con la memoria.
¿Señales de estrés o protección temprana?
Otros cambios parecieron más bien respuestas clásicas al estrés. La ubiquitina —la pequeña etiqueta que la célula usa para marcar proteínas dañadas para su eliminación— aumentó en la fracción citoplasmática de la corteza frontal. La forma fosforilada de TDP‑43, que con frecuencia se acumula en los depósitos anormales observados en ELA y DFT, aumentó en el citoplasma de la corteza frontal, el cuerpo estriado y el tálamo/hipotálamo, aunque el TDP‑43 total no lo hizo. Estos desplazamientos sugieren que la radiación de baja dosis empuja la maquinaria de manejo de proteínas del cerebro sin desencadenar los patrones completos de desnaturalización y agregación que definen la enfermedad. Los autores enfatizan que estas respuestas varían según la región cerebral y según si una proteína está dentro o fuera del núcleo, lo que subraya lo finamente ajustada que puede ser la reacción del cerebro al estrés.
Qué podría significar para el riesgo de ELA — y posibles beneficios
¿Significa esto que la radiación de baja dosis causa ELA? Los datos no apoyan una respuesta sencilla afirmativa. Los investigadores no observaron la deslocalización característica ni la acumulación de las proteínas principales de la ELA, y muchos cambios apuntaron a una regulación alterada más que a un daño rotundo. De forma intrigante, estos resultados concuerdan con trabajos previos del mismo grupo y de otros que sugieren que pequeñas cantidades de radiación pueden a veces desencadenar «hormesis»: un fenómeno en el que el estrés leve activa vías de reparación y reduce proteínas dañinas, como las vinculadas con el Alzheimer o el Parkinson, en modelos animales. El estudio actual insinúa que, al menos a corto plazo, una única dosis baja de radiación gamma remodela los marcadores relacionados con la ELA de maneras que podrían ser adaptativas en lugar de destructivas.
Grandes preguntas y esperanza cautelosa
Para el lector no especializado, la conclusión clave es que la relación entre radiación y salud cerebral es más matizada que «toda radiación es mala». En este modelo de animal grande, la exposición a radiación gamma de baja dosis produjo cambios sutiles y específicos por región en proteínas asociadas con la ELA y la DFT, sin reproducir los patrones dañinos observados en cerebros de pacientes. Estos cambios podrían reflejar el intento del cerebro de afrontar y reparar el estrés, y en algunos casos incluso podrían resultar beneficiosos. Sin embargo, el estudio analizó solo un mes después de una única exposición, y solo en el cerebro (no en la médula espinal, donde la ELA golpea con más fuerza). Se necesitan estudios a largo plazo y con dosis repetidas antes de considerar traducir estos hallazgos a personas. Aun así, este trabajo abre una nueva ventana sobre cómo la radiación a niveles cotidianos interactúa con las moléculas que sustentan enfermedades neurodegenerativas devastadoras —y plantea la posibilidad de que, en entornos cuidadosamente controlados, pequeñas dosis podrían algún día aprovecharse para estimular las propias defensas del cerebro.
Cita: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
Palabras clave: esclerosis lateral amiotrófica, demencia frontotemporal, radiación de baja dosis, proteínas cerebrales, modelo de minipuerco