Clear Sky Science · es
El casete de lisis del jumbovirus PhiKZ
Cómo los virus gigantes hacen estallar a las bacterias
Los virus que infectan bacterias —llamados bacteriófagos o, simplemente, fagos— se estudian como armas de precisión contra infecciones peligrosas, como las causadas por Pseudomonas aeruginosa, una bacteria resistente común en hospitales. Un fago especialmente grande, phiKZ, ha fascinado a los científicos porque construye una compartimentación protectora “similar a un núcleo” dentro de su huésped. Sin embargo, hasta ahora no se sabía bien cómo este fago gigante rompe realmente a su huésped para escapar. Este estudio desvela el conjunto de genes y herramientas moleculares que phiKZ utiliza para temporizar y ejecutar ese paso final y explosivo.
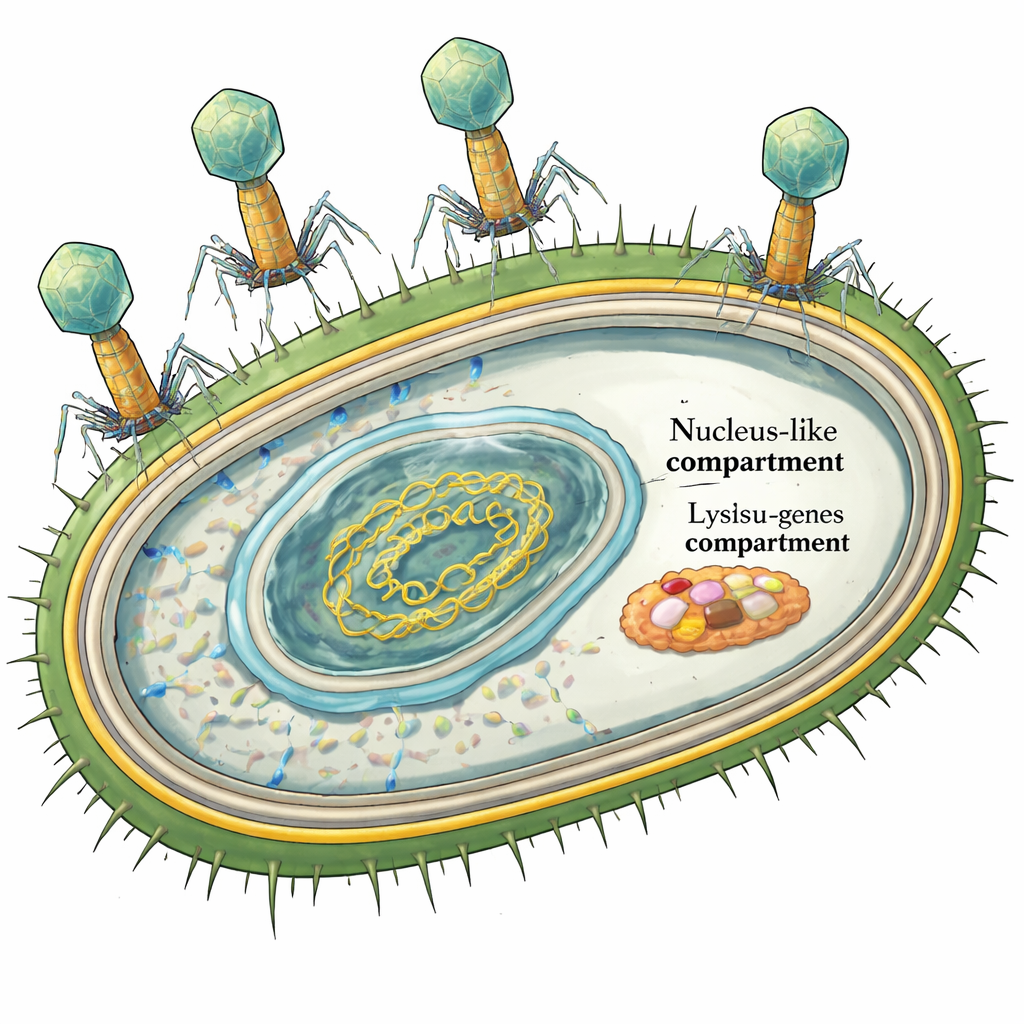
El fago gigante y su plan de escape
PhiKZ es un fago “jumbó”, con un genoma de más de 200.000 letras de ADN. Trabajos previos mostraron en detalle cómo oculta su ADN dentro de una cápsula proteica para eludir las defensas bacterianas. Pero el acto final de la infección —la destrucción controlada de la célula bacteriana— era un misterio. La mayoría de los fagos que infectan bacterias con dos membranas, como Pseudomonas, usan un sistema de lisis en cuatro partes: una proteína perfora la membrana interna, otra corta la pared celular, y un complejo de dos partes colapsa la membrana externa. Dado que el genoma de phiKZ parecía carecer de un gen reconocible que formara poros, algunos investigadores propusieron que podría usar una estrategia completamente diferente para situar su enzima cortadora de pared en su lugar.
Encontrando el kit de lisis oculto
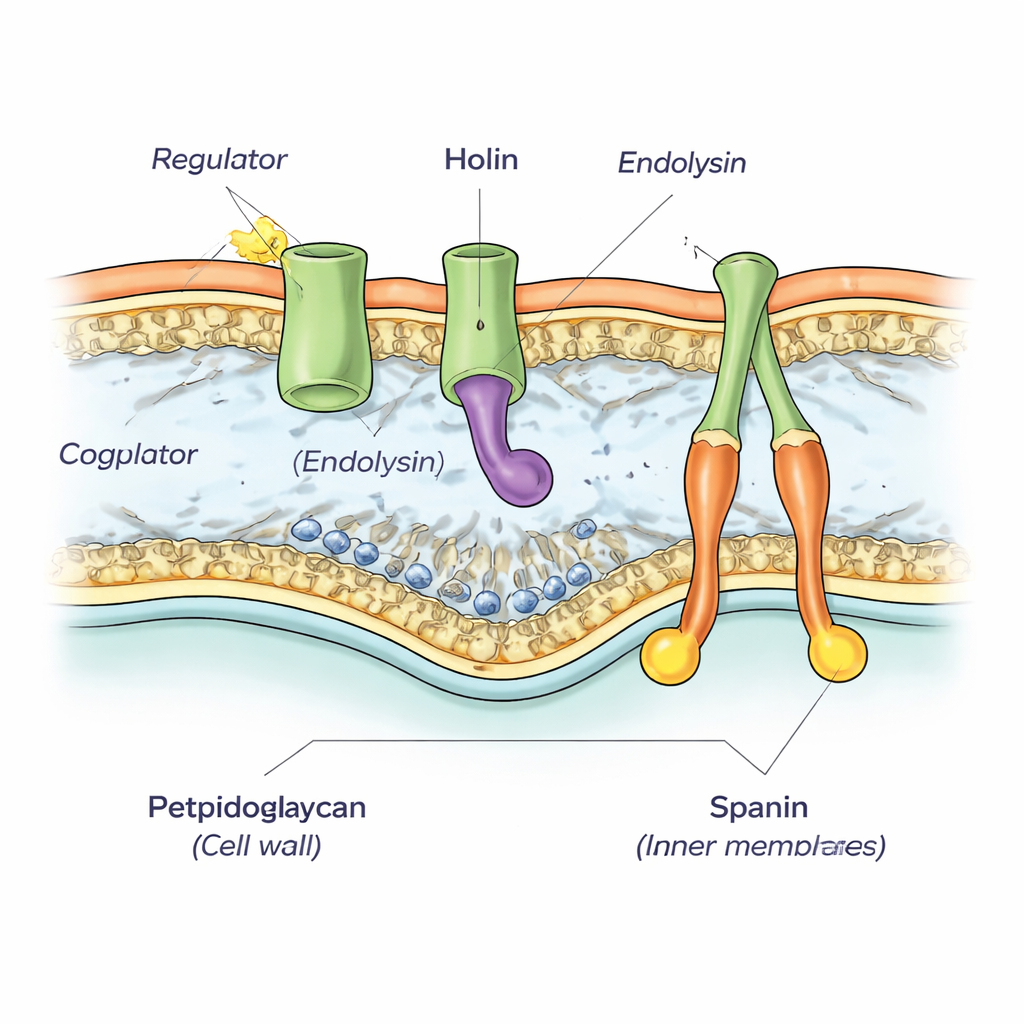
Al reexaminar la región del genoma de phiKZ que rodea a una enzima conocida por cortar la pared (llamada endolisina), los autores descubrieron un racimo compacto de cinco genes. Mediante análisis de secuencias y predicciones por ordenador, demostraron que dos de esos genes codifican los spaninas, un par de proteínas que conectan la membrana interna y la externa y más tarde ayudan a su fusión. Otro gen codifica la propia endolisina. Un cuarto gen resultó ser la holina que faltaba —la proteína que se acumula silenciosamente en la membrana interna antes de abrir de repente poros grandes. Los investigadores confirmaron estas funciones experimentalmente trasplantando genes de phiKZ a sistemas bien estudiados del fago lambda y Escherichia coli y mostrando que las versiones de phiKZ podían sustituir a las piezas faltantes.
Un interruptor de temporización para la destrucción celular
El quinto gen del racimo codifica una proteína pequeña que permanece en el citoplasma bacteriano en lugar de insertarse en una membrana. Cuando los autores expresaron esta proteína junto con la holina en E. coli, las células murieron notablemente antes que cuando la holina actuaba sola, aun cuando el resto de la maquinaria de lisis estaba ausente. Esto sugiere que la proteína adicional actúa como reguladora, empujando a la holina hacia una formación de poros más temprana o más intensa. Cuando el equipo recortó secciones de la larga cola orientada hacia el interior de la holina, encontraron que el regulador ya no podía acelerar el proceso y, en algunos casos, incluso bloqueaba la lisis. Modelos estructurales producidos con el software AlphaFold respaldaron una asociación física entre la cola interior de la holina y el regulador, formando un complejo estable de dos proteínas.
Pistas de un mecanismo de demora a altas dosis virales
Al infectar cultivos bacterianos con distintos números de partículas de phiKZ, los investigadores notaron un patrón intrigante. A dosis virales bajas, el cultivo lisa relativamente rápido y de forma abrupta. Sin embargo, a dosis altas, la lisis se retrasaba y se prolongaba durante más de dos horas. Esta desaceleración contraintuitiva recuerda a un fenómeno clásico llamado inhibición de lisis, conocido por otro fago llamado T4, en el que infecciones adicionales indican al virus que posponga la ruptura de la célula para así producir más partículas virales. Dado que phiKZ tiene un par holina-regulador capaz tanto de adelantar como, en algunas condiciones, bloquear la lisis, los autores sugieren que un sistema de demora similar podría existir en este fago jumbó.
Por qué importa para la terapia con fagos
Al establecer que phiKZ porta un casete de lisis convencional pero sofisticado —completo con holina, endolisina, spaninas y un regulador de temporización— este trabajo muestra que incluso los fagos jumbó exóticos dependen de herramientas familiares para salir de sus huéspedes. Para el público general, la conclusión clave es que el “momento de explosión” de los fagos terapéuticos puede ajustarse mediante pequeñas proteínas reguladoras que se comunican con las holinas formadoras de poros. Entender y, eventualmente, diseñar estos interruptores de temporización podría ayudar a crear tratamientos con fagos que maten bacterias lo más rápido posible o, cuando convenga, retrasen la lisis para maximizar la amplificación viral antes del golpe final.
Cita: Manohar, P., Wan, J., Ganser, G. et al. The Lysis cassette of jumbophage PhiKZ. Sci Rep 16, 5840 (2026). https://doi.org/10.1038/s41598-026-36188-9
Palabras clave: lisis por bacteriófagos, fago gigante phiKZ, sistema holina-endolisina, fago de Pseudomonas aeruginosa, inhibición de lisis