Clear Sky Science · es
FcIgG-GE11-Melittin como un nuevo peptibody dirigido a EGFR con potente actividad citotóxica frente a células cancerosas
El veneno de abeja se encuentra con la terapia contra el cáncer de precisión
Muchos fármacos prometedores contra el cáncer son simplemente demasiado agresivos para el resto del organismo como para usarse con seguridad. Un ejemplo notable es la melitina, la toxina principal del veneno de abeja: puede destruir células cancerosas, pero también dañar glóbulos rojos y tejidos sanos. Este estudio explora una solución ingeniosa: construir un “misil guiado” que transporte la melitina directamente a las células tumorales que muestran un marcador superficial específico, mientras deja en gran medida intactas las células normales.
Por qué dirigirnos a un interruptor común en el cáncer
Un actor clave en muchos tumores es una molécula llamada receptor del factor de crecimiento epidérmico, o EGFR. Este receptor se encuentra en la superficie de las células y ayuda a controlar el crecimiento y la supervivencia. En varios cánceres —incluidos pulmón, colorrectal, próstata y algunos de cabeza y cuello y riñón— EGFR se sobreexpresa, promoviendo una división celular descontrolada. Por ello, los fármacos que se unen a EGFR se han convertido en una clase importante de terapias dirigidas. Sin embargo, los fármacos existentes contra EGFR bloquean principalmente las señales; no perforan activamente las células cancerosas. Los investigadores se preguntaron si podrían aprovechar la poderosa capacidad lisante de la melitina y entregarla de forma selectiva a las células tumorales ricas en EGFR.
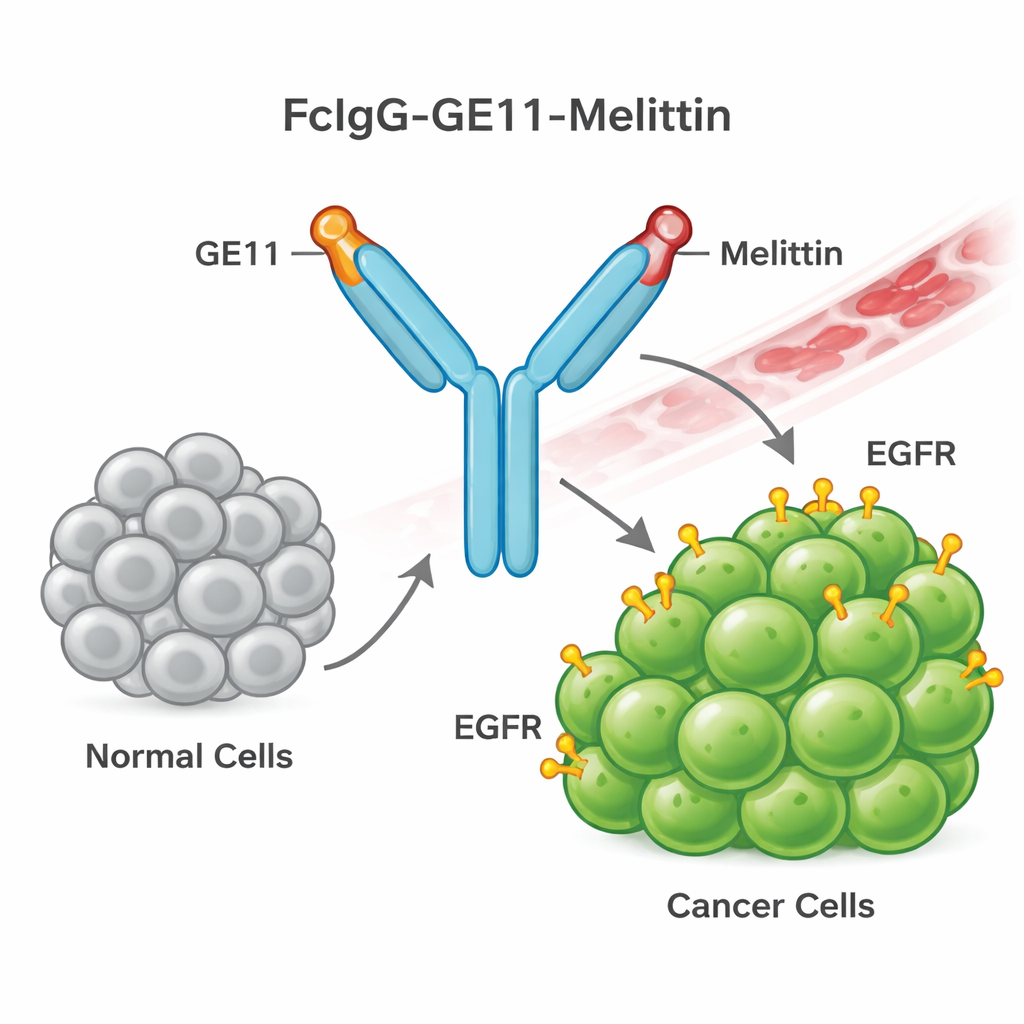
Construyendo un arma guiada con veneno de abeja
Para ello, el equipo diseñó una nueva proteína de fusión a la que denominaron FcIgG-GE11-Melittin. Combina tres partes: una “cola” de anticuerpo (la región Fc de la IgG humana) que mejora la estabilidad en el torrente sanguíneo y facilita la purificación; un péptido guía corto llamado GE11 que reconoce y se une a EGFR en células cancerosas; y la melitina, el péptido del veneno de abeja que puede romper membranas celulares. Se modificaron bacterias para producir esta proteína de fusión en grandes cantidades. La proteína se refoldó y purificó, y las pruebas de laboratorio confirmaron que adoptaba la forma dimérica esperada y portaba la etiqueta de anticuerpo humano, mostrando que el constructo se había construido correctamente.
Agarre a las células tumorales, no a cualquier célula
La siguiente pregunta fue si esta molécula diseñada realmente encuentra y se adhiere a las células cancerosas ricas en EGFR. Mediante citometría de flujo, los autores evaluaron la unión en células de cáncer de pulmón A549, que se sabe sobreexpresan EGFR. Las células tratadas con FcIgG-GE11-Melittin mostraron un fuerte aumento de fluorescencia, lo que indica que muchas moléculas de fusión se habían adherido a su superficie. Un peptibody no relacionado, Romiplostim, mostró casi ninguna unión, sirviendo como control negativo. El perfil de unión del nuevo constructo coincidió estrechamente con el de Cetuximab, un anticuerpo conocido contra EGFR, lo que respalda la idea de que el componente GE11 está guiando correctamente la proteína de fusión hacia su objetivo.
Eliminar células cancerosas preservando las sanguíneas
El equipo probó luego qué tan bien la proteína de fusión podía matar distintas líneas celulares cancerosas en cultivo. La melitina libre fue extremadamente potente pero indiscriminada, reduciendo drásticamente la supervivencia celular incluso a dosis bajas en células de pulmón (A549), próstata (DU145) y colorrectal (SW480). En contraste, FcIgG-GE11-Melittin mostró una tasa de muerte dependiente de la dosis que fue más potente en células positivas para EGFR, mientras que una línea de mama con baja expresión de EGFR (MDA-MB-453) fue relativamente resistente. Este patrón sugiere que el ataque del constructo de fusión depende de la orientación hacia EGFR más que del daño aleatorio de membranas. Lo más importante, en experimentos con glóbulos rojos humanos, la melitina libre causó casi una hemólisis completa a dosis moderadas, mientras que la proteína de fusión produjo menos del 5 % de hemólisis incluso a concentraciones muy altas. En otras palabras, unir la melitina al vehículo buscador de EGFR redujo drásticamente su tendencia a romper glóbulos rojos.
Qué podría significar esto para la futura atención del cáncer
En conjunto, el trabajo muestra que acoplar una toxina potente que altera membranas, como la melitina, a un sistema de direccionamiento preciso puede convertirla de una sustancia ampliamente tóxica en un arma más selectiva para tumores. FcIgG-GE11-Melittin se une fuertemente a células cancerosas que sobreexpresan EGFR, las mata de forma controlada y dependiente de la dosis, y muestra un daño mínimo sobre glóbulos rojos en el laboratorio. Aunque se necesitan más estudios en animales y ensayos de seguridad antes de cualquier uso en pacientes, este enfoque ilustra cómo reingeniar toxinas naturales en terapias guiadas podría abrir nuevas vías para tratar de forma más eficaz los cánceres positivos para EGFR y con menos efectos secundarios.
Cita: Hallaji, M., Fayaz, S., Allahyari, M. et al. FcIgG-GE11-Melittin as a novel EGFR targeted peptibody with potent cytotoxic activity against cancer cells. Sci Rep 16, 7047 (2026). https://doi.org/10.1038/s41598-026-36167-0
Palabras clave: terapia contra el cáncer dirigida, EGFR, melitina del veneno de abeja, peptibody, toxinas selectivas para tumores