Clear Sky Science · es
Modelo de probabilidad multinomial de DSB inducidas por radiación y racimos no-DSB: daños en tándem y biestrendiados
Por qué importan las pequeñas lesiones del ADN
Cuando pensamos en el daño por radiación a nuestros genes, solemos imaginar rupturas espectaculares en la doble hélice del ADN. Pero la mayoría de las lesiones por radiación son más sutiles y más concentradas que una única rotura limpia. Este artículo explora esos racimos ocultos de pequeñas heridas del ADN que pueden, de forma silenciosa, impulsar el riesgo de cáncer por radiación médica, exposición laboral y rayos cósmicos en el espacio.
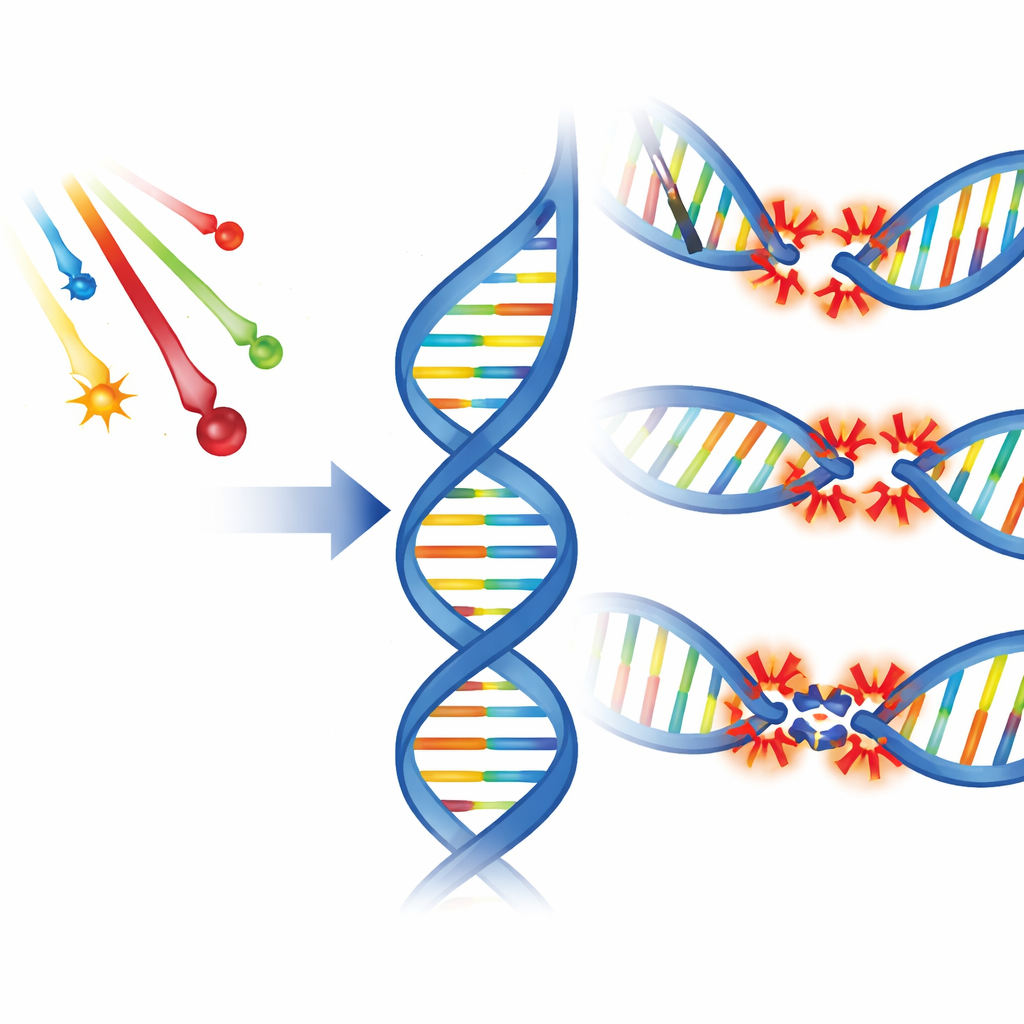
Diferentes tipos de roturas en la escalera del ADN
La radiación ionizante daña el ADN de varias maneras básicas. Puede cortar una hebra de la doble hélice, cortar ambas hebras muy cerca una de la otra o alterar químicamente las bases que codifican la información genética. Los científicos llaman a esto roturas de una hebra, roturas de doble hebra y daño en las bases. Es importante: la radiación frecuentemente provoca varias de estas lesiones empaquetadas en pocas vueltas de la hélice del ADN. Estos sitios concurridos, conocidos como daño agrupado, vienen en dos sabores principales: racimos biestrendiados, donde las lesiones se enfrentan en hebras opuestas, y racimos en tándem, donde múltiples lesiones se alinean a lo largo de la misma hebra. Los experimentos han mostrado que los racimos no–DSB—compuestos sobre todo por daño en bases y roturas de una hebra—son más comunes que las roturas de doble hebra francas, especialmente a dosis bajas.
Rellenando los puntos ciegos de los experimentos
Las técnicas de laboratorio existentes solo pueden ver parte de este panorama. Los ensayos enzimáticos y la imagen de alta resolución pueden detectar muchos racimos biestrendiados, donde las lesiones en hebras opuestas se convierten en roturas visibles. Pero todavía faltan métodos para contar los racimos en tándem, con múltiples lesiones a lo largo de una misma hebra. Eso significa que nuestras mediciones actuales subestiman cuántas lesiones agrupadas ocurren realmente. Para salvar esa brecha, el autor construye un modelo teórico que no depende de ver cada lesión directamente. En su lugar, usa la cantidad de energía que la radiación deposita en un volumen diminuto que contiene ADN, y cómo esa energía se divide probabilísticamente en distintos tipos de lesiones elementales.
Un mapa probabilístico del caos microscópico
El núcleo del trabajo es un modelo de probabilidad multinomial: un marco matemático que sigue cómo una ráfaga entrante de energía puede dar lugar a varios resultados a la vez. En un cilindro a escala nanométrica que contiene alrededor de 73 pares de bases de ADN, el modelo considera cuatro posibilidades cada vez que se deposita energía: impactos directos en la columna vertebral del ADN que causan roturas de hebra, impactos directos en las bases que causan daño químico, impactos indirectos en el agua circundante que producen radicales reactivos, y energía inofensiva absorbida por proteínas y otras moléculas próximas. Al combinar estas probabilidades con espectros detallados de deposición de energía para electrones y varios iones, el modelo enumera con qué frecuencia aparecerán diferentes combinaciones de lesiones—y, de forma crucial, qué tan cerca estarán unas de otras a lo largo o a través de las hebras del ADN.
Lo que el modelo revela sobre las trazas de radiación
Aplicando este marco a electrones y haces de iones usados en terapia contra el cáncer y en entornos espaciales, el estudio predice más de 30 categorías de daño en el ADN, incluidas 24 tipos de lesiones agrupadas. Los cálculos reproducen mediciones existentes de roturas de doble hebra para protones, helio, carbono y iones de hierro, lo que da confianza en las predicciones no observadas sobre los racimos. Para condiciones típicas médicas y relevantes en el espacio, se estima que el número total de racimos no–DSB es aproximadamente de cuatro a seis veces mayor que el número de roturas de doble hebra. Dentro de esos racimos no-DSB, las lesiones en tándem aparecen sorprendentemente a menudo: alrededor de la mitad a tres quintas partes tan frecuentes como los racimos biestrendiados, con solo un descenso moderado a medida que las trazas de radiación se vuelven más densas. El modelo también muestra que la mayoría de las roturas de doble hebra son en sí mismas “complejas”, contienen daño adicional de bases en las cercanías, lo que puede complicar la reparación.
Implicaciones para la salud, la terapia y los vuelos espaciales
El daño agrupado no-DSB no es solo un detalle contable. Estas lesiones concentradas son procesadas principalmente por las vías de reparación por escisión de bases, que pueden ser lentas y propensas a errores cuando muchas lesiones se sitúan en una región pequeña. Los intentos de reparación pueden convertir racimos no-DSB en roturas de doble hebra retardadas o en mutaciones mucho tiempo después de la exposición inicial. El nuevo modelo probabilístico ofrece una forma rápida de estimar estas lesiones ocultas para cualquier tipo de radiación, sin el elevado coste computacional de las simulaciones completas de trazas Monte Carlo. Sus predicciones sugieren que las normas de protección radiológica, la planificación de la radioterapia contra el cáncer y las evaluaciones de riesgo para astronautas deberían prestar tanta atención a estos racimos sutiles como a las más evidentes roturas de doble hebra.
Mensaje clave
En resumen, este trabajo muestra que la radiación produce muchos más daños de ADN no–DSB estrechamente agrupados de lo que se apreciaba anteriormente—varias veces más que las roturas de doble hebra francas—y que los racimos en tándem a lo largo de una sola hebra son casi tan comunes como los biestrendiados. Al combinar datos de deposición de energía con probabilidades multinomiales, el modelo ofrece una herramienta práctica para estimar estas lesiones invisibles en muchos tipos de radiación. Para el público general, el mensaje principal es que el daño más peligroso del ADN por radiación puede que no sea las raras y dramáticas roturas que podemos ver con facilidad, sino las numerosas pequeñas heridas agrupadas que desafían silenciosamente los sistemas de reparación celular.
Cita: Cucinotta, F.A. Multinomial probability model of radiation induced DSB and non-DSB clusters: tandem and bistranded damage clusters. Sci Rep 16, 7877 (2026). https://doi.org/10.1038/s41598-026-36157-2
Palabras clave: daño de ADN agrupado, biología de la radiación, radiación ionizante, radioterapia contra el cáncer, radiación espacial