Clear Sky Science · es
El paisaje transcripcional unicelular del pulmón pediátrico con fibrosis quística a partir de muestras respiratorias mínimamente invasivas
Por qué esto importa para los niños con fibrosis quística
La fibrosis quística es más conocida por el moco espeso y las infecciones pulmonares, pero bajo esos síntomas se libra una batalla compleja entre las células inmunitarias y el delicado revestimiento de las vías respiratorias. Este estudio se centra en esa batalla en niños, célula por célula, utilizando pequeñas muestras recogidas durante revisiones pulmonares de rutina. Al cartografiar qué células están presentes y cuán activas están, los investigadores muestran que los patrones dañinos de inflamación comienzan temprano en la vida y pueden ser difíciles de revertir, incluso con medicamentos modernos que corrigen el defecto genético subyacente.
Echar un vistazo a los pulmones jóvenes, una célula a la vez
Para explorar lo que ocurre dentro de los pulmones de los niños, el equipo empleó herramientas mínimamente invasivas durante broncoscopias flexibles—procedimientos que estos pacientes ya se sometían por razones médicas. Cepillaron suavemente la superficie interna de la tráquea y los bronquios y recogieron líquido de lavado de zonas más profundas del pulmón. Estas muestras procedían de dos niños con fibrosis quística (un lactante y un adolescente) y tres niños sin la enfermedad emparejados por edad. Usando secuenciación de ARN unicelular, una técnica que lee qué genes están activados en miles de células individuales, construyeron un mapa de alta resolución de las células inmunitarias y de las que revisten las vías respiratorias en los pulmones de cada niño. 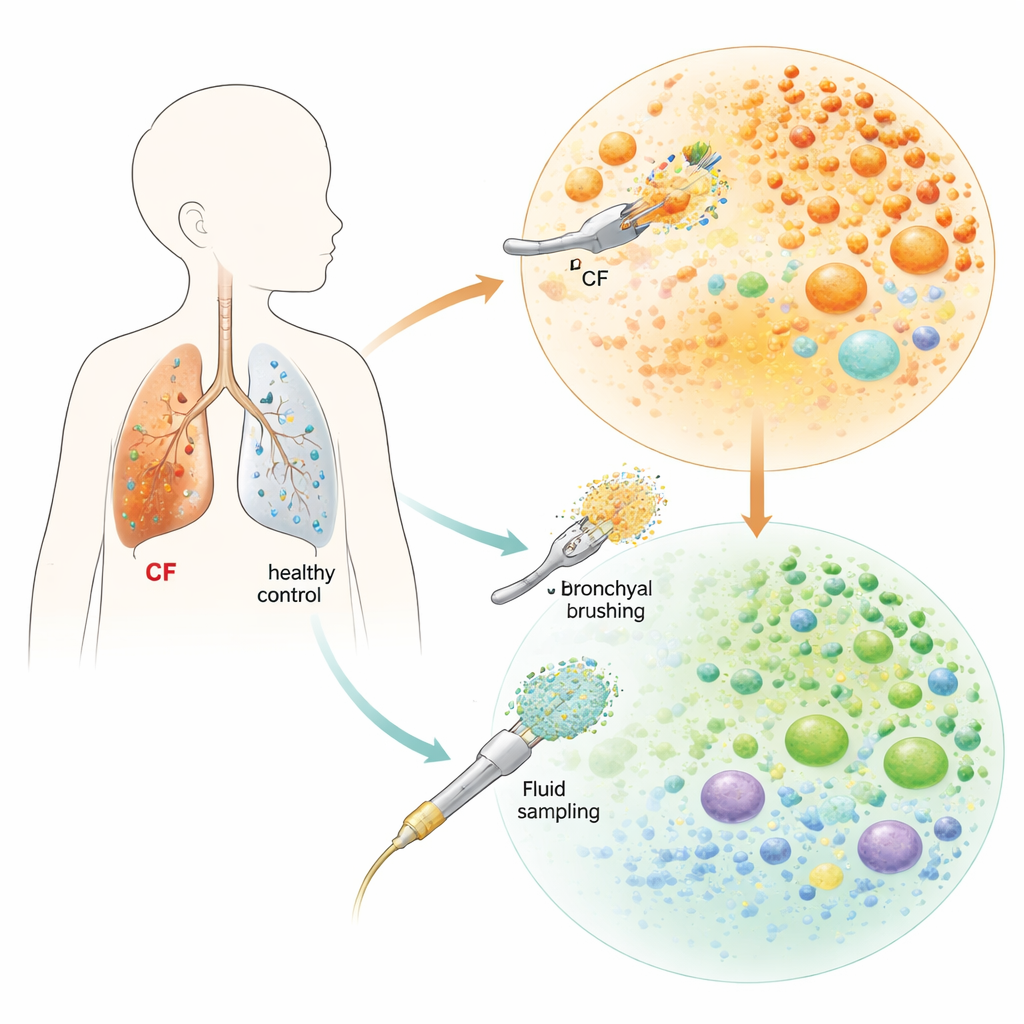
Un campo abarrotado de células inmunes de primera respuesta
En los niños sin fibrosis quística, las muestras de lavado pulmonar estaban dominadas por macrófagos—células «limpiadoras» que patrullan los espacios aéreos y ayudan a mantener la calma. En cambio, los niños con fibrosis quística mostraron un cambio dramático hacia los neutrófilos, glóbulos blancos de acción rápida que pueden dañar el tejido cuando persisten. No solo eran más abundantes, sino que aparecían en varias variantes distintas. Estas incluían formas inmaduras, células inflamatorias altamente activadas y un subconjunto llamativo marcado por proteínas de respuesta al estrés conocidas como proteínas de choque térmico. Si bien tales respuestas al estrés pueden comenzar siendo protectoras, pueden anclar a los neutrófilos en un estado agresivo y de larga duración que mantiene la inflamación encendida y puede impulsar el daño de las vías respiratorias observado en la fibrosis quística.
Defensores inflamados y refuerzos ausentes
Los macrófagos que permanecían en los pulmones con fibrosis quística también se veían diferentes. En lugar de la mezcla de tipos de mantenimiento común observada en el grupo de comparación, las muestras de fibrosis quística estaban enriquecidas en macrófagos que producen señales inmunitarias fuertes, lo que sugiere un desplazamiento hacia un papel más inflamatorio. Al mismo tiempo, había relativamente pocas células T—otro brazo clave del sistema inmunitario—en el líquido de las vías respiratorias de los niños con fibrosis quística. Trabajos previos han mostrado que los neutrófilos pueden privar a las células T de los nutrientes que necesitan para funcionar, empujándolas efectivamente fuera de la vía aérea. Esta combinación de neutrófilos agresivos, macrófagos activados y escasez de células T puede ayudar a explicar por qué los pulmones con fibrosis quística permanecen inflamados y propensos a la infección durante muchos años.
Un revestimiento de las vías respiratorias que se une a la lucha
Las muestras por cepillado permitieron a los investigadores observar las células que recubren las vías respiratorias: células basales (que pueden reponer el revestimiento), células ciliadas (con proyecciones similares a pelos que barren el moco) y células secretoras (que producen moco y moléculas protectoras). La mezcla global de estos tipos celulares fue similar entre los niños con fibrosis quística y los de comparación, pero su comportamiento no lo fue. En fibrosis quística, las células secretoras activaron genes vinculados a la defensa inmunitaria y a la actividad antimicrobiana, lo que sugiere que están trabajando en exceso como parte de la respuesta inflamatoria. Las células ciliadas también activaron genes relacionados con la inflamación y la resistencia a una forma de muerte celular asociada al hierro y al daño oxidativo. En conjunto, estos patrones apuntan a una superficie de la vía aérea que no es solo un observador pasivo, sino un participante activo e inflamado en el proceso de la enfermedad. 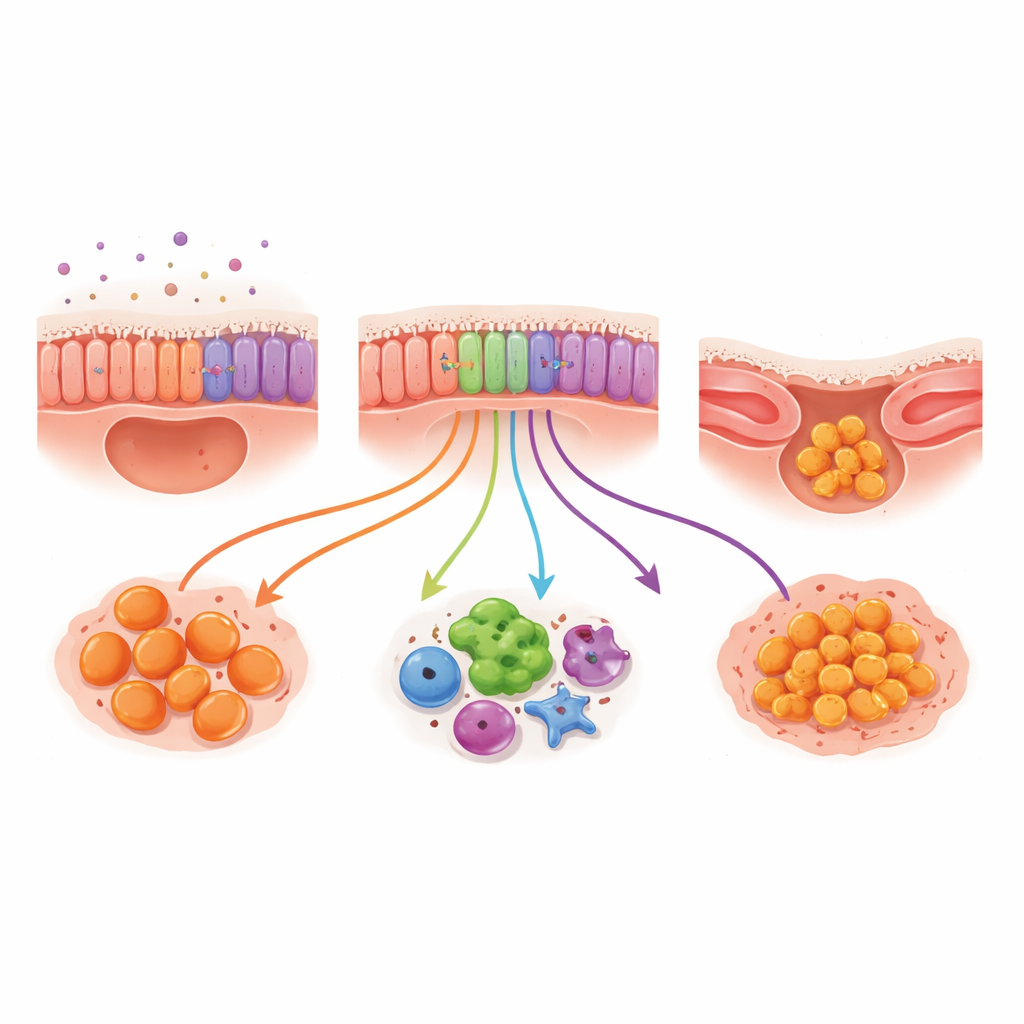
Conversaciones célula a célula que alimentan el daño pulmonar
Para entender cómo las células del revestimiento de las vías respiratorias y los neutrófilos se influyen mutuamente, el equipo analizó las «conversaciones» entre ellos—señales enviadas por un tipo celular y recibidas por otro. Encontraron que las células epiteliales a menudo actuaban como emisoras, usando varios sistemas moleculares para alcanzar a los neutrófilos. Algunas de estas señales probablemente ayudan a calmar la inflamación, mientras que otras animan a los neutrófilos a congregarse, activarse y engullir material. Este tira y afloja sugiere que el revestimiento de las vías respiratorias intenta equilibrar el control del daño y la defensa, pero en la fibrosis quística las señales proinflamatorias parecen imponerse, manteniendo el pulmón en un estado crónico de lesión latente.
Por qué los cambios tempranos son difíciles de revertir
Un hallazgo clave es que estos patrones inflamatorios estaban presentes tanto en un lactante como en un adolescente que había estado tomando un fármaco avanzado para la fibrosis quística que mejora la proteína defectuosa. A pesar de esta terapia dirigida, las células pulmonares del adolescente todavía se parecían más a las del lactante no tratado que a las de los niños de comparación. Esto implica que, una vez que se han desarrollado daño estructural e inflamación arraigada, restaurar simplemente la función proteica subyacente puede no ser suficiente para restablecer el paisaje inmunitario y epitelial. El estudio también muestra que el muestreo suave de las vías respiratorias, combinado con análisis genómicos unicelulares y espaciales, puede seguir estos cambios a lo largo del tiempo. Este enfoque podría ayudar a diseñar y probar nuevos tratamientos antiinflamatorios y antimicrobianos dirigidos a preservar la estructura pulmonar desde los primeros momentos de la vida.
Cita: Sun, Y., Vicencio, A.G., Beasley, M.B. et al. The single-cell transcriptional landscape of the pediatric cystic fibrosis lung from minimally invasive respiratory specimens. Sci Rep 16, 8113 (2026). https://doi.org/10.1038/s41598-026-36125-w
Palabras clave: pulmón con fibrosis quística, inflamación neutrofílica, secuenciación de ARN unicelular, epitelio de las vías respiratorias, broncoscopia pediátrica