Clear Sky Science · es
Las posiciones R5 y R7 en andamios fluoroquinolónicos impulsan la interrupción de filamentos de F-actina
Convertir antibióticos en aliados del cerebro
Muchos trastornos cerebrales comunes, desde el Alzheimer hasta la enfermedad de Parkinson, comparten un culpable oculto: diminutas varillas estructurales dentro de las neuronas que se atascan y se vuelven rígidas con el tiempo. Estas varillas están hechas de una proteína llamada actina, normalmente una parte flexible del andamiaje interno de la célula. Este estudio explora una posibilidad sorprendente: que una clase bien conocida de antibióticos, las fluoroquinolonas, podría rediseñarse para deshacer con suavidad estos nocivos haces de actina y, potencialmente, ayudar a proteger el cerebro.
Cuando los andamios celulares fallan
Las células cerebrales sanas remodelan constantemente su esqueleto interno para formar y rehacer conexiones. Los filamentos de actina son centrales en este proceso, formándose y disolviéndose según se necesite. Bajo estrés, sin embargo, la actina puede bloquearse en agregados rígidos en forma de varilla que obstruyen la célula, alteran el transporte de carga vital y favorecen la acumulación de proteínas vinculadas a enfermedad como la amiloide y la tau. Con los años, estas varillas pueden madurar hasta convertirse en estructuras densas conocidas como cuerpos de Hirano, que se observan con frecuencia en cerebros de personas con varias condiciones neurodegenerativas. Dado que los fármacos existentes que apuntan a la actina suelen ser extremadamente tóxicos, los investigadores buscan pequeñas moléculas más seguras que aflojen estos agregados sin dañar las células.
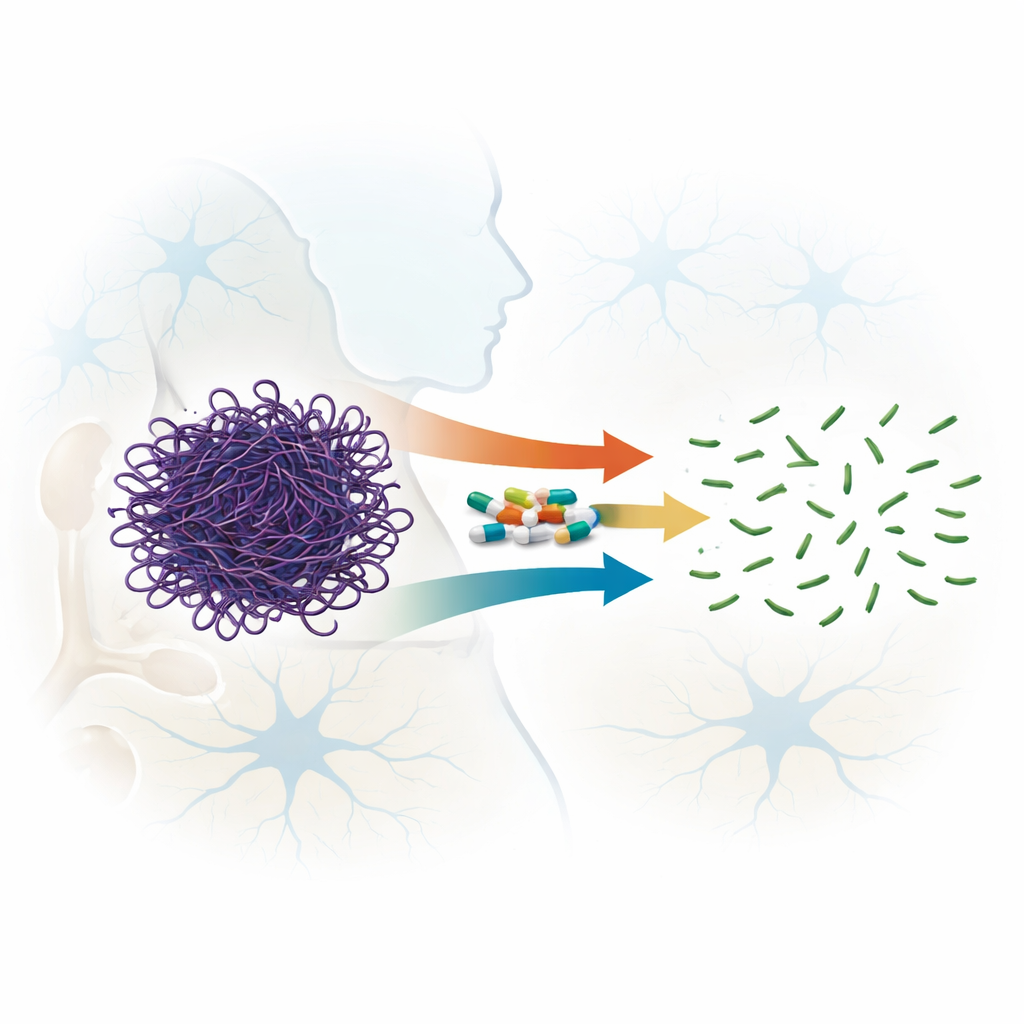
Un talento inesperado de fármacos familiares
Las fluoroquinolonas son antibióticos de amplio espectro usados en todo el mundo para tratar infecciones, y algunos miembros más recientes de esta familia pueden cruzar la barrera hematoencefálica. Indicios previos sugerían que ciertas fluoroquinolonas podían desestabilizar los filamentos de actina. En este trabajo, los autores compararon sistemáticamente siete compuestos relacionados, que abarcan cuatro generaciones de la familia, para ver qué tan bien desarman filamentos de actina ya formados en lugar de limitarse a impedir su formación. Mediante medidas de dispersión de luz, microscopía electrónica y filtración en gel, mostraron que todos los fármacos probados podían interrumpir los filamentos de actina, pero con fuerzas muy diferentes. Dos fármacos, sparfloxacino (un compuesto de tercera generación) y moxifloxacino (cuarta generación), destacaron por cortar rápida e irreversiblemente los filamentos largos en fragmentos mucho más pequeños, incluso a ratios fármaco:proteína relativamente bajos.
Ver cómo se desmoronan los filamentos
Imágenes de alta resolución y pruebas biofísicas revelaron cómo cambian los filamentos bajo el tratamiento farmacológico. La microscopía electrónica mostró que la actina no tratada forma hebras largas y continuas, mientras que las fluoroquinolonas efectivas las convierten en fragmentos cortos y dispersos. Los miembros menos potentes produjeron filamentos con quiebres y curvaturas pero no los rompieron completamente. Medidas térmicas de la estabilidad proteica confirmaron esta perturbación física: una vez tratados, los filamentos de actina se comportaron más como su forma libre y no ensamblada, con temperaturas de fusión más bajas, aunque su estructura de bloque básico permaneció casi sin cambios. Esto sugiere que los fármacos no desenrollan ni dañan la actina en sí, sino que separan principalmente la forma en que las unidades se adhieren entre sí en los filamentos.
Acercándose al agarre molecular
Para entender por qué algunas fluoroquinolonas funcionan mejor que otras, el equipo combinó experimentos avanzados de resonancia magnética nuclear con simulaciones computacionales de interacciones fármaco–proteína. Hallaron que todos los compuestos dependen de un “núcleo” en forma de anillo compartido para contactar la actina, especialmente en dos posiciones de ese núcleo que tocan repetidamente el filamento. Sin embargo, grupos químicos adicionales unidos en sitios específicos—denominados R5 y R7—influyen fuertemente en la firmeza y el lugar donde cada molécula se une. En los disruptores más efectivos, estas posiciones llevan un grupo amino y sistemas anulares voluminosos que se insertan en un pequeño bolsillo en la interfaz entre hebras vecinas de actina. Allí interfieren con contactos estabilizadores clave, incluida una puente salina importante que normalmente ayuda a mantener unidos los filamentos.
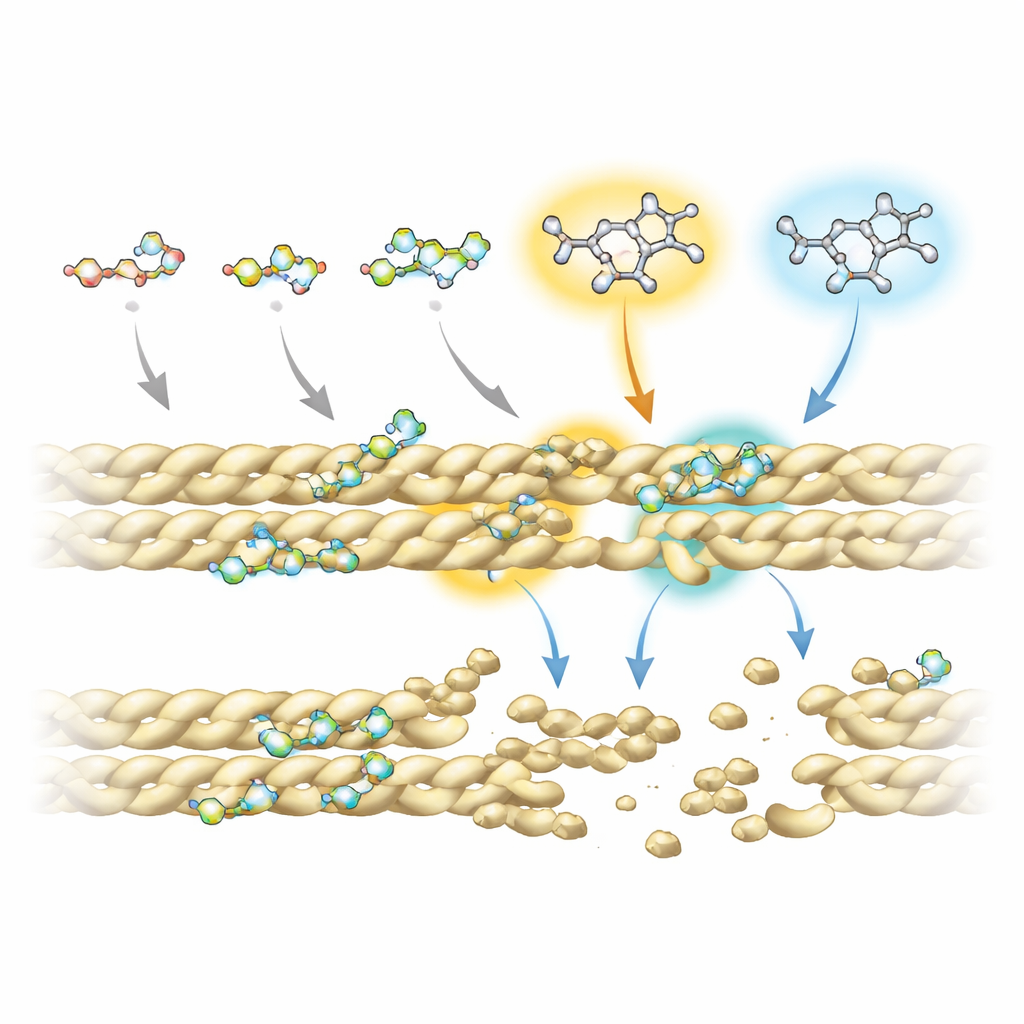
De células de levadura a futuras terapias
Los investigadores también probaron los fármacos en una cepa de levadura que acumula naturalmente haces de actina, imitando aspectos de las células enfermas. Al microscopio, la levadura no tratada mostró grandes y brillantes racimos de actina, mientras que las células expuestas a fluoroquinolonas—especialmente sparfloxacino, moxifloxacino y, a dosis más altas, ácido nalidíxico—presentaron patrones mucho más difusos y puntiformes, lo que indica que los haces se habían descompuesto. Importante, la acción de los fármacos pareció relativamente suave: debilitaron el empaquetamiento de los filamentos sin distorsionar de forma grave la forma subyacente de la actina, y su unión fue más débil que la de las toxinas clásicas contra la actina, lo que podría reducir el riesgo de efectos secundarios severos.
Diseñar fármacos más inteligentes que apunten a la actina
En conjunto, este estudio muestra que pequeños ajustes a antibióticos bien conocidos pueden cambiar drásticamente cómo interactúan con el andamiaje interno de la célula. Al identificar las posiciones R5 y R7 como “mandos de control” clave tanto para la disrupción de la actina como para la penetración cerebral, los autores trazan un plano para crear nuevas moléculas inspiradas en las fluoroquinolonas que desmantelen selectivamente los agregados nocivos de actina. Aunque estos hallazgos son una prueba de principio temprana en laboratorio, plantean la posibilidad de que futuros fármacos derivados de antibióticos familiares puedan ayudar a eliminar andamiajes tóxicos en las neuronas y frenar o prevenir algunas formas de neurodegeneración.
Cita: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
Palabras clave: agregados de actina, antibióticos fluoroquinolónicos, enfermedad neurodegenerativa, reutilización de fármacos, citoesqueleto