Clear Sky Science · es
La expresión de ACE2 en las células epiteliales del colon se asocia con infección viral, inmunidad y metabolismo energético
Por qué importa el intestino en un virus respiratorio
Cuando pensamos en la COVID-19, imaginamos pulmones llenos de líquido y pacientes con dificultad para respirar. Sin embargo, muchas personas infectadas por SARS-CoV-2 también presentan dolor abdominal, diarrea y problemas intestinales persistentes. Este estudio explora por qué los intestinos —especialmente el colon— pueden ser un objetivo importante para el virus. Al estudiar células individuales del colon de niños, los investigadores muestran que una puerta de entrada viral clave, la proteína ACE2, está muy activa en células intestinales específicas y se relaciona no solo con la infección viral sino también con nuestras defensas inmunitarias y con la forma en que las células gestionan la energía.
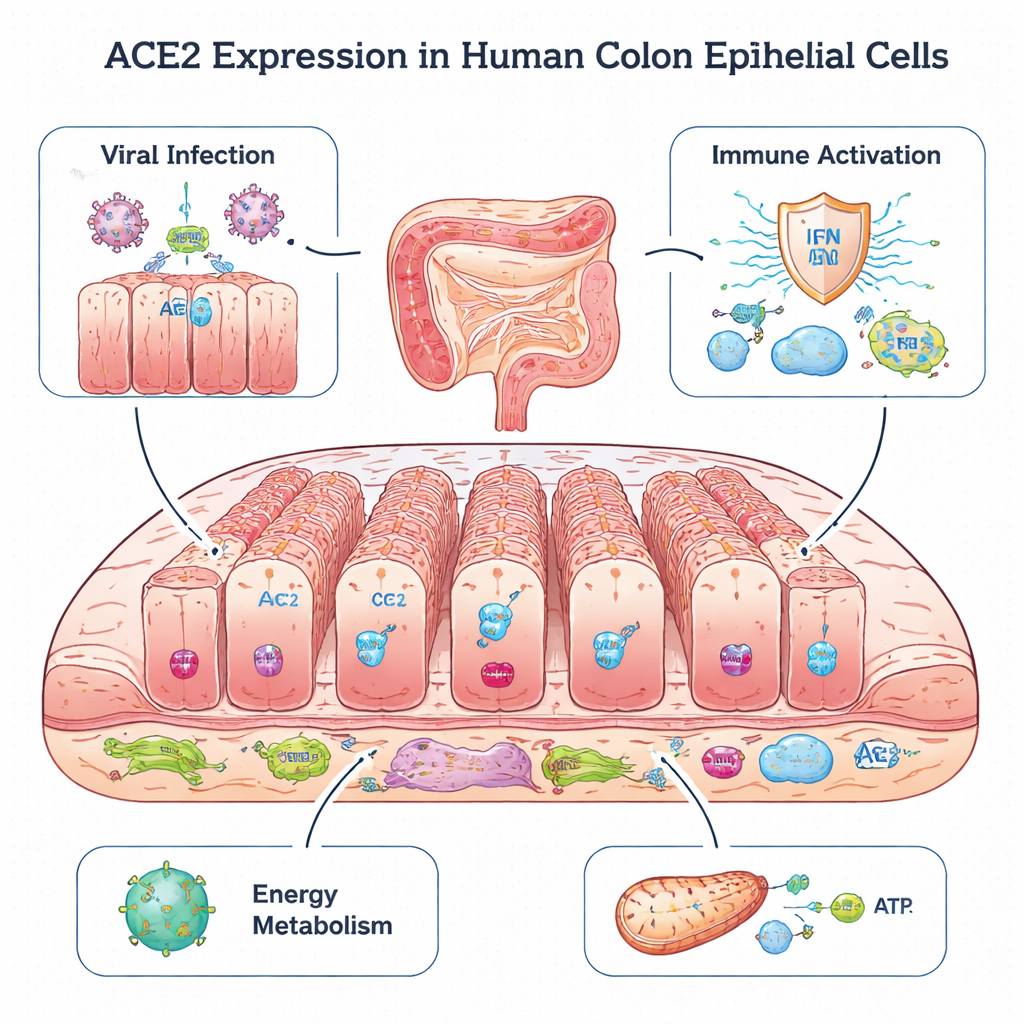
Una puerta celular en el colon
ACE2 es más conocida como el principal punto de entrada que tanto el SARS original como el SARS‑CoV‑2 utilizan para infectar células en el pulmón. Paradójicamente, estudios en animales sugieren que ACE2 también puede proteger los tejidos del daño al ayudar a mantener en equilibrio un sistema hormonal que controla la presión arterial. En el intestino, ya se sabe que ACE2 favorece un microbioma saludable y previene la inflamación. En este trabajo, los científicos volvieron a analizar datos de secuenciación de ARN de célula única a partir de biopsias de colon de 17 niños: algunos tenían intestinos sanos y otros colitis o enfermedad inflamatoria intestinal, incluida la colitis ulcerosa y la enfermedad de Crohn. Esta técnica les permitió ver qué genes están activos en miles de células individuales y localizar exactamente dónde se expresa ACE2.
Colonocitos: objetivos principales y primeros respondedores
El análisis reveló que ACE2 se concentra casi exclusivamente en los colonocitos, un tipo principal de célula epitelial que recubre el interior del colon y mira hacia el contenido intestinal. En comparación con otras células epiteliales, los colonocitos mostraron también mayor actividad de genes que ayudan a los virus a entrar en las células, brotar y salir. Al mismo tiempo, estas células expresaron muchos genes implicados en la detección de material genético viral y en el desencadenamiento de respuestas de interferón tipo I y tipo III, sistemas de alarma temprana clave de la defensa inmune. También produjeron señales inflamatorias y moléculas que presentan fragmentos virales a las células T, lo que sugiere que los colonocitos son tanto posibles blancos virales como centinelas tempranas importantes que alertan al sistema inmune.
Redes vinculadas de inmunidad y uso de energía
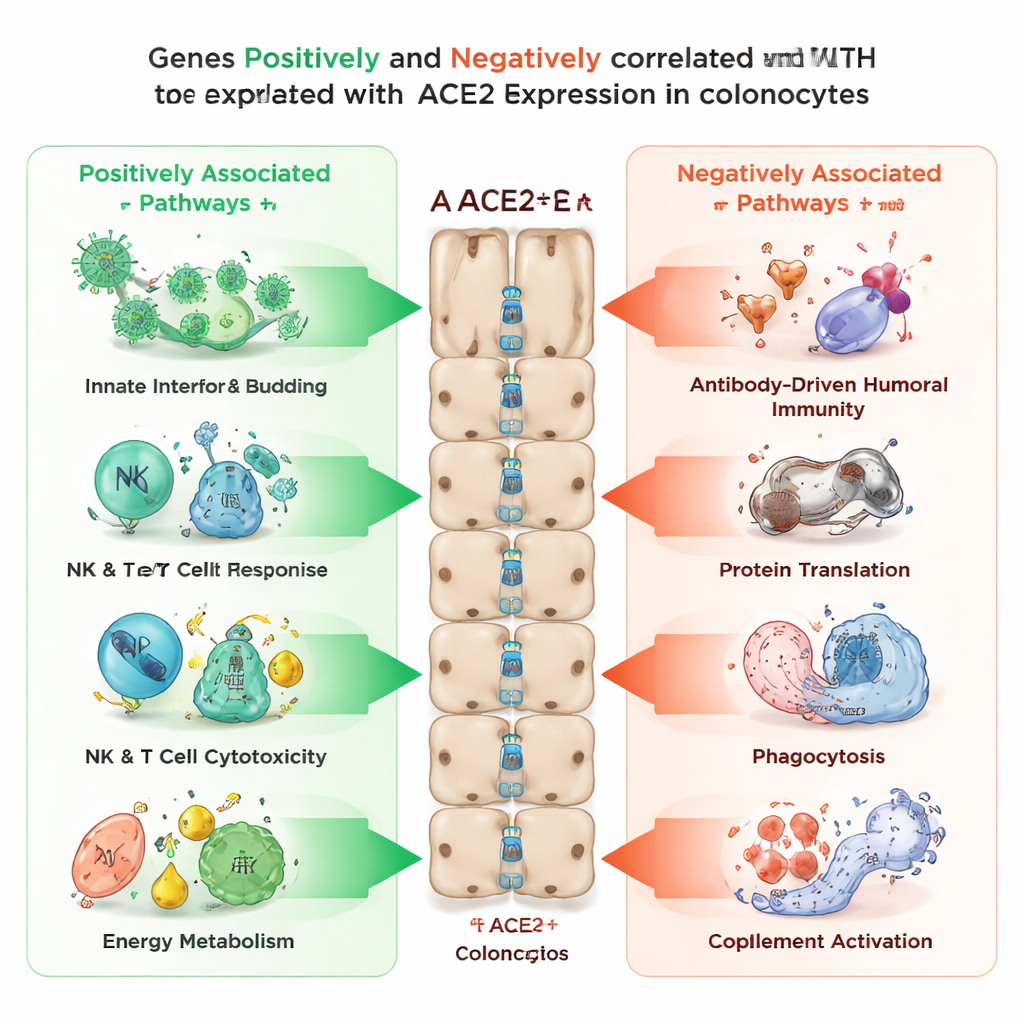
Los investigadores preguntaron luego qué otros genes tienden a activarse o desactivarse al mismo tiempo que ACE2 en los colonocitos. Encontraron más de 3.400 genes que aumentaban con los niveles de ACE2 y más de 2.100 que disminuían a medida que ACE2 aumentaba. Los genes con correlación positiva con ACE2 se enriquecieron en procesos relacionados con la entrada y salida viral, la señalización inmune innata, la actividad citotóxica de células NK y células T, y varias vías de producción de energía dentro de las células, incluida la función mitocondrial y el procesamiento de grasas y azúcares. En contraste, los genes que se movían en la dirección opuesta —altos cuando ACE2 era bajo— se asociaron con la inmunidad basada en anticuerpos (humoral), la maquinaria de síntesis proteica de la célula, procesos de fagocitosis y el sistema del complemento, otro brazo de la defensa inmune. Este patrón sugiere que ACE2 marca un estado en el que los colonocitos están orientados hacia una detección antiviral rápida y la producción de energía, mientras que otros programas inmunitarios más lentos están regulados a la baja.
Pruebas en intestinos inflamados
Para comprobar que estos patrones ocurren en tejidos reales, el equipo utilizó inmunofluorescencia multiplex —una técnica que ilumina proteínas específicas con diferentes colores— en muestras de colon de niños con colitis ulcerosa, enfermedad de Crohn y controles. Confirmaron que la proteína ACE2 se localiza principalmente en células epiteliales marcadas por EPCAM. En pacientes con enfermedad inflamatoria intestinal, las células ACE2‑positivas mostraron niveles más altos de IFNA4 y RSAD2, dos proteínas fuertemente asociadas con la señalización por interferón y la actividad antiviral. Esto indica que, en el intestino inflamado, las células colonocíticas que expresan ACE2 no son solo posibles puertas de entrada para virus; también son focos de respuesta antiviral.
Qué significa esto para los pacientes y las terapias futuras
Para el público general, el mensaje es que el colon no es un espectador pasivo en la COVID‑19. La misma proteína que permite la entrada del virus en las células también ayuda a coordinar la inmunidad intestinal y el uso de energía, sobre todo en niños con inflamación intestinal preexistente. Este doble papel puede ayudar a explicar por qué algunos pacientes desarrollan síntomas gastrointestinales y por qué las personas con enfermedad inflamatoria intestinal tienen resultados complejos, pero no necesariamente peores de forma generalizada, durante la COVID‑19. El trabajo también alimenta discusiones más amplias sobre fármacos que actúan sobre vías relacionadas con la coagulación y la presión arterial, algunos de los cuales podrían reducir el daño pulmonar y vascular en infecciones graves. Aunque el estudio se basa en correlaciones y no puede probar causa y efecto, destaca a las células del colon ricas en ACE2 como actores importantes en la intersección de la entrada viral, la defensa inmune y el metabolismo —señalando al intestino como un campo clave y potencialmente tratable en la enfermedad por coronavirus.
Cita: Qi, Y., Huang, Y., Chen, H. et al. ACE2 expression by colonic epithelial cells is associated with viral infection, immunity, and energy metabolism. Sci Rep 16, 5738 (2026). https://doi.org/10.1038/s41598-026-36052-w
Palabras clave: ACE2, colonocitos, COVID-19 intestinal, enfermedad inflamatoria intestinal, inmunidad antiviral