Clear Sky Science · es
Análisis proteómico del secretoma de células progenitoras endoteliales identifica a Serpine 1 como un potente regulador de la osteogénesis
Curar huesos rotos sin injertos de donante
Cuando un hueso está gravemente fracturado o falta un fragmento, los cirujanos a menudo tienen dificultades para restaurar tanto la resistencia como la forma. Las opciones actuales —tomar hueso de otra parte del cuerpo o usar injertos sintéticos— pueden ser dolorosas, conllevan riesgos y no siempre tienen éxito. Este estudio explora una idea diferente: en lugar de trasplantar células, ¿podemos administrar las proteínas naturales adecuadas para activar la maquinaria corporal de construcción ósea?
Por qué algunas lesiones óseas se niegan a sanar
La mayoría de las fracturas se reparan por sí solas, pero los grandes defectos óseos —como los causados por traumatismos, tumores o una severa reabsorción mandibular— a menudo no. En esos casos, el organismo simplemente no dispone de suficientes células vasculares locales ni de células madre formadoras de hueso para reconstruir el segmento perdido. Los investigadores en ingeniería de tejidos intentan resolver esto combinando tres ingredientes: células vivas capaces de formar nuevo hueso, un andamio que les proporcione una estructura sobre la que crecer y señales que les indiquen qué hacer. Los trasplantes celulares pueden funcionar, pero son caros, altamente regulados y no siempre prácticos para la clínica habitual. Esto ha impulsado la búsqueda de soluciones “sin células” basadas en biomateriales inteligentes y proteínas seleccionadas con precisión.
Señales secretadas por células que forman vasos
Las células progenitoras endoteliales son células poco abundantes en la sangre que ayudan a formar nuevos vasos sanguíneos. Trabajos previos mostraron que cuando estas células se implantan cerca del hueso, favorecen la curación, principalmente enviando señales solubles en lugar de convertirse en hueso. En el nuevo estudio, los autores recolectaron el medio de cultivo en el que estas células habían crecido y emplearon análisis proteómico avanzado para catalogar cientos de moléculas secretadas. Se centraron en ocho proteínas fuertemente vinculadas con el crecimiento vascular y la formación ósea. Utilizando células madre de médula ósea humana y células endoteliales microvasculares humanas en el laboratorio, probaron de forma sistemática cuáles de estas proteínas potenciaban mejor la proliferación celular, dirigían la migración y desencadenaban la deposición de mineral similar al óseo.
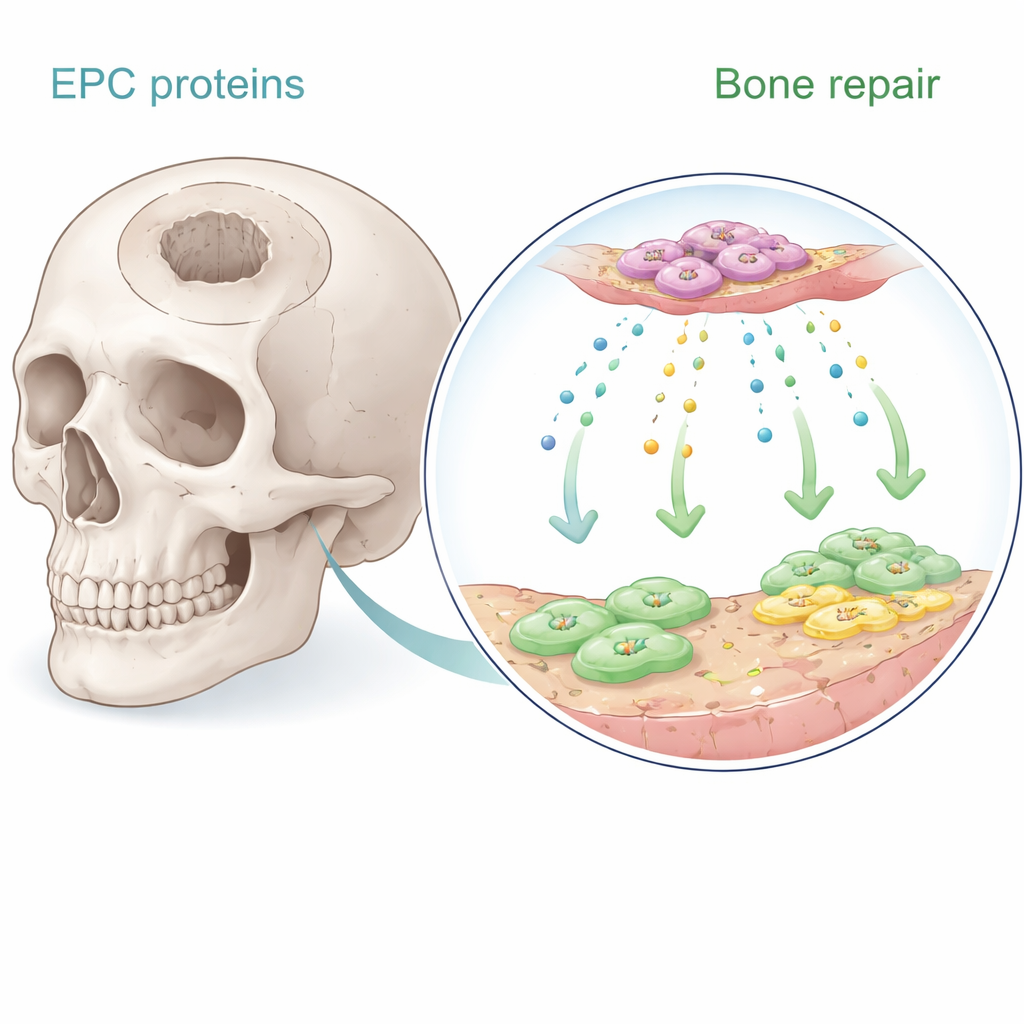
Una proteína sorprendente toma la delantera
Entre las candidatas, destacó una proteína: Serpine-1, más conocida por su papel en la regulación de la coagulación y la cicatrización. En placas de cultivo, Serpine-1 incrementó de forma significativa la proliferación tanto de las células madre de médula ósea como de las células endoteliales de forma dependiente de la dosis, rindiendo mejor que factores de crecimiento bien conocidos como BMP-2 y SDF-1 en este aspecto. También promovió la maduración de las células madre hacia fenotipos formadores de hueso, tal como mostraron tinciones clásicas que revelan la actividad de la fosfatasa alcalina y la presencia de depósitos minerales ricos en calcio. Otras proteínas, como el factor de crecimiento derivado de plaquetas y BMP-2, fueron más eficaces para animar a las células a desplazarse hacia un área de “herida” en ensayos de migración, pero Serpine-1 ofreció la rara combinación de aumentar tanto el número celular como el comportamiento osteogénico.
Convertir una proteína en un implante práctico
Encontrar una proteína prometedora es solo la mitad del reto; también debe administrarse en el sitio de la lesión de manera controlada. El equipo encapsuló Serpine-1 dentro de pequeñas esferas biodegradables hechas de un polímero médico llamado PLGA, y luego mezcló estas microsferas en un gel blando de colágeno. Esto creó un andamio que liberaba la proteína de forma lenta y sostenida. Lo probaron en ratones practicando un orificio circular de 4 milímetros en el cráneo, un defecto de tamaño que no se cura por sí solo. Algunos defectos se rellenaron solo con colágeno, otros con colágeno más microsferas vacías y otros con el andamio cargado con Serpine-1. Tras ocho semanas, escaneos micro-CT de alta resolución mostraron que el grupo tratado con Serpine-1 presentaba un volumen óseo, densidad y grosor significativamente mayores dentro del defecto. De forma notable, solo estos animales desarrollaron nuevo hueso en el centro de la brecha, en lugar de limitarse a los bordes.
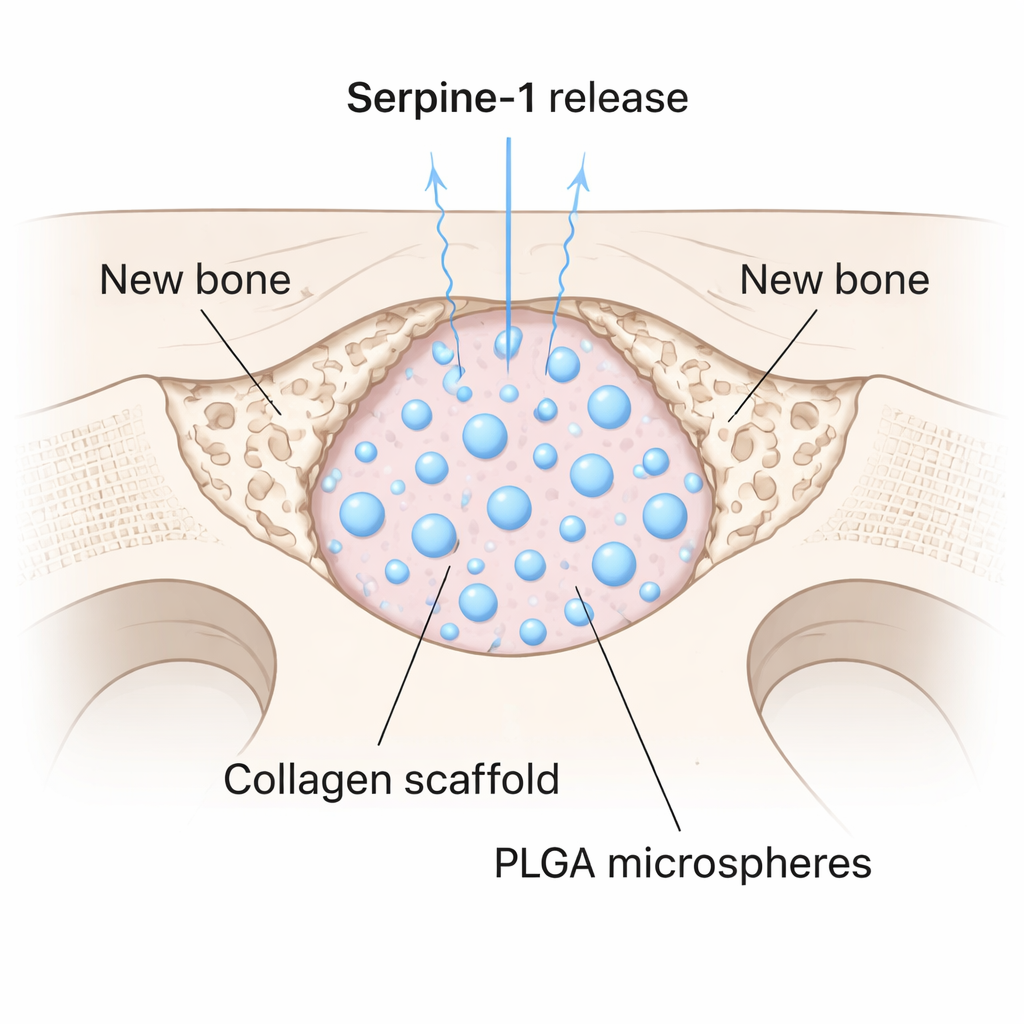
Qué podría significar esto para el cuidado óseo futuro
El estudio presenta a Serpine-1 como una señal poderosa y hasta ahora subestimada para la formación ósea. Al emparejar esta proteína con un andamio de liberación lenta, los investigadores lograron una regeneración ósea significativa en un defecto que normalmente permanecería vacío. Aunque Serpine-1 no atrajo células hacia el defecto tan eficazmente como algunos otros factores, su capacidad para ayudar a que las células existentes se multipliquen y maduren sugiere que podría combinarse con proteínas que promueven la migración para obtener resultados aún mejores. Para los pacientes, este tipo de materiales sin células y basados en proteínas podría algún día reducir la necesidad de extraer hueso del propio cuerpo o depender de terapias celulares complejas, ofreciendo una manera más sencilla de inducir la curación de lesiones óseas persistentes.
Cita: Asbi, T., Tamari, T., Doppelt-Flikshtain, O. et al. Proteomic analysis of endothelial progenitor cells secretome identifies Serpine 1 as a potent regulator of osteogenesis. Sci Rep 16, 5165 (2026). https://doi.org/10.1038/s41598-026-36048-6
Palabras clave: regeneración ósea, Serpine-1, ingeniería de tejidos, células progenitoras endoteliales, andamio de colágeno