Clear Sky Science · es
El aprendizaje auto-supervisado en grafos predice asociaciones entre ARN no codificante y enfermedades
Por qué los ARN ocultos importan para nuestra salud
La mayoría aprendimos que la función principal del ARN es ayudar a construir proteínas. Pero en la última década los científicos han descubierto una gran cantidad de ARN “no codificantes” que nunca se convierten en proteínas y, aun así, regulan el funcionamiento celular. Hoy se sabe que muchos de estos moléculas promueven o inhiben cánceres y otras enfermedades complejas. Identificar qué ARN no codificantes están vinculados a qué enfermedades podría revelar nuevas formas de diagnosticar precozmente o diseñar tratamientos más precisos, pero probar todas las posibilidades en el laboratorio sería imposiblemente lento. Este estudio presenta un método computacional potente que puede cribar enormes redes biológicas y proponer de forma fiable las conexiones ARN–enfermedad más prometedoras para que los investigadores las verifiquen experimentalmente.
De desechos a piezas clave de la célula
Durante años, los ARN no codificantes se descartaron como restos sin sentido de la actividad génica. Hoy sabemos que familias como los microARN, los ARN largos no codificantes y los ARN circulares ayudan a coordinar procesos vitales, desde el empaquetamiento del ADN hasta la activación y desactivación de genes y la transmisión de señales dentro de las células. Debido a que participan en numerosos puntos de control, incluso cambios pequeños en estos ARN pueden inclinar el equilibrio hacia el cáncer u otras enfermedades. Los clínicos ya los consideran potenciales biomarcadores y dianas terapéuticas. El problema es la escala: existen miles de ARN distintos y cientos de enfermedades, y los experimentos tradicionales para probar cada enlace posible son caros y consumen mucho tiempo. Ahí es donde entra la predicción computacional, que ofrece una forma de reducir el espacio de búsqueda.
Cómo leer una red biológica
Los métodos computacionales previos intentaron predecir enlaces ARN–enfermedad fragmentando grandes tablas de datos o entrenando modelos de aprendizaje automático con ejemplos conocidos. Estos enfoques ayudaron, pero a menudo ignoraron cómo los ARN y las enfermedades están entrelazados en redes. Las modernas “redes neuronales de grafos” tratan a ARN y enfermedades como nodos conectados por aristas, similar a una red social. Pueden aprender patrones sobre quién está conectado con quién. Sin embargo, la mayoría de estos métodos de grafos necesitan muchos ejemplos de entrenamiento fiables y numerosas características de entrada cuidadosamente diseñadas. Eso los hace sensibles a datos faltantes, mediciones ruidosas y sobreajuste: funcionan bien con datos conocidos pero fallan al predecir asociaciones nuevas.
Aprender a partir de los propios datos
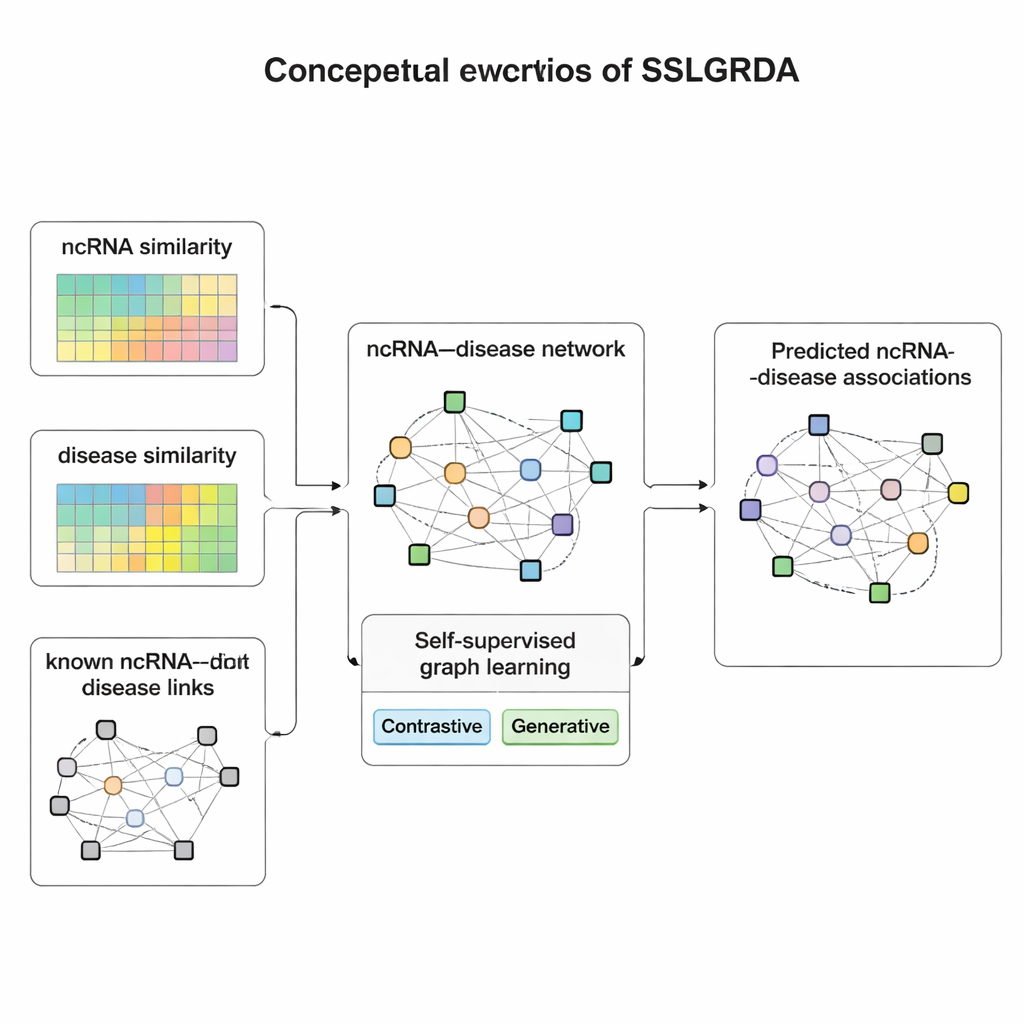
Los autores presentan SSLGRDA, un nuevo marco que enseña a un modelo de grafos a aprender patrones útiles sin depender en gran medida de datos etiquetados. La idea clave es el “aprendizaje auto-supervisado”: en lugar de decirle al modelo qué ARN corresponde a qué enfermedad, el modelo se inventa sus propias tareas de práctica basadas únicamente en la estructura y los atributos de la red. Los investigadores construyen dos tipos de grafos. Uno mantiene ARN y enfermedades como tipos de nodos distintos conectados por enlaces conocidos. El otro los integra en una sola gran red que también incluye información de similitud—qué tan parecidos son dos ARN o dos enfermedades—de modo que incluso elementos pobremente conectados ganan vecinos de apoyo. Sobre estos grafos, SSLGRDA emplea dos estilos de autoentrenamiento. Las estrategias contrastivas piden al modelo que reconozca que diferentes “vistas” de un mismo nodo (por ejemplo, sus conexiones frente a sus atributos) deben producir representaciones internas similares, mientras separan claramente nodos no relacionados. Las estrategias generativas ocultan deliberadamente partes de las características de entrada y desafían al modelo a reconstruirlas, animándole a captar estructura profunda en lugar de memorizar ruido.
Poniendo el método a prueba
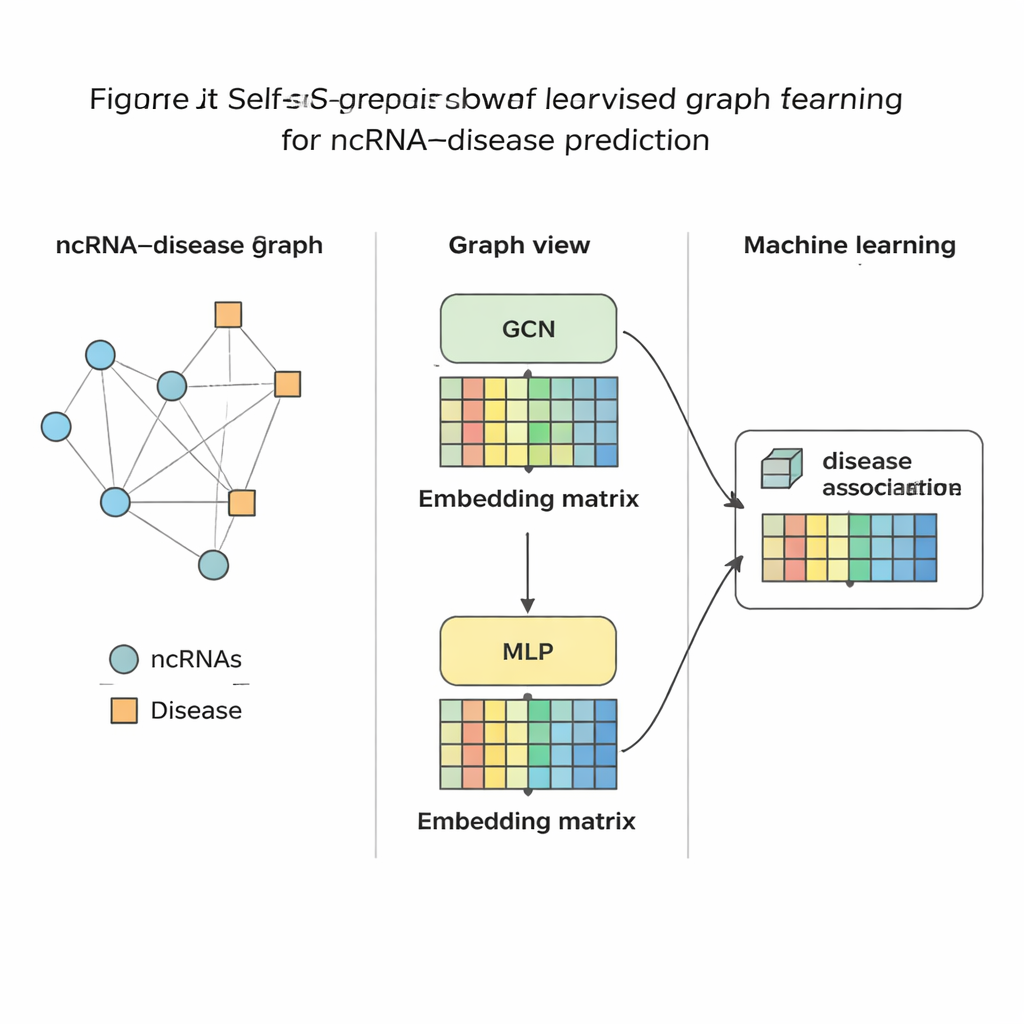
Una vez que SSLGRDA ha destilado cada ARN y cada enfermedad en una huella numérica compacta, se entrena un clasificador estándar de aprendizaje automático para juzgar si un enlace entre ellos es probable o no. Los autores evaluaron este enfoque en nueve conjuntos de datos diferentes que abarcan tres tipos principales de ARN y cientos de enfermedades. En general, sus variantes auto-supervisadas contrastivas sobre el grafo integrado (homogéneo) fueron las más eficaces, superando a varias herramientas existentes, incluidas fuertes líneas base basadas en grafos. El método no solo alcanzó mayor precisión en pruebas globales, sino que también situó a los socios correctos cerca de la parte superior cuando se enfocó en un ARN o una enfermedad a la vez—crucial para el uso real, donde un biólogo puede comenzar por un cáncer concreto y preguntar qué ARN estudiar. Además, mostraron que las mismas ideas se transfieren bien a otras redes biomédicas, como las que conectan microbios con enfermedades o fármacos.
De las predicciones a posibles terapias
Para demostrar su valor práctico, el equipo aplicó SSLGRDA para buscar nuevos ARN no codificantes implicados en cáncer de mama, cáncer de colon y varias otras condiciones. Muchas de las sugerencias mejor clasificadas se confirmaron posteriormente en bases de datos independientes o en informes científicos, lo que respalda la capacidad del modelo para detectar patrones biológicamente significativos. Para el público no especializado, la conclusión es que este trabajo ofrece una manera más inteligente de extraer pistas ocultas sobre enfermedades de la maraña de datos biológicos en expansión. Al aprender automáticamente cómo se agrupan e interactúan ARN y enfermedades, los métodos de grafos auto-supervisados como SSLGRDA pueden guiar a los investigadores de laboratorio hacia los objetivos más prometedores, acelerando potencialmente el recorrido desde los datos crudos hasta mejores diagnósticos y tratamientos.
Cita: Wu, Q., Tang, S. Self-supervised learning on graphs predicts non-coding RNA and disease associations. Sci Rep 16, 5231 (2026). https://doi.org/10.1038/s41598-026-36030-2
Palabras clave: ARN no codificante, asociación con enfermedades, redes neuronales de grafos, aprendizaje auto-supervisado, biología computacional