Clear Sky Science · es
SULT1E1 ejerce un papel protector en la EPOC al inhibir la vía AKT: un estudio in vivo e in vitro
Por qué una enzima pulmonar importa para la respiración cotidiana
La enfermedad pulmonar obstructiva crónica (EPOC) es una de las principales causas de muerte en el mundo, y aun así los médicos carecen de herramientas para detenerla en sus inicios o revertir su daño. Este estudio arroja luz sobre un actor inesperado en la EPOC: una pequeña enzima llamada SULT1E1 que ayuda a procesar hormonas y compuestos químicos en el organismo. Siguiendo esta enzima desde grandes conjuntos de datos hasta muestras de sangre de pacientes, pulmones de animales y células cultivadas, los investigadores encuentran evidencias de que SULT1E1 actúa como una especie de escudo incorporado para las vías respiratorias; y que su pérdida podría contribuir al avance de la EPOC.
Una nueva mirada a una enfermedad pulmonar conocida
La EPOC no es una sola dolencia sino un conjunto de problemas pulmonares crónicos, que incluye bronquitis crónica y enfisema, generalmente desencadenados por la exposición prolongada al humo o al aire contaminado. Con el tiempo, las vías respiratorias se inflaman, presentan fibrosis y se obstruyen con mucosidad, dejando a las personas sin aliento con incluso un esfuerzo leve. Los tratamientos actuales alivian principalmente los síntomas; hacen poco por detener el daño lento e irreversible del tejido pulmonar. Por eso los científicos buscan nuevas pistas moleculares —proteínas o vías que no solo indiquen la gravedad de la enfermedad, sino que también puedan ser dianas para proteger o reparar los pulmones.
Rastreando una enzima a través de conjuntos de datos y pacientes
Los investigadores comenzaron por analizar cuatro grandes conjuntos de datos públicos de expresión génica de tejido pulmonar humano, comparando muestras de personas con EPOC y de individuos sin la enfermedad. Entre cientos de genes que mostraban diferencias, SULT1E1 destacó por estar marcadamente reducida en pulmones con EPOC. Esta enzima normalmente contribuye a desactivar el estrógeno y otras hormonas y participa en el manejo seguro de fármacos y compuestos extraños. Los análisis de redes y vías mostraron que SULT1E1 está vinculada a muchas proteínas metabólicas y relacionadas con hormonas, lo que sugiere que cambios en su nivel podrían propagarse a través de múltiples sistemas relevantes para la salud pulmonar.
Para comprobar si este patrón se mantenía más allá de las pantallas del ordenador, el equipo midió SULT1E1 en pacientes reales. En muestras de sangre de 92 personas con EPOC y 40 voluntarios sanos, tanto el nivel de proteína en suero como la actividad génica en células inmunitarias fueron significativamente más bajos en el grupo con EPOC. Importante fue que quienes presentaban los niveles más bajos de SULT1E1 tendían a tener la función pulmonar más deteriorada, según pruebas respiratorias estándar (FEV1% y la relación FEV1/FVC). Este vínculo estrecho sugiere que SULT1E1 podría servir como un marcador sencillo basado en sangre del grado de progresión de la EPOC.
Pruebas en pulmones animales y células cultivadas
La historia no se detuvo en los análisis de sangre. En un modelo de rata expuesto a irritantes que imitan la EPOC humana, los animales desarrollaron el daño pulmonar clásico a la microscopía, y su tejido pulmonar mostró también una caída notable de la proteína SULT1E1. Para entender qué hace realmente esta enzima en las células de las vías respiratorias, los científicos recurrieron a una línea celular bronquial humana cultivada en placas. Cuando redujeron SULT1E1, las células proliferaron más rápido, resistieron la muerte celular programada y empezaron a adoptar rasgos asociados con la cicatrización y el endurecimiento del tejido —un proceso denominado transición epitelio‑mesénquima (EMT). Al aumentar SULT1E1, todos estos cambios se invirtieron: la proliferación se ralentizó, la muerte celular volvió hacia niveles normales y los marcadores de EMT disminuyeron.
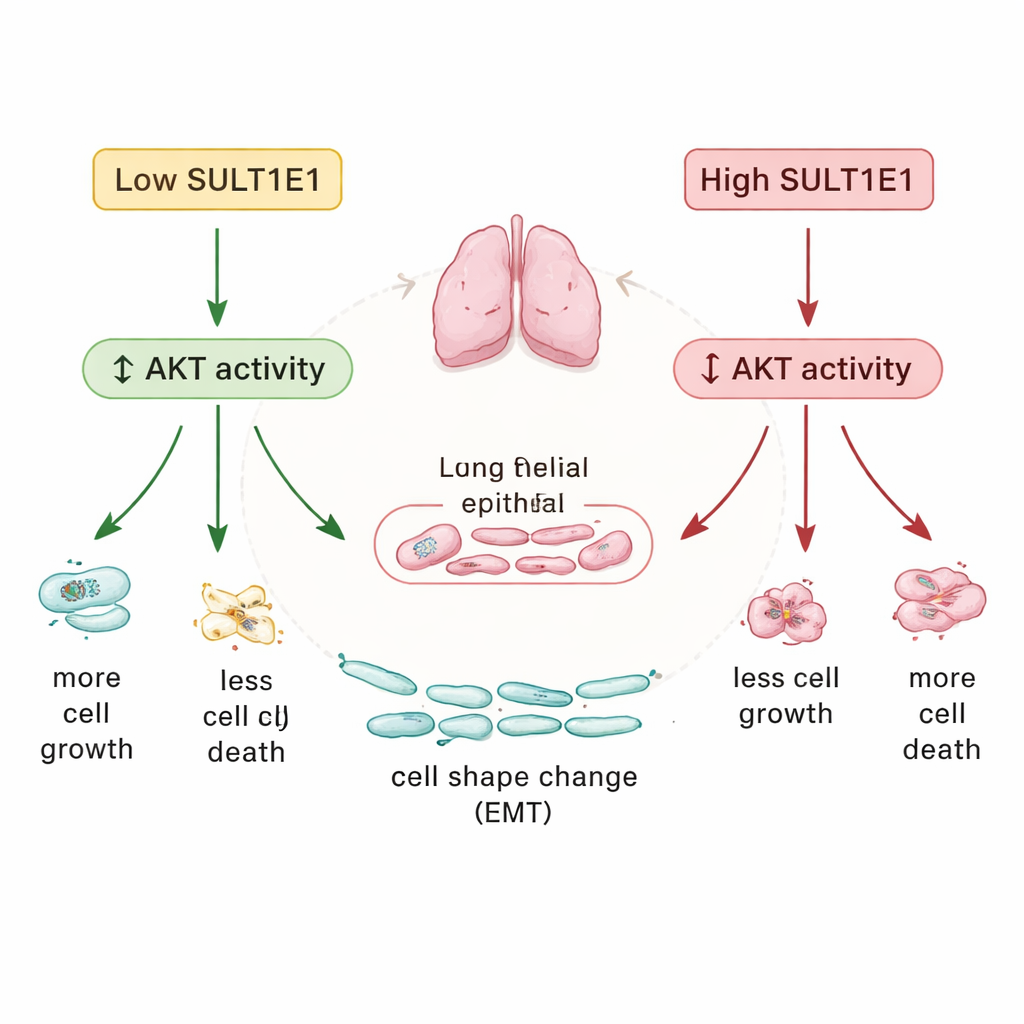
El interruptor de señal que conecta las piezas
Indagando más, el equipo atribuyó estos efectos a una vía de señalización central dentro de las células conocida como la vía AKT, que ayuda a controlar el crecimiento, la supervivencia y las respuestas al estrés. En las células pulmonares carentes de SULT1E1, AKT estaba más fuertemente activada; con exceso de SULT1E1, la actividad de AKT descendía. En otras palabras, SULT1E1 parece actuar como un freno natural sobre la señalización AKT. Cuando ese freno falla en la EPOC, el resultado es un cambio hacia un crecimiento celular excesivo, una reducción del recambio celular y alteraciones estructurales en el revestimiento de las vías respiratorias —todos rasgos característicos de la enfermedad. Los investigadores especulan que esto podría deberse en parte al manejo alterado del estrógeno, que a su vez puede potenciar la activación de AKT, aunque también son posibles funciones no hormonales de SULT1E1.
Qué podría significar esto para las personas con EPOC
En conjunto, los hallazgos presentan a SULT1E1 como un guardián discreto de los pulmones: cuando está presente en niveles saludables, mantiene bajo control señales clave de crecimiento y supervivencia, ayudando a conservar un revestimiento de las vías respiratorias estable. En la EPOC, ese guardián se pierde o debilita, y la vía AKT se sobreactiva, promoviendo la hiperproliferación y la fibrosis de las células de las vías respiratorias. Para los pacientes, este trabajo ofrece dos perspectivas principales. Primero, SULT1E1 en sangre podría convertirse en un marcador cómodo para valorar la gravedad de la enfermedad o seguir la respuesta al tratamiento. Segundo, fármacos que aumenten la actividad de SULT1E1 —o que imiten su efecto modulador sobre AKT— podrían algún día constituir una nueva clase de terapias dirigidas pensadas no solo para aliviar los síntomas, sino para frenar el daño subyacente que dificulta la respiración.
Cita: Song, W., Zhang, W., Wang, F. et al. SULT1E1 exerts a protective role in COPD by inhibiting the AKT pathway: an in vivo and in vitro study. Sci Rep 16, 6238 (2026). https://doi.org/10.1038/s41598-026-35997-2
Palabras clave: EPOC, SULT1E1, inflamación pulmonar, señalización AKT, biomarcador