Clear Sky Science · es
Efectos del hacinamiento molecular en la estabilidad de las proteínas en un proteoma bacteriano
Por qué importa la vida abarrotada de las proteínas
Dentro de cada célula viva, las proteínas realizan sus funciones en un espacio tan repleto de otras moléculas que casi la mitad del volumen puede estar ocupada. Sin embargo, la mayoría de los experimentos de laboratorio estudian proteínas en soluciones diluidas, casi vacías. Este artículo plantea una pregunta simple pero importante: ¿cómo cambia esta realidad saturada la estabilidad y el comportamiento de las proteínas, y qué implica eso para el funcionamiento de la vida a escala molecular?
Mirando en un mundo celular lleno
Para explorar esto, los investigadores trabajaron con una bacteria llamada Cupriavidus necator, un microbio de interés para tecnologías verdes como la captura de carbono y la producción de bioplásticos. Abrieron las células con cuidado, conservando cientos de proteínas cercanas a sus formas naturales. Luego añadieron altas concentraciones de polímeros grandes y hidrófilos —agentes de hacinamiento comunes llamados PEG, dextrano y Ficoll— que suelen usarse para imitar el interior denso de las células.
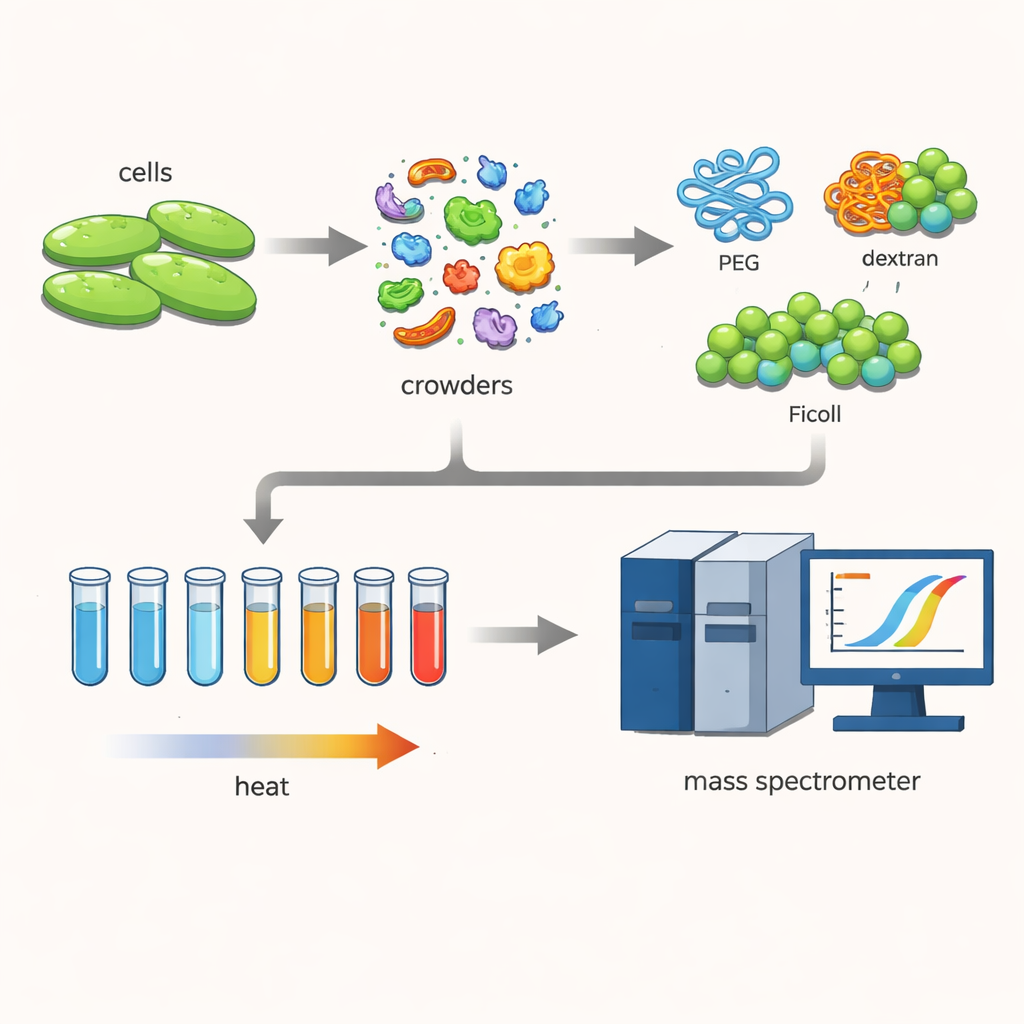
Observando cómo se ‘‘deshacen’’ las proteínas
El equipo usó una técnica conocida como perfilado térmico del proteoma. Calentaron muchas pequeñas muestras de la mezcla proteica paso a paso desde 30 hasta 70 grados Celsius. A medida que subía la temperatura, las proteínas menos estables se desdoblaban y se agrupaban, saliendo de la solución. Etiquetando las proteínas solubles que quedaban y midiéndolas con un espectrómetro de masas sensible, los científicos pudieron reconstruir curvas de fusión para cada proteína y determinar su temperatura de fusión —el punto en el que la mitad ha abandonado el estado soluble y funcional. Comparar estas temperaturas con y sin agentes de hacinamiento reveló cómo el entorno denso desplazaba la estabilidad proteica.
Un panorama mixto: algunas proteínas más firmes, otras más frágiles
En promedio, añadir cualquiera de los seis polímeros hizo bajar las temperaturas de fusión en todo el proteoma bacteriano, lo que implica un efecto desestabilizador leve a escala global. Pero esta tendencia general ocultó una historia mucho más matizada. Para decenas de proteínas individuales, los agentes de hacinamiento aumentaron o disminuyeron claramente la estabilidad, a veces por varios grados. La mayoría de las proteínas se vieron afectadas por sólo uno de los seis reactivos, pero un puñado respondió a varios, y casi todas estas mostraron estabilización o desestabilización consistente, lo que sugiere características subyacentes compartidas en cómo interactúan con los agentes de hacinamiento.
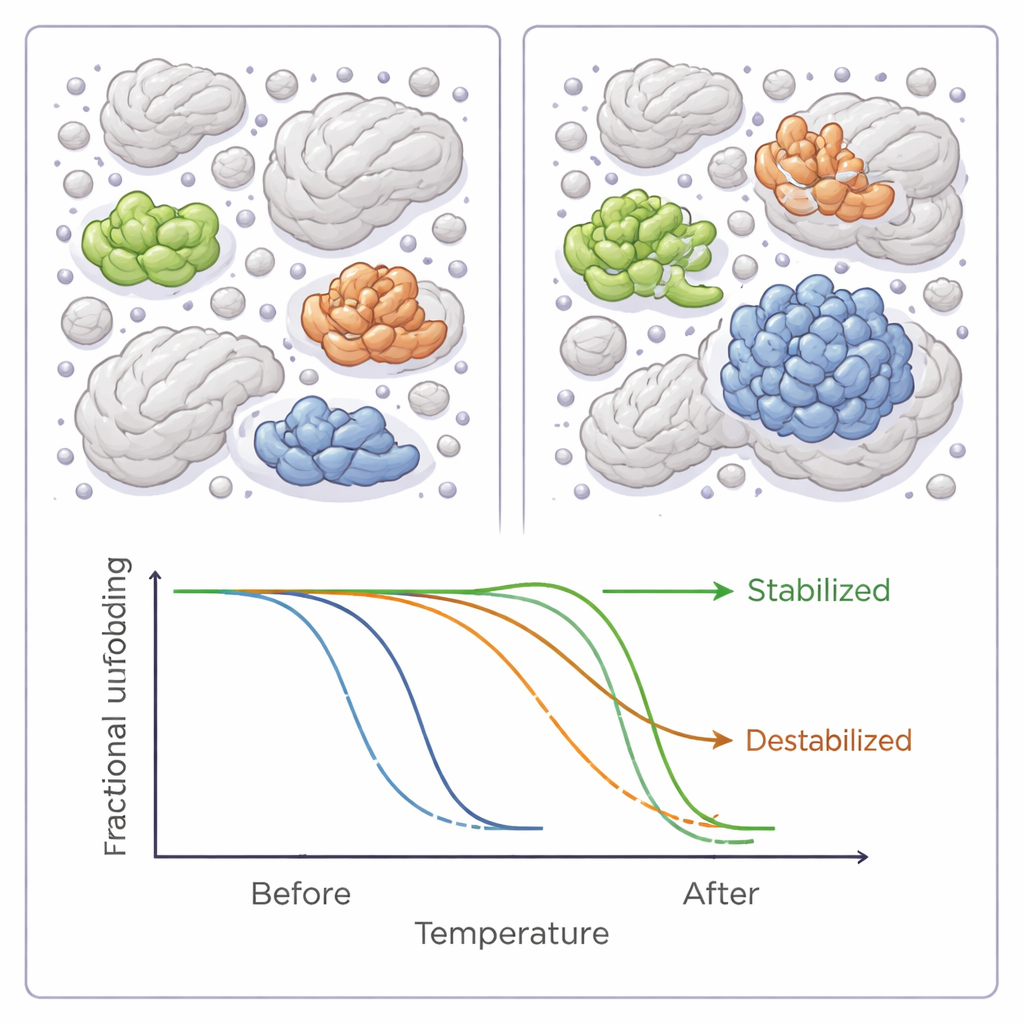
Qué hace que una proteína gane o pierda en una multitud
Cuando los autores examinaron más de cerca las propiedades de estas proteínas sensibles surgieron patrones. Las proteínas que se volvían más estables en condiciones de hacinamiento tendían a ser más hidrofóbicas —es decir, tenían superficies que repelen el agua— y eran más a menudo enzimas clásicas con sitios activos bien definidos. También era más probable que participaran en interacciones proteína‑proteína o que llevasen modificaciones químicas que regulan su función. Las proteínas desestabilizadas, en cambio, eran de media más pequeñas y menos ornamentadas con tales modificaciones. Estos hallazgos coinciden con modelos computacionales y otros experimentos que sugieren que el hacinamiento puede favorecer a algunas proteínas y hacer a otras más vulnerables, según su tamaño, forma y cómo interactúan normalmente con socios.
Más allá del simple apretón: cómo actúan realmente los crowders
Las explicaciones tradicionales del hacinamiento molecular se centran en el «volumen excluido», la idea de que las moléculas grandes simplemente dejan menos espacio, empujando a las proteínas a permanecer plegadas. Si esa fuera toda la historia, cabría esperar que los agentes de hacinamiento estabilizaran principalmente las proteínas y que hubiera vínculos fuertes con lo voluminosos o viscosos que sean los polímeros. En cambio, los autores observaron solo conexiones débiles con el tamaño y la densidad de los polímeros. Sus datos encajan mejor con una imagen de «exclusión preferencial»: los crowders y las proteínas se evitan químicamente, lo que indirectamente favorece ciertos estados plegados pero también puede perturbar interacciones delicadas que mantienen estables a otras proteínas. En resumen, no es solo apretamiento físico, sino un empuje y tirón químico sutil lo que moldea el comportamiento proteico.
Qué significa esto para entender la química de la vida
Para quienes no son especialistas, el mensaje clave es que las proteínas dentro de las células no pueden entenderse completamente en aislamiento, nadando en un tampón claro. La jungla molecular densa que las rodea puede hacer que algunas proteínas sean más robustas y otras más frágiles, cambiando cómo se comportan redes enteras de reacciones. Este estudio, al medir cambios de estabilidad para cientos de proteínas a la vez, demuestra que los efectos del hacinamiento son complejos y específicos de cada proteína, y probablemente impulsados por interacciones directas tanto como por el simple empaquetamiento. Cuando los investigadores diseñen fármacos, enzimas industriales o microbios diseñados, reconocer esta realidad abarrotada será crucial para predecir cómo se comportan realmente las proteínas en sistemas vivos.
Cita: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
Palabras clave: hacinamiento molecular, estabilidad de proteínas, perfilado térmico del proteoma, proteoma bacteriano, entorno celular