Clear Sky Science · es
La deficiencia de Negr1 altera la señalización del glutamato y la vía de la quinurenina en un modelo murino de trastornos psiquiátricos
Por qué importa este estudio cerebral
Muchas enfermedades mentales comunes, desde la depresión hasta la esquizofrenia, se asocian con cambios sutiles en la forma en que las células cerebrales se comunican entre sí. Este estudio examina un gen de riesgo, llamado NEGR1, en ratones para ver cómo su pérdida modifica la química cerebral y el comportamiento. Al seguir el movimiento de estos animales tras administrarles un fármaco que interrumpe brevemente un receptor clave del cerebro, y midiendo los metabolitos relacionados, los investigadores revelan cómo la genética, el sexo y el metabolismo cerebral pueden combinarse para moldear la vulnerabilidad a los trastornos psiquiátricos.
Un gen que mantiene el equilibrio de las señales cerebrales
El gen NEGR1 codifica una proteína en la superficie celular que ayuda a las neuronas a formar y estabilizar conexiones. Trabajos previos mostraron que eliminar este gen en ratones altera la estructura cerebral, reduce determinadas conexiones inhibidoras (GABA) y cambia las respuestas a fármacos vinculados a la dopamina, como la anfetamina. Dado que estos cambios apuntan a un desplazamiento hacia señales excitatorias más intensas, el equipo se centró en otro sistema excitatorio mayor: el glutamato y sus receptores NMDA, que son centrales para el aprendizaje, la memoria y el comportamiento flexible. También examinaron la “vía de la quinurenina”, una ruta metabólica que degrada el aminoácido triptófano en compuestos que pueden potenciar o bloquear los receptores NMDA.
Probar el comportamiento con un fármaco que altera la mente
Para sondear la función del receptor NMDA, los investigadores usaron MK-801, un fármaco conocido que bloquea brevemente estos receptores y puede imitar aspectos del desequilibrio del glutamato observado en afecciones psiquiátricas. Ratones machos y hembras portaban bien el gen Negr1 normal o bien carecían por completo de él. Los animales recibieron inyecciones diarias de MK-801 y se probaron en un campo abierto, donde se registró automáticamente su movimiento total, el tiempo en las esquinas y las rotaciones similares a giros. En los machos sin exposición previa al fármaco, una sola dosis de MK-801 produjo un estallido de actividad mayor en los ratones deficientes en Negr1 que en los normales, lo que sugiere que sus cerebros eran inusualmente sensibles a esta perturbación de la señalización del glutamato.
Un patrón sorprendente de tolerancia rápida
Cuando se administró MK-801 de forma repetida, el patrón cambió. En los machos, la actividad se disparó algunos días pero disminuyó cada segundo día, formando un patrón en zigzag que sugiere una tolerancia rápida y parcial a los efectos del fármaco. A lo largo de nueve días, los machos normales mostraron una respuesta en aumento consistente con sensibilización, mientras que los machos deficientes en Negr1 mostraron una acumulación de actividad atenuada y cambios más suaves de un día a otro, lo que apunta a una sensibilidad alterada del receptor NMDA. Las hembras de ambos genotipos se adaptaron aún más rápido: alrededor del quinto día, MK-801 dejó de producir efectos conductuales fuertes, por lo que se interrumpió el tratamiento. En todas las medidas, el sexo tuvo una influencia importante y los efectos claros del genotipo aparecieron principalmente en los machos.
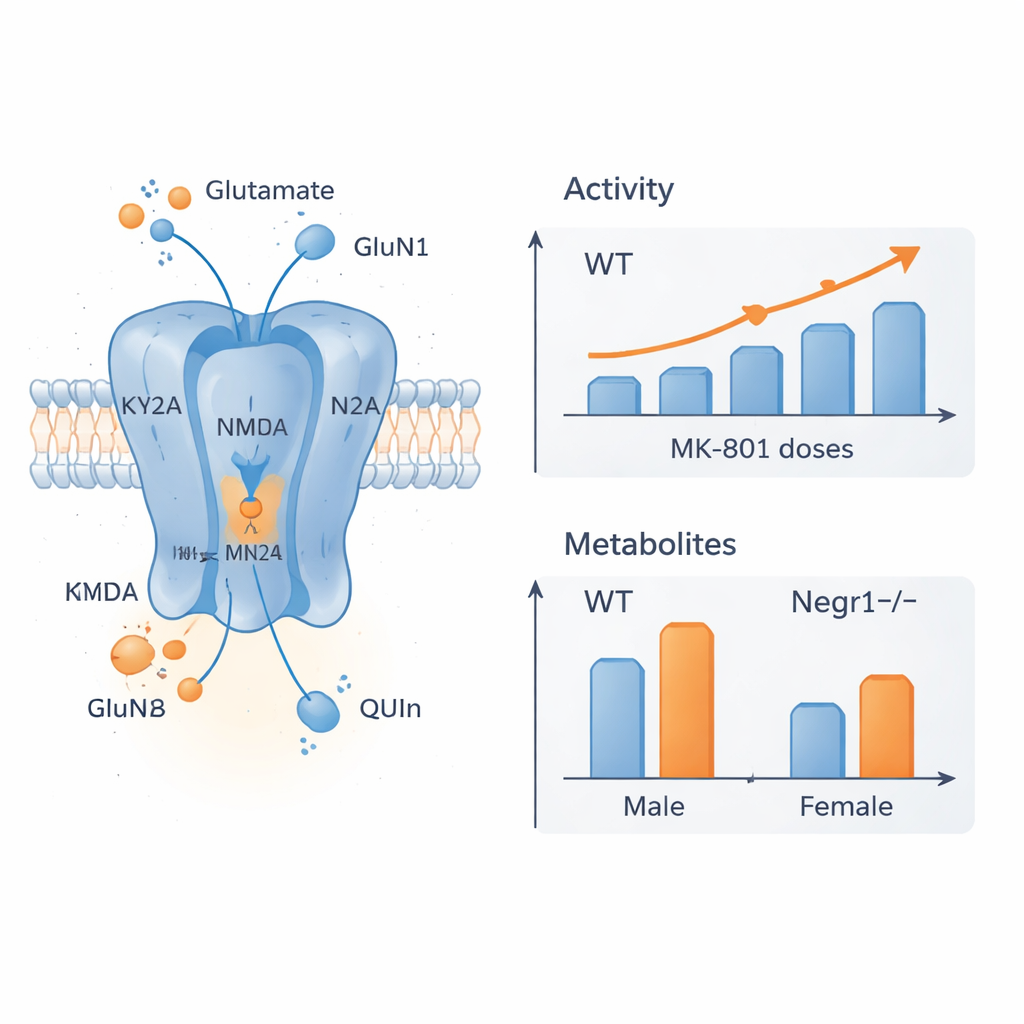
Desplazamientos en receptores y químicos cerebrales
Para descubrir qué estaba detrás de estas diferencias conductuales, el equipo midió la actividad génica de subunidades clave del receptor NMDA y de una enzima que produce D-serina, un co-señal para estos receptores. Se centraron en regiones cerebrales cruciales para el estado de ánimo y la cognición: la corteza frontal y el hipocampo. En la corteza frontal, las hembras deficientes en Negr1 tratadas con MK-801 mostraron una reducción en la expresión de subunidades receptoras centrales, lo que sugiere que sus cerebros ajustan la composición de los receptores en respuesta tanto a la mutación como al fármaco. En el hipocampo de los machos, los ratones deficientes en Negr1 presentaron una expresión basal más alta de ciertas subunidades NMDA, en línea con pruebas anteriores de mayor disponibilidad de receptores; el tratamiento con MK-801 luego redujo esos niveles hacia la normalidad. En paralelo, análisis químicos detallados de sangre y múltiples regiones cerebrales revelaron que varios metabolitos de la vía de la quinurenina y el propio glutamato estaban alterados de forma específica según el sexo y la región, con la corteza frontal como la más afectada y algunos cambios volviéndose más marcados con la edad.
Qué significa esto para entender las enfermedades mentales
En conjunto, estos hallazgos presentan a NEGR1 como un organizador molecular que ayuda a mantener el equilibrio entre las señales excitatorias e inhibitorias del cerebro, en parte modulando la función del receptor NMDA y el metabolismo del triptófano. Cuando falta Negr1, los ratones responden de forma distinta al bloqueo del receptor NMDA, muestran cambios en los químicos cerebrales dependientes del sexo y desarrollan tolerancia de maneras inusuales. Para el lector no experto, el mensaje clave es que un único gen de riesgo no actúa de forma aislada: sus efectos dependen del sexo, la región cerebral y el estado metabólico. Este trabajo refuerza la idea de que dirigir vías vinculadas a NEGR1 —en lugar de centrarse solo en receptores individuales— podría, a la larga, ayudar a personalizar los tratamientos para enfermedades mentales marcadas por desequilibrios del glutamato.
Cita: Kuuskmäe, C., Mikheim, K., Mohammadrahimi, N. et al. Negr1 deficiency alters glutamate signalling and kynurenine pathway in a mouse model of psychiatric disorders. Sci Rep 16, 5317 (2026). https://doi.org/10.1038/s41598-026-35968-7
Palabras clave: gen NEGR1, receptor NMDA, señalización del glutamato, vía de la quinurenina, trastornos psiquiátricos