Clear Sky Science · es
APOBEC3B aumenta la eficacia de los inhibidores de PARP en la eliminación de la célula madre del cáncer de ovario
Por qué esta investigación importa para las pacientes con cáncer de ovario
Muchas mujeres con cáncer de ovario avanzado responden bien al principio a fármacos modernos llamados inhibidores de PARP, que atacan vulnerabilidades en el sistema de reparación del ADN del tumor. Sin embargo, con el tiempo la enfermedad suele reaparecer a medida que las células cancerosas aprenden a sobrevivir a estos tratamientos. Este estudio explora un aliado inesperado dentro de las propias células tumorales: una enzima que altera el ADN llamada APOBEC3B, y muestra que, en las condiciones adecuadas, puede facilitar la eliminación de las células madre del cáncer de ovario con inhibidores de PARP.
Un cáncer letal que vuelve una y otra vez
El carcinoma seroso de alto grado es la forma más común y más mortal de cáncer de ovario. Suele diagnosticarse tarde, cuando la enfermedad ya se ha extendido en el abdomen, y más del 80 % de las pacientes con enfermedad avanzada recaen en cinco años. Un sospechoso clave en estas recaídas es una pequeña población de “células madre cancerosas”. Estas células pueden autorrenovarse, sobrevivir a la quimioterapia y reconstruir tumores tras el tratamiento. Entender qué hace que estas células con características de madre sean resistentes—y cómo atacarlas—es esencial para mejorar la supervivencia a largo plazo.
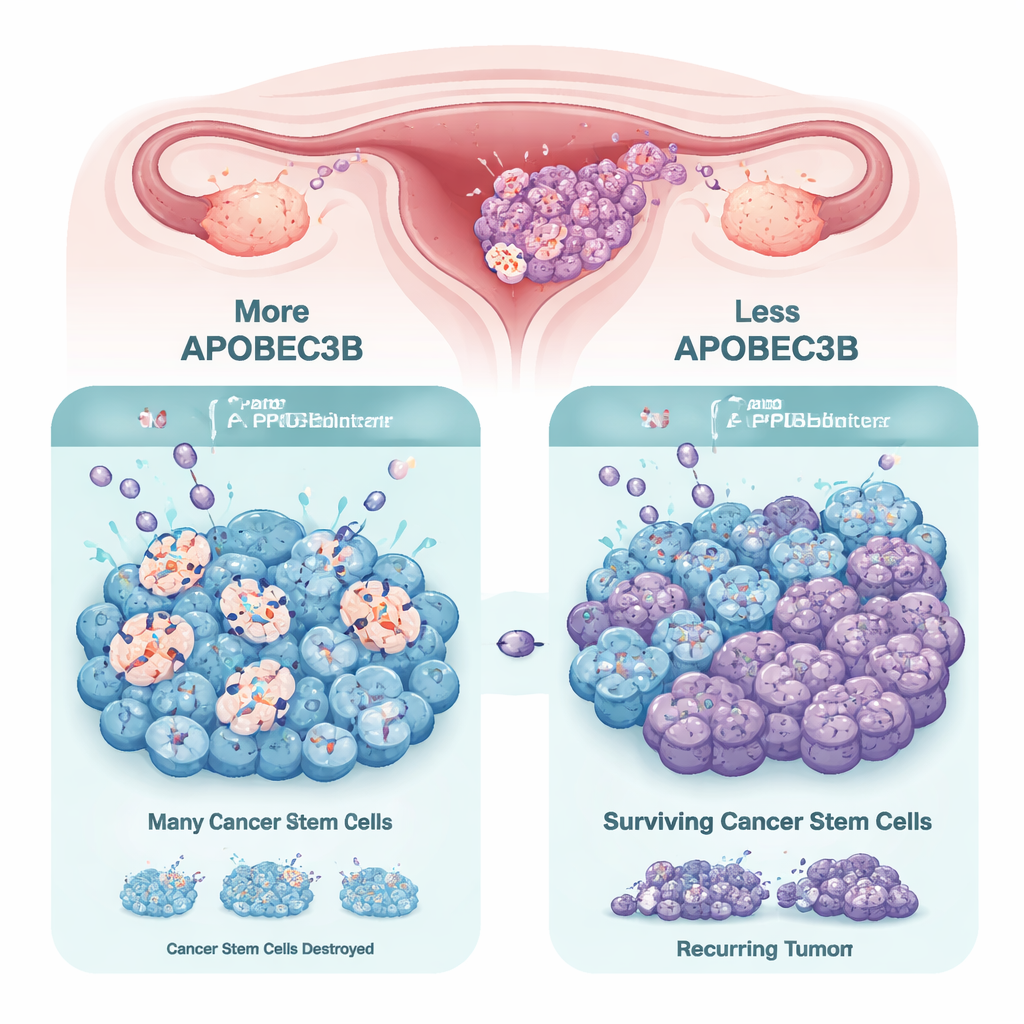
Una enzima mutante con doble vida
La familia de enzimas APOBEC3 normalmente ayuda a proteger nuestras células de virus cambiando letras específicas del ADN, lo que puede introducir mutaciones. En muchos cánceres, un miembro, APOBEC3B, está sobreactivado y contribuye al daño en el ADN y al caos genético, lo que puede impulsar la evolución tumoral y la resistencia a las terapias. En tumores de ovario y modelos derivados de pacientes, los investigadores confirmaron que APOBEC3B suele ser la enzima APOBEC3 más abundante. Sin embargo, al comparar células tumorales ordinarias con “esferas” tumorales parecidas a células madre cultivadas en tres dimensiones, descubrieron que las células con rasgos de madre reducen consistentemente la expresión de APOBEC3B. Esto sugiere que las células madre cancerosas pueden disminuir su carga mutacional para preservar su supervivencia y capacidad de autorrenovación.
Reducir APOBEC3B hace a las células madre más resistentes
Para probar si APOBEC3B influye realmente en la condición de madre, el equipo usó herramientas genéticas para disminuir su expresión en modelos de cáncer de ovario derivados de pacientes y en líneas celulares establecidas. Cuando los niveles de APOBEC3B se redujeron, las células cancerosas formaron esferas tumorales con mayor eficiencia y mostraron niveles más altos de marcadores clásicos de stemness como SOX2, OCT4 y NANOG. La fracción de células con propiedades semejantes a las de las células madre aumentó, lo que indica que la pérdida de APOBEC3B ayuda a las células tumorales a cambiar hacia un estado más resistente y similar al de las células madre. En ratones, los tumores carentes de APOBEC3B no crecieron más rápido por sí mismos, pero se comportaron de forma distinta cuando se trataron con inhibidores de PARP.
Más APOBEC3B, más daño—y mejor respuesta al fármaco
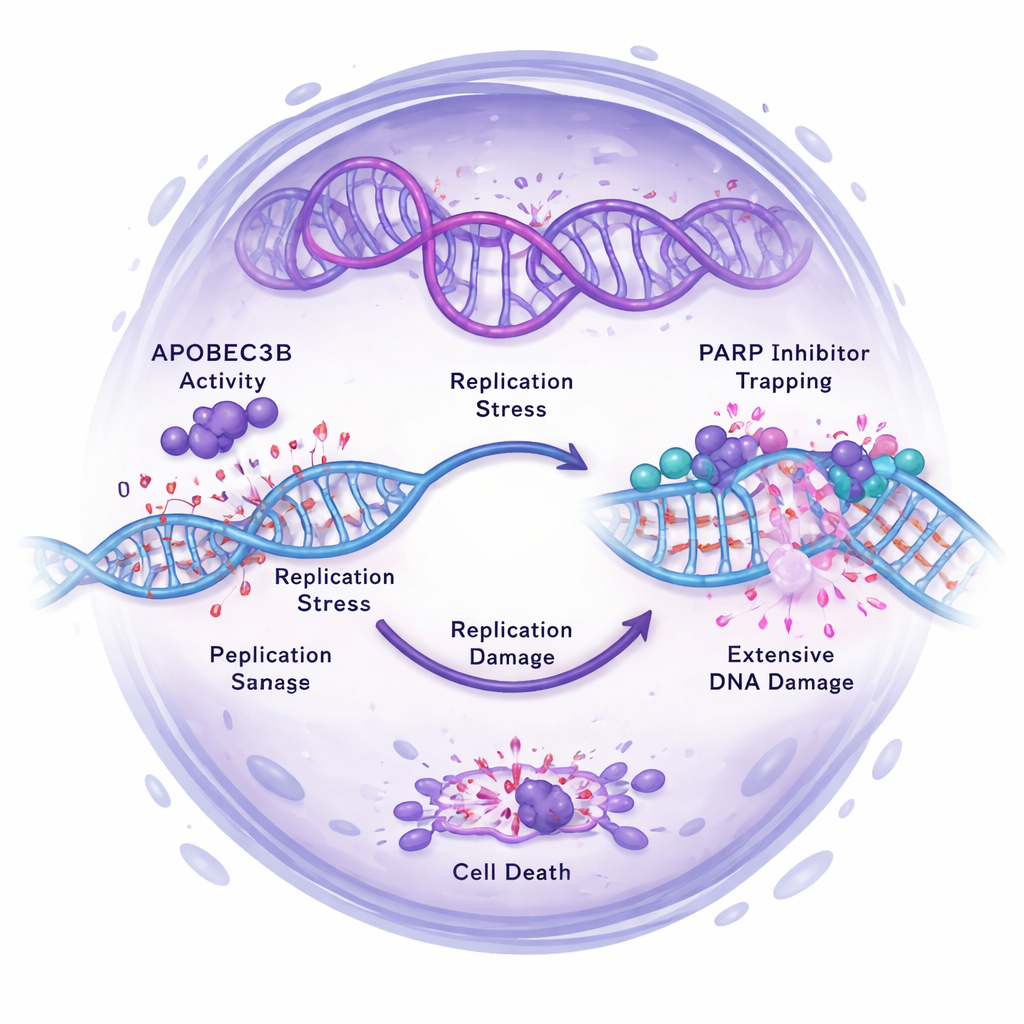
Los investigadores preguntaron luego cómo APOBEC3B afecta el rendimiento de inhibidores de PARP como Olaparib, que actúan bloqueando la reparación del ADN y empujando a las células tumorales hacia un daño letal en el ADN. En múltiples líneas celulares de cáncer de ovario, reducir APOBEC3B hizo que las células fueran más resistentes a los inhibidores de PARP, especialmente en esferas 3D enriquecidas en células con rasgos de madre. Por el contrario, aumentar APOBEC3B sensibilizó a ciertas células a los inhibidores de PARP, reduciendo mucho su supervivencia. En experimentos en ratones, los tumores con APOBEC3B normal se redujeron o ralentizaron drásticamente con Olaparib, mientras que los tumores deficientes en APOBEC3B continuaron creciendo a pesar del tratamiento. Los análisis moleculares mostraron la razón: altos niveles de APOBEC3B intensificaban el estrés de replicación del ADN y las roturas de doble cadena, activando vías de señalización de daño en el ADN. Cuando APOBEC3B se redujo, el daño en el ADN inducido por inhibidores de PARP, la activación de puntos de control y el estrés de replicación disminuyeron, y las células tenían más probabilidad de detenerse de forma segura en el ciclo celular en lugar de morir.
Una nueva forma de pensar sobre la resistencia y el diseño de tratamientos
Al profundizar con secuenciación de ARN, el equipo encontró que la combinación de pérdida de APOBEC3B e inhibición de PARP reconfiguró muchos genes implicados en la replicación y reparación del ADN, apoyando la idea de que APOBEC3B amplifica los efectos perjudiciales de los inhibidores de PARP sobre los genomas de las células tumorales. También probaron si otra enzima reparadora, UNG, era necesaria para este efecto y hallaron que la sensibilidad a inhibidores de PARP en células con alto APOBEC3B era en gran parte independiente de UNG. En conjunto, los datos señalan al estrés de replicación impulsado por APOBEC3B—no solo su actividad mutacional—como el socio principal que ayuda a los inhibidores de PARP a matar a las células madre del cáncer de ovario.
Qué significa esto para las pacientes y futuras terapias
Para el público general, el mensaje es que no todo el caos genético dentro de un tumor es necesariamente mala noticia. En este estudio, niveles más altos de la enzima mutadora APOBEC3B hicieron en realidad que las células madre del cáncer de ovario fueran más vulnerables a los inhibidores de PARP al sobrecargar su capacidad de reparación del ADN. Cuando APOBEC3B se redujo, las células madre cancerosas se volvieron más parecidas a células madre y mejoraron su capacidad para resistir el tratamiento. Estos hallazgos sugieren que medir los niveles de APOBEC3B podría ayudar a predecir qué pacientes se beneficiarán más de los inhibidores de PARP, y que el momento o la combinación de futuros fármacos dirigidos a APOBEC3B con inhibidores de PARP debe manejarse con cuidado. Aprovechar el efecto de “auto-sabotaje” de APOBEC3B en las células tumorales podría abrir nuevas estrategias para prevenir recaídas y eliminar más eficazmente las raíces de los tumores de ovario.
Cita: Rivera, M., Liu, L., Enlund, S. et al. APOBEC3B enhances the efficacy of PARP inhibitors in elimination of ovarian cancer stem cell. Sci Rep 16, 5194 (2026). https://doi.org/10.1038/s41598-026-35939-y
Palabras clave: cáncer de ovario, inhibidores de PARP, células madre cancerosas, APOBEC3B, resistencia a fármacos