Clear Sky Science · es
La agregación supramolecular de la acuaporina-4 determina la migración colectiva y la mecánica de los astrocitos
Cómo se mueven juntas las células cerebrales para reparar
Cuando el cerebro resulta herido o inflama, sus células de soporte —los astrocitos— acuden rápido para proteger, reparar o aislar las zonas dañadas. Este estudio explora un factor sorprendente que ayuda a determinar qué tan bien se desplazan estas células en grupo: pequeños canales de agua llamados acuaporina-4 (AQP4). Al observar cómo las moléculas de AQP4 se agrupan o se dispersan en las membranas de los astrocitos, los investigadores revelan cómo la “plomería” del agua del cerebro ayuda a coordinar el movimiento colectivo celular y cómo la inflamación crónica puede descarrilar este proceso.
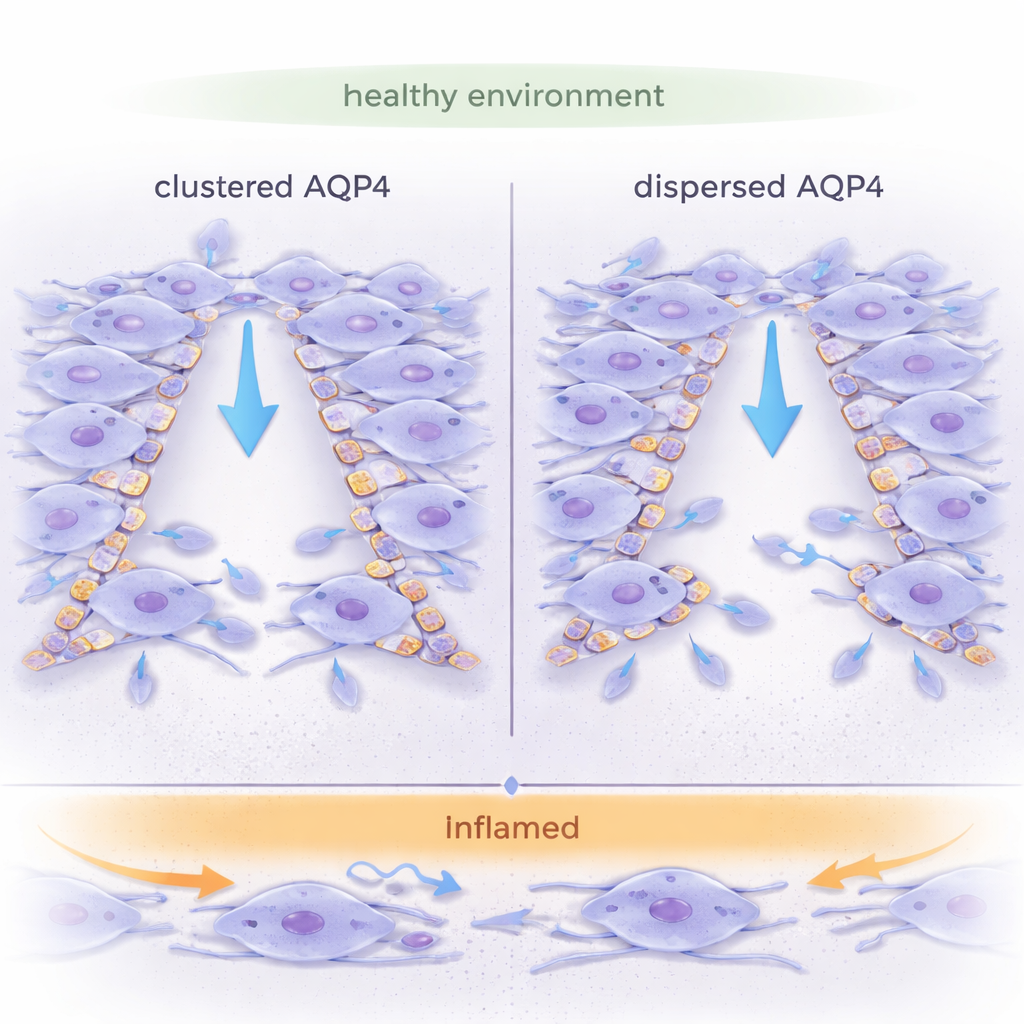
Portales de agua en las células cerebrales
Los astrocitos son células en forma de estrella que ayudan a mantener el equilibrio del cerebro, guiar su desarrollo y responder a las lesiones. Están llenos de AQP4, una proteína que forma poros que permiten que el agua entre y salga rápidamente de la célula. A diferencia de muchos otros canales de agua, la AQP4 puede ensamblarse en grandes parches cristalinos llamados arreglos ortogonales de partículas (OAPs), o permanecer como unidades más pequeñas y dispersas (tetrámeros). Se cree que la organización de la AQP4 influye en cómo las células cambian de forma y se mueven, pero la mayor parte de los trabajos anteriores se centraron en células individuales. Este estudio planteó una pregunta más realista: ¿cómo afecta la organización de la AQP4 a la forma en que láminas enteras de astrocitos migran juntas, como lo harían al cerrar una herida en el tejido cerebral?
Probando el movimiento celular en salud e inflamación
Los investigadores cultivaron dos tipos de astrocitos de ratón: células normales que pueden formar arreglos de AQP4 y células modificadas genéticamente (OAP-nulas) que carecen de la principal variante formadora de arreglos de AQP4 y, por tanto, contienen mayoritariamente tetrámeros dispersos. Después crearon un “raspado” en una capa densa de células, imitando una herida, y observaron qué tan rápido y de forma uniforme cerraban la brecha. Para reproducir un cerebro con lesión crónica, además mantuvieron algunas cultivos expuestos durante una semana a dos moléculas inflamatorias, IL-1β y TNF-α, antes de las pruebas. Usando imágenes en lapso de tiempo y un método de visión por computador llamado velocimetría de imagen por partículas, cuantificaron no solo cuánto y qué tan rápido se movían las células, sino también cuán recto, coordinado o deformado era su movimiento a lo largo de toda la lámina.
Canales dispersos, movimiento más fluido
En condiciones no inflamadas, los astrocitos con AQP4 dispersa (OAP-nulas) fueron notablemente mejores en la migración colectiva: cerraron las heridas más rápido y se movieron de forma más dirigida y lineal que las células con grandes arreglos de AQP4. Su frente avanzado era suave y continuo, y las células vecinas se desplazaban de forma cohesionada, como una “lámina”. En contraste, los astrocitos con AQP4 agrupada (tipo salvaje) mostraron un frente más irregular, con muchas protuberancias individuales y distorsiones internas, lo que sugiere que las células tiraban en direcciones ligeramente distintas. Las mediciones de deformación dentro de la capa celular confirmaron que las láminas OAP-nulas experimentaban menos tironeos internos y un movimiento más uniforme y coordinado.
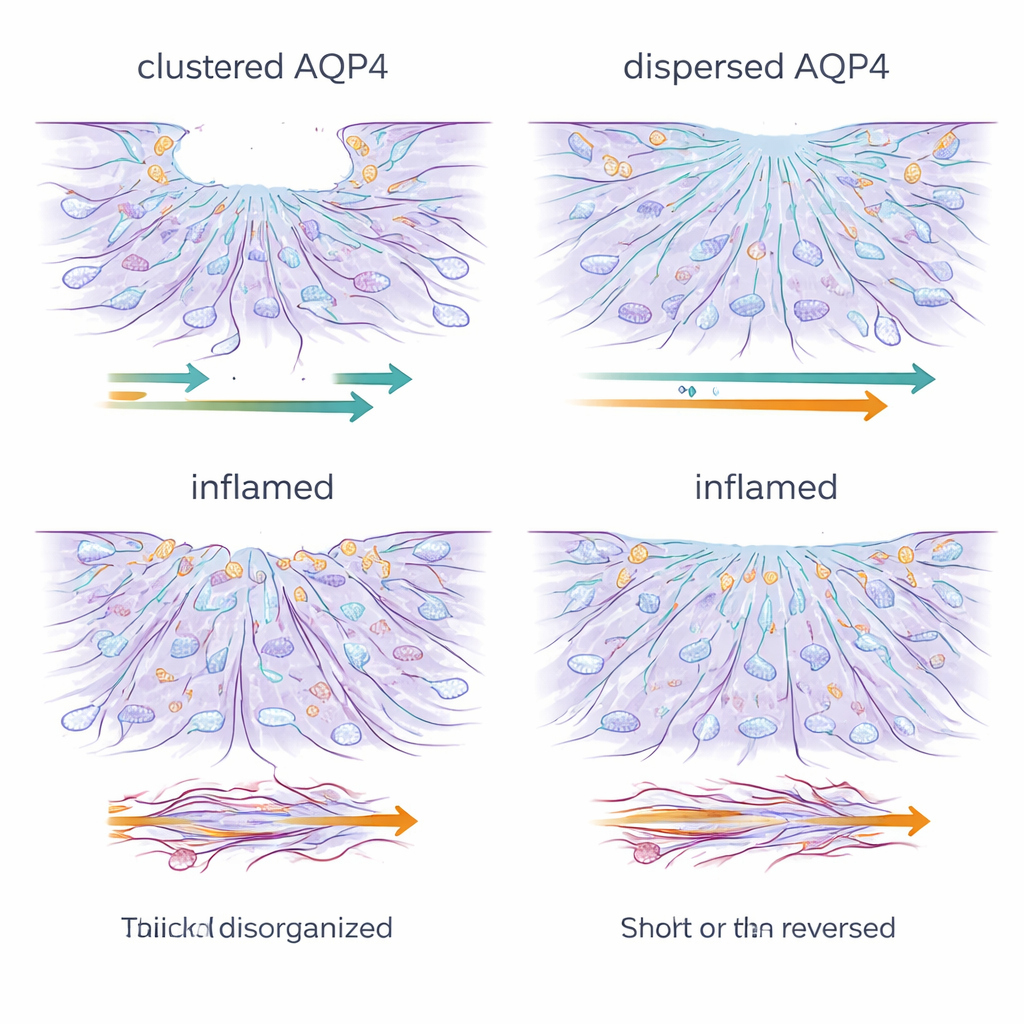
La inflamación frena y desordena al equipo de reparación
La exposición crónica a señales inflamatorias cambió profundamente este panorama. Independientemente de la organización de la AQP4, los astrocitos tratados se convirtieron en malos reparadores: prácticamente no se movían e incluso, en algunos casos, retrocedían, ampliando la brecha. La microscopía mostró que las finas y dinámicas estructuras del borde celular necesarias para avanzar —lamelipodios y filopodios— se perdieron y fueron reemplazadas por gruesas y rígidas fibras de tensión de actina, la principal proteína estructural celular. Al mismo tiempo, los niveles de AQP4 y de conexina-43, una proteína clave que forma canales de comunicación entre astrocitos, cayeron drásticamente. La red de uniones comunicantes que normalmente ayuda a los astrocitos a actuar como una unidad coordinada se vio alterada, y experimentos de transferencia de tintes confirmaron que la comunicación célula–célula a larga distancia quedó gravemente debilitada.
Por qué importa esto para la salud cerebral
Estos hallazgos sugieren que no solo importa cuánto AQP4 tiene una célula, sino cómo está organizada para que los astrocitos se muevan eficazmente en grupo. La AQP4 dispersa parece reducir la resistencia interna entre células y promover un movimiento más recto y coordinado, mientras que los grandes agregados se asocian con un estilo de movimiento más errático y tenso. La inflamación crónica anula en gran medida estas ventajas al remodelar el citoesqueleto celular, silenciar los canales de agua y de comunicación, y convertir un equipo de reparación organizado en una lámina rígida y pobremente conectada. Para no especialistas, la conclusión es que los canales de agua y los sistemas de comunicación célula–célula del cerebro hacen mucho más que apoyar pasivamente a las neuronas: modelan activamente cómo las células de soporte se movilizan tras una lesión. Entender y, eventualmente, modular la organización de la AQP4 y las señales inflamatorias podría abrir nuevas vías para mejorar la reparación cerebral, limitar la formación de cicatrices o incluso influir en la propagación de tumores cerebrales.
Cita: Barile, B., Mennona, N.J., Mola, M.G. et al. Supramolecular aggregation of aquaporin-4 shapes astrocyte collective migration and mechanics. Sci Rep 16, 6021 (2026). https://doi.org/10.1038/s41598-026-35900-z
Palabras clave: astrocitos, acuaporina-4, inflamación cerebral, migración celular, cicatriz glial